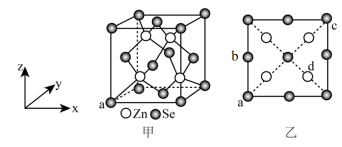
我国科学家在相当于110万大气压下合成了一种稳定的氦钠化合物,结构如图所示:小球代表Na,正方体代表He,小正方体代表共用电子,共用电子被迫集中在晶体结构的立方空间内。下列说法错误的是


| A.该物质的化学式为Na2He | B.极高的压力,可以影响He的化学性质 |
| C.该物质固态时能够导电 | D.Na的配位数为4 |
更新时间:2022-07-15 12:36:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特征:Fe2+位于立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,M为+1价。晶体的晶胞结构如图所示,下列说法不正确的是


| A.该晶体中既有离子键又有极性共价键 |
| B.与每个Fe2+距离相等且最近的CN-有6个 |
| C.M+离子位于晶胞体心 |
| D.晶体的化学式可表示为M2Fe (CN)3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
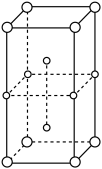
【推荐2】下列有关晶体的说法中正确的是

| A.分子晶体的分子内均存在共价键,可能存在氢键 |
| B.通过晶体X射线衍射实验,可得出晶体的晶胞结构 |
| C.分子晶体的结构为分子密堆积 |
| D.Na和Cl在50GPa~300GPa的高压下反应生成晶体的一种晶胞如上图,该晶体的化学式为NaCl3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列说法正确的是
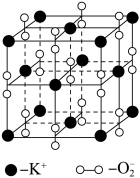

A.超氧化钾化学式为KO2,每晶胞含14个K+和14个O |
| B.超氧化钾固体属于离子晶体,其配位数为8 |
| C.晶体中与每个K+距离最近的K+有6个 |
| D.晶体中,0价氧原子与-2价氧原子的数目比为3∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】红镍矿是一种重要的含镍矿物,其主要成分的晶胞如下图所示,下列说法正确的
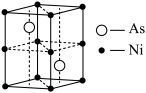

| A.该化合物的化学式为Ni2As |
| B.该化合物中As的配位数为8 |
| C.该化合物中Ni的配位数为6 |
| D.该晶胞平均占有5个Ni原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】晶体的结构如下图所示,下列说法中不 正确的是


| A.在图①NaCl晶体中,距Na+最近的Cl-形成正八面体 |
| B.在图②CaF2晶体中,每个晶胞平均占有4个Ca2+ |
| C.在图③金刚石晶体中,碳原子与碳碳键个数的比为1∶2 |
| D.图④表示铜晶体为面心立方堆积,铜原子的配位数为8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】锌的性质与铝相似,可发生反应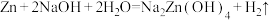 。下列关于反应物和产物的性质说法正确的是
。下列关于反应物和产物的性质说法正确的是
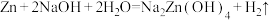 。下列关于反应物和产物的性质说法正确的是
。下列关于反应物和产物的性质说法正确的是| A.五种物质中有两种离子晶体、三种分子晶体 |
B.NaOH晶胞结构与NaCl晶胞结构相似,因此NaOH晶体中 配位数是8 配位数是8 |
C.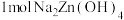 中存在4mol配位键 中存在4mol配位键 |
| D.锌的熔点高于水的熔点,是因为锌的相对原子质量大,分子间作用力大的原因 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是( )
①原子晶体中只存在非极性共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④干冰升华时,分子内共价键会发生断裂
⑤晶格能由大到小顺序:NaF>NaCl>NaBr>NaI
⑥分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
⑦分子晶体中分子间作用力越大,分子越稳定
①原子晶体中只存在非极性共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④干冰升华时,分子内共价键会发生断裂
⑤晶格能由大到小顺序:NaF>NaCl>NaBr>NaI
⑥分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
⑦分子晶体中分子间作用力越大,分子越稳定
| A.①②③⑥ | B.①②④ | C.③⑤⑥⑦ | D.③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,晶胞如图(a)所示,其中Ti的电负性为1.5,一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子,其晶胞如图(b)所示。下列有关说法正确的是
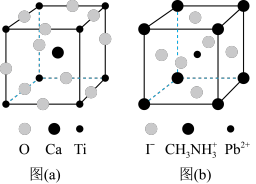

| A.基态Ti原子的核外电子排布式为1s22s22p63s23p64s23d2 |
| B.TiF4、TiCl4、 TiBr4、 TiI4熔点依次升高 |
| C.用图(b) 晶胞中的金属卤化物光电材料制作的太阳能电池,在使用过程中产生单质铅和碘,会降低了器件效率和使用寿命。 |
| D.图(b)晶胞中Pb2+与图(a) 晶胞中Ca的空间位置相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下表数据是部分物质对应的熔点,下列说法正确的是
| 物质 | AlF3 | AlCl3 | BF3 | NF3 |
| 熔点/℃ | 1291 | 160 | -127 | -207 |
| A.键长:B-F<B-Cl,推测BCl3的熔点低于BF3的 |
| B.因为BF3、NF3都为XY3型化合物,且熔点较低,所以两者的空间结构相同 |
| C.NCl3和NF3结构相似,NCl3的相对分子质量大于NF3的,推测NCl3的熔点将高于-207℃ |
| D.由于AlF3、AlCl3的熔点相差很大,推测两者的晶体类型不同且AlCl3为非电解质 |
您最近一年使用:0次

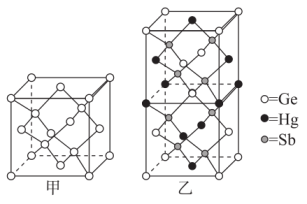
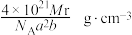

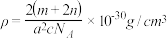
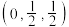 。下列说法正确的是
。下列说法正确的是