根据要求完成。
(1)基态氟原子氟原子有_______ 种不同能量的电子,价电子排布图为_______ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:_______ ; 中有
中有_______ 种运动状态不同的电子。
(3)基态硼原子的核外电子排布图为_______ 。
(4)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(5)锰元素在周期表中的位置为_______ ;属于_______ 区元素(填“s”“p”“d”“ds”或“f”)。铜、锌两种元素的第一电离能、第二电离能如表所示:
铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是_______ 。
(1)基态氟原子氟原子有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
 中有
中有(3)基态硼原子的核外电子排布图为
(4)基态K原子中,核外电子占据最高能层的符号是
(5)锰元素在周期表中的位置为
电离能/ |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
更新时间:2022-07-01 23:23:59
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
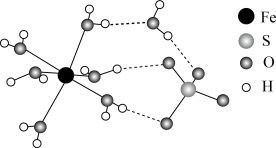
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的 是______________ (填元素符号)。
(2)③的气态氢化物的电子式______________ ,②④形成的可溶于水的气态化合物的结构式______________ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________ (填物质的化学式),酸性最强的含氧酸为______________ (填物质的化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为
_______ ,有_______ 个未成对电子。
(2)基态氮原子价层电子的轨道表示式(电子排布图)为_______ 。
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为
(2)基态氮原子价层电子的轨道表示式(电子排布图)为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请填空:
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是_______ (填离子符号)。
(2)Fe基态核外电子排布式为_______ 。
(3)Al在周期表中的位置_______ ;基态Zn的价层电子排布式_______ 。
(4)基态Ti原子的核外电子排布式为_______ 。
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(2)Fe基态核外电子排布式为
(3)Al在周期表中的位置
(4)基态Ti原子的核外电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】以第3周期元素为例,核外电子排布、原子半径如何变化?
| 第三周期元素 | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar |
| 原子结构示意图 | ||||||||
| 核外电子排布 | ||||||||
| 原子半径 | — | |||||||
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】V的价电子排布图___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:_______________________________ ,核外电子运动状态有_______ 种。
(2)B是原子序数为35的元素,其原子中有___________ 个电子层,有_________ 个能级。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为_________________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应方程式:____________ 。
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:
(2)B是原子序数为35的元素,其原子中有
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为
您最近一年使用:0次
【推荐3】根据物质结构有关性质和特点,回答以下问题:
(1)[Co(N3)(NH3)5]SO4中Co的配位数为___ ,其内外界之间的化学键类型为___ (填离子键、共价键、配位键)。
(2)向硫酸铜溶液中加入过量氨水后,再加少量乙醇得到的深蓝色晶体[Cu(NH3)4]SO4∙H2O中,与Cu2+形成配位键的原子是___ (填元素符号)。
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于下列___ (填字母)。
a.水 b.CCl4 c.C6H6(苯) d.NiSO4溶液
(4)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如图所示,该分子中存在的化学键为___ (填选项字母)

a.σ键 b.π键 c.离子键 d.配位键
(5)过渡元素Fe基态原子价电子轨道表达式为___ 。第四电离能I4(Co)<I4(Fe),其原因是___ 。
(1)[Co(N3)(NH3)5]SO4中Co的配位数为
(2)向硫酸铜溶液中加入过量氨水后,再加少量乙醇得到的深蓝色晶体[Cu(NH3)4]SO4∙H2O中,与Cu2+形成配位键的原子是
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于下列
a.水 b.CCl4 c.C6H6(苯) d.NiSO4溶液
(4)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如图所示,该分子中存在的化学键为

a.σ键 b.π键 c.离子键 d.配位键
(5)过渡元素Fe基态原子价电子轨道表达式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1)
请回答下列问题:
(1)在周期表中,最可能处于同一族的是____
A.Q和R B.S和T
C.T和U D.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是____
A.U2++2e-→U B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是____
A.UCl4 B. RCl C.SCl3D.TCl
(4)S元素最可能是_____
A.s区元素 B.p区元素
C.过渡金属 D.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是____
A.硼(1s22s22p1) B.铍(1s22s2) C.锂(1s22s1) D.氦(1s2)
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
请回答下列问题:
(1)在周期表中,最可能处于同一族的是
A.Q和R B.S和T
C.T和U D.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是
A.U2++2e-→U B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是
A.UCl4 B. RCl C.SCl3D.TCl
(4)S元素最可能是
A.s区元素 B.p区元素
C.过渡金属 D.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是
A.硼(1s22s22p1) B.铍(1s22s2) C.锂(1s22s1) D.氦(1s2)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Zn2+、三乙撑二胺和对苯二甲酸根离子可形成晶体M,其晶胞示意图如图。
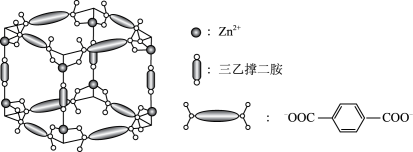
(1)Zn2+的价层电子排布式是_____ 。
(2)C、N、O的电负性从大到小 的顺序是_____ ;C、N、O的第一电离能从大到小 的顺序是_____ 。
(3)三乙撑二胺(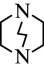 )与
)与 能形成配位键的原因是
能形成配位键的原因是_____ 。
(4)下列事实可用“水分子间存在氢键”解释的是_____ (填字母序号 )。
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(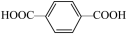 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为_____ ,羧基上碳原子的杂化方式为____ ,对苯二甲酸中最多有_____ 个原子共平面。

(1)Zn2+的价层电子排布式是
(2)C、N、O的电负性
(3)三乙撑二胺(
 )与
)与 能形成配位键的原因是
能形成配位键的原因是(4)下列事实可用“水分子间存在氢键”解释的是
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(
 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】丁二酮肟可用于镍的检验和测定,其结构式如图:
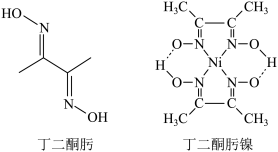
(1)Ni元素基态原子电子排布式为____ ,价电子排布图为:____ ,其中未成对电子数为:____ 。C、N、O第一电离能由大到小的顺序是____ 。
(2)1mol丁二酮肟含有的σ键数目是____ ,已知CN-与N2互为等电子体。推算HCN分子中σ和π键数目之比为:____ 。
(3)与氮原子同族的P的氢化物,它的空间立体构型是:____ ,它是含有____ 键的____ 分子。
(4)CO 的杂化方式是:
的杂化方式是:____ ,它的空间构型是:____ 。
(5)丁二酮肟镍分子内含有的作用力有____ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力

(1)Ni元素基态原子电子排布式为
(2)1mol丁二酮肟含有的σ键数目是
(3)与氮原子同族的P的氢化物,它的空间立体构型是:
(4)CO
 的杂化方式是:
的杂化方式是:(5)丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
您最近一年使用:0次

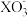 +6H+=3X2+3H2O,短周期元素X在周期表中的位置是
+6H+=3X2+3H2O,短周期元素X在周期表中的位置是

