Ⅰ.已知下列物质均由短周期元素组成,X无论是盐酸还是氢氧化钠,转化均能进行,又已知C的相对分子质量比D少16,A、B、C、D、E中均含有同一元素。_______ 。
(2)当X是氢氧化钠溶液时,C的化学式_______ 。
(3)写出A和足量氢氧化钠在加热条件下反应的化学方程式_______ 。
Ⅱ.金属及其化合物用途广泛,研究金属的提取、冶炼意义重大。
(4)下列各组金属,冶炼方法一定不同的是_______ (填字母)。
a.Hg、Ag b.Na、Mg c.Al、Fe d.Na、Ca
(5)以铬铁矿(主要成分为FeO和 ,含有少量
,含有少量 、
、 等杂质)为主要原料生产化工原料重铬酸钠
等杂质)为主要原料生产化工原料重铬酸钠 并制取铬,其主要工艺流程如下:
并制取铬,其主要工艺流程如下: 氧化为
氧化为 。
。
①“操作②”是_______ 。
②工业上可用固体A制取粗硅,写出反应的化学方程式:_______ 。
③写出溶液D转化为溶液E过程中反应的离子方程式:_______ 。
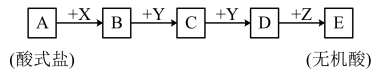
(2)当X是氢氧化钠溶液时,C的化学式
(3)写出A和足量氢氧化钠在加热条件下反应的化学方程式
Ⅱ.金属及其化合物用途广泛,研究金属的提取、冶炼意义重大。
(4)下列各组金属,冶炼方法一定不同的是
a.Hg、Ag b.Na、Mg c.Al、Fe d.Na、Ca
(5)以铬铁矿(主要成分为FeO和
 ,含有少量
,含有少量 、
、 等杂质)为主要原料生产化工原料重铬酸钠
等杂质)为主要原料生产化工原料重铬酸钠 并制取铬,其主要工艺流程如下:
并制取铬,其主要工艺流程如下: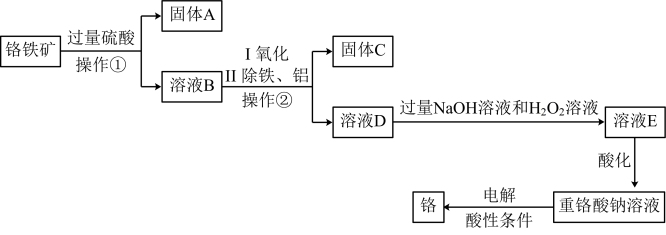
 氧化为
氧化为 。
。①“操作②”是
②工业上可用固体A制取粗硅,写出反应的化学方程式:
③写出溶液D转化为溶液E过程中反应的离子方程式:
21-22高一下·辽宁·期末 查看更多[3]
辽宁省协作校2021-2022学年高一下学期期末考试化学试题河南省开封市杞县新世纪中学2022—2023学年高二上学期开学联考化学试题(已下线)专题06 化学与可持续发展-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
更新时间:2022-07-19 08:07:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】铁酸钴是一种化学性质稳定、导电良好、电阻率极高、磁谱特性好的优良磁性材料。利用某含钴渣制备铁酸钴的生产流程如图所示。
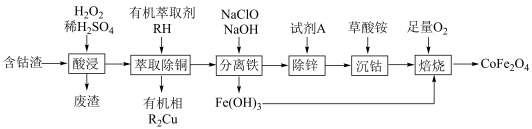
已知:①酸浸所得溶液中含有的阳离子为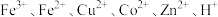 ;
;
②萃取除铜的过程可表示为: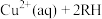 (有机相)、
(有机相)、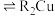 (有机相)
(有机相)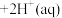 ;
;
③几种金属离子沉淀的相关 见下表:
见下表:
回答下列问题:
(1)要从萃取除铜所得有机相中得到硫酸铜溶液,主要操作步骤为:①加入试剂___________ ;②充分振荡、静置;③___________ ;若得到 硫酸铜溶液(密度为
硫酸铜溶液(密度为 ,质量分数为
,质量分数为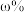 ),理论上可制得的蓝矾的质量为
),理论上可制得的蓝矾的质量为___________ 。
(2)“分离铁”中,写出通过氧化还原反应得到 的离子方程式
的离子方程式___________ ;该步骤中,应控制 的范围为
的范围为___________ 。
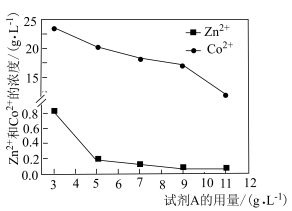
(3)一定条件下,试剂A的用量对锌钴分离的影响如下图所示。A的用量在___________  时效果最好,理由是
时效果最好,理由是___________ 。
(4)焙烧得到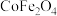 的化学方程式为
的化学方程式为___________ 。

已知:①酸浸所得溶液中含有的阳离子为
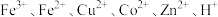 ;
;②萃取除铜的过程可表示为:
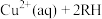 (有机相)、
(有机相)、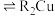 (有机相)
(有机相)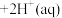 ;
;③几种金属离子沉淀的相关
 见下表:
见下表:| 离子 |  |  |  |  |  |
开始沉淀时的 | 6.2 | 5.3 | 6.5 | 2.1 | 7.2 |
沉淀完全时的 | 8.2 | 6.7 | 9.9 | 3.2 | 9.4 |
(1)要从萃取除铜所得有机相中得到硫酸铜溶液,主要操作步骤为:①加入试剂
 硫酸铜溶液(密度为
硫酸铜溶液(密度为 ,质量分数为
,质量分数为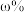 ),理论上可制得的蓝矾的质量为
),理论上可制得的蓝矾的质量为(2)“分离铁”中,写出通过氧化还原反应得到
 的离子方程式
的离子方程式 的范围为
的范围为(3)一定条件下,试剂A的用量对锌钴分离的影响如下图所示。A的用量在
 时效果最好,理由是
时效果最好,理由是
(4)焙烧得到
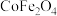 的化学方程式为
的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】校化学兴趣小组承担了某项研究课题的一部分:通过实验探究气体X(已知由两种元素组成)的元素组成,实验装置如下,将0.17gX气体由注射器A缓缓送入B装置(B装置中的空气已预先除去),使之完全反应,生成的气体全部用D装置抽取收集。实验的现象和数据记录如下:

(1)参加反应的氧元素的质量是________ g,X中一定有______ 元素。
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25g/L,试推测该气体的化学式是_________ ,其质量是___________ g。(常见气体密度如下)
(3)写出B装置中发生反应的化学方程式_________ 。

| 现象 | 反应前质量(g) | 反应后质量(g) | |
| B装置中 | 逐渐变成亮红色 | 21.32 | 21.08 |
| C装置中 | 变蓝色 | 32.16 | 32.43 |
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25g/L,试推测该气体的化学式是
| 气 体 | H2 | O2 | CO | CH4 | N2 | CO2 |
| 常温常压时的密度(g/L) | 0.09 | 1.43 | 1.25 | 0.72 | 1.25 | 1.98 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】按要求写出下列含氯物质转化的方程式。
⑴某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。
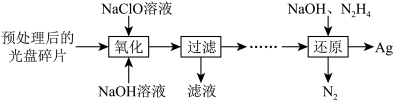
①NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的离子方程式为____ 。
②AgCl所发生“还原”反应的化学方程式为____ 。
⑵Cl2O可用作氯化剂,可由Cl2与潮湿的Na2CO3反应制得,反应的产物之一为NaHCO3。该反应的化学方程式为____ 。
⑶高氯酸钠是强氧化剂,可由电解NaClO3溶液制得。该反应的离子方程式为____ 。
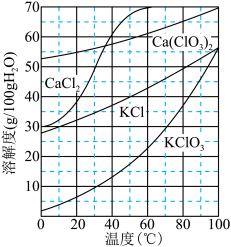
⑷如图所示为几种含氯化合物的溶解度随温度的变化曲线。常温下将其中某两种物质的饱和溶液混合,会发生反应。该反应的化学方程式为____ 。
⑴某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。

①NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的离子方程式为
②AgCl所发生“还原”反应的化学方程式为
⑵Cl2O可用作氯化剂,可由Cl2与潮湿的Na2CO3反应制得,反应的产物之一为NaHCO3。该反应的化学方程式为
⑶高氯酸钠是强氧化剂,可由电解NaClO3溶液制得。该反应的离子方程式为
⑷如图所示为几种含氯化合物的溶解度随温度的变化曲线。常温下将其中某两种物质的饱和溶液混合,会发生反应。该反应的化学方程式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
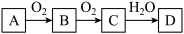
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是_______ 。
②在工业生产中B气体的大量排放被雨水吸收后形成_______ 而污染了环境。
③B气体能使酸性KMnO4溶液褪色,写出发生反应的离子方程式_______ ;
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是A_______ ;C_______ 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式:_______ 。该反应_______ (填“属于”或“不属于”)氧化还原反应。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②在工业生产中B气体的大量排放被雨水吸收后形成
③B气体能使酸性KMnO4溶液褪色,写出发生反应的离子方程式
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是A
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体( )。
)。
I.[查阅资料]
(1) 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成。
溶液混合无沉淀生成。
(2)向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。
(3) 易被氧化;
易被氧化; 难溶于水,可溶于稀HCl。
难溶于水,可溶于稀HCl。
II.[制备产品]
实验装置如图所示(省略夹持装置):
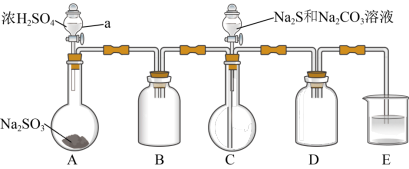
实验步骤:
(1)检查装置气密性,按图示加入试剂:装置A中发生反应的化学方程式为:_____ ;E中的试剂是______ (填字母)。
A.稀 B.
B. 溶液 C.饱和
溶液 C.饱和 溶液
溶液
(2)先向C中烧瓶加入 和
和 ,混合溶液,再向A中烧瓶滴加浓
,混合溶液,再向A中烧瓶滴加浓 。
。
(3)待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经_______ (填写操作名称)、过滤、洗涤、干燥,得到产品。
III.[探究与反思]
(1)为验证产品中含有 和
和 ,该小组设计了以下实验方案,请将方案补充完整,(所需试剂从稀
,该小组设计了以下实验方案,请将方案补充完整,(所需试剂从稀 、稀
、稀 、稀
、稀 、蒸馏水中选择)。
、蒸馏水中选择)。
取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,过滤,
溶液,有白色沉淀生成,过滤,____ ,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有 ,和
,和 。
。
(2)为减少装置C中生成 的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是
的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是_______ 。
 )。
)。I.[查阅资料]
(1)
 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成。
溶液混合无沉淀生成。(2)向
 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。(3)
 易被氧化;
易被氧化; 难溶于水,可溶于稀HCl。
难溶于水,可溶于稀HCl。II.[制备产品]
实验装置如图所示(省略夹持装置):

实验步骤:
(1)检查装置气密性,按图示加入试剂:装置A中发生反应的化学方程式为:
A.稀
 B.
B. 溶液 C.饱和
溶液 C.饱和 溶液
溶液(2)先向C中烧瓶加入
 和
和 ,混合溶液,再向A中烧瓶滴加浓
,混合溶液,再向A中烧瓶滴加浓 。
。(3)待
 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经III.[探究与反思]
(1)为验证产品中含有
 和
和 ,该小组设计了以下实验方案,请将方案补充完整,(所需试剂从稀
,该小组设计了以下实验方案,请将方案补充完整,(所需试剂从稀 、稀
、稀 、稀
、稀 、蒸馏水中选择)。
、蒸馏水中选择)。取适量产品配成稀溶液,滴加足量
 溶液,有白色沉淀生成,过滤,
溶液,有白色沉淀生成,过滤, ,和
,和 。
。(2)为减少装置C中生成
 的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是
的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
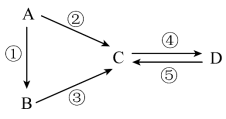
【推荐3】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:___________ 。
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:___________ 。
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式___________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出反应③的化学方程式:
(3)若C是一种强碱溶液,焰色试验火焰为黄色。写出反应②的离子方程式:
(4)若A是太阳能电池用的光伏材料,B是A的氧化物,写出用B制备A的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层。以高铝铬铁矿(主要含 和
和 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
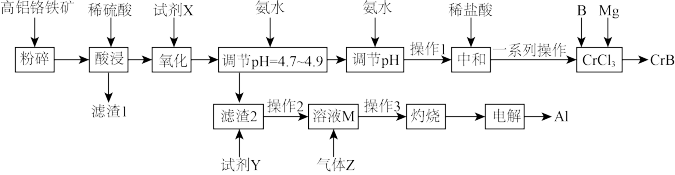
下表列出了相关金属离子生成氢氧化物沉淀的pH:
(1)滤渣1的主要成分是_______ 。
(2)已知试剂X是 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。
(3)试剂Y是_______ ,操作3的名称是_______ 。
(4)向M溶液中通入过量气体Z发生反应的离子方程式为_______ 。
(5)第二次加氨水调节pH的范围是_______ ;加稀盐酸中和前,需要洗涤沉淀,证明沉淀洗涤干净的操作方法是_______ 。
(6)硼化铬是在 时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:_______ 。
 和
和 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 2.3 | 10.4 | 4.9 | 7.5 | 3.4 |
| 沉淀完全的pH | 4.1 | 12.4 | 6.8 | 9.7 | 4.7 |
(1)滤渣1的主要成分是
(2)已知试剂X是
 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)试剂Y是
(4)向M溶液中通入过量气体Z发生反应的离子方程式为
(5)第二次加氨水调节pH的范围是
(6)硼化铬是在
 时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
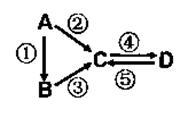
(1)若A是当前最常用的太阳能转换为电能的材料。C的水溶液俗称水玻璃,D为硅酸。则:
写出反应②的化学方程式________________ 。
(2)若A是应用最广泛的金属。反应①、⑤均用盐酸,D物质是红褐色。则:
写出反应③的化学方程式_________ 。B溶液中加入NaOH溶液的现象是___________ ,沉淀颜色发生变化对应的化学方程式是_________________________ 。
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2。则:反应②的离子方程式为_____________ 。反应④的离子方程式为____________________ 。

(1)若A是当前最常用的太阳能转换为电能的材料。C的水溶液俗称水玻璃,D为硅酸。则:
写出反应②的化学方程式
(2)若A是应用最广泛的金属。反应①、⑤均用盐酸,D物质是红褐色。则:
写出反应③的化学方程式
(3)若D物质是常见的两性氢氧化物,反应②③⑤均要用强碱溶液,反应④是通入过量的CO2。则:反应②的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:
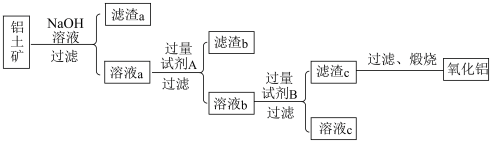
(1)滤渣a中除含泥沙外,一定含有____ ,分离溶液a和滤渣a的操作需要的玻璃仪器为__________________ 。
(2)溶液a中含铝元素的溶质与过量试剂A反应的离子方程式为_______________ ,溶液a与过量试剂A反应生成滤渣b的离子方程式为__________________ 。
(3)溶液b与过量试剂B反应生成滤渣c的离子方程式为_______________________ 。
(4)加热滤渣c得到氧化铝的操作需要使用的仪器除了酒精灯、三角架、泥三角,还有________ (填主要仪器名称),实验室里还常往NaAlO2溶液中通入过量的_______ 来制取A1(OH)3。

(1)滤渣a中除含泥沙外,一定含有
(2)溶液a中含铝元素的溶质与过量试剂A反应的离子方程式为
(3)溶液b与过量试剂B反应生成滤渣c的离子方程式为
(4)加热滤渣c得到氧化铝的操作需要使用的仪器除了酒精灯、三角架、泥三角,还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】化学在金属矿物和海水资源的开发利用过程中具有重要的意义和作用。按要求回答下列问题。
(1)在工业生产中金属冶炼的原理错误的是_
A 电解熔融的 NaCl 来制取 Na
B 电解熔融的 AlCl3来制取 Al
C CO 还原 Fe2O3制取 Fe
D 铝热反应原理制锰:4Al+3MnO2 3Mn+2 Al2O3
3Mn+2 Al2O3
(2)下图是从海水中提取溴的简单流程:

提取溴的过程中,经过 2 次 Br- Br2转化的目的是
Br2转化的目的是_____
(3)吸收塔中发生反应的离子方程式是_____
(4)海带中富含碘元素,实验室从海带中提取 I2的途径如下图所示:

①步骤 I 灼烧海带至灰烬时所用的主要仪器名称是_____ 。
②步骤 IV 向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_____ 。
③步骤 V 加入萃取剂 M 为_____ ,步骤 VI 从 I2的有机溶液获得 I2可以用 _____ 的方法。
(1)在工业生产中金属冶炼的原理错误的是
A 电解熔融的 NaCl 来制取 Na
B 电解熔融的 AlCl3来制取 Al
C CO 还原 Fe2O3制取 Fe
D 铝热反应原理制锰:4Al+3MnO2
 3Mn+2 Al2O3
3Mn+2 Al2O3(2)下图是从海水中提取溴的简单流程:

提取溴的过程中,经过 2 次 Br-
 Br2转化的目的是
Br2转化的目的是(3)吸收塔中发生反应的离子方程式是
(4)海带中富含碘元素,实验室从海带中提取 I2的途径如下图所示:

①步骤 I 灼烧海带至灰烬时所用的主要仪器名称是
②步骤 IV 向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③步骤 V 加入萃取剂 M 为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为TiO2,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
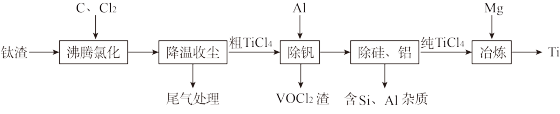
已知“降温收尘”后,粗TiCl4中含有的几种物质的沸点:
回答下列问题:
(1)TiO2与C. Cl2,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下,TiO2与C.Cl2反应的总化学方程式为_______ ;
②随着温度升高,尾气中CO的含量升高,原因是_______ 。
(2)“除钒”过程中的化学方程式为_______ ;
(3)“除硅、铝”过程中,分离TiCl4中含Si、Al杂质的方法是_______ 。
(4)“除钒”和“除硅、铝”的顺序不能交换,理由是_______ 。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。

已知“降温收尘”后,粗TiCl4中含有的几种物质的沸点:
| 物质 | TiCl4 | VOCl3 | SiCl4 | AlCl3 |
| 沸点/℃ | 136 | 127 | 57 | 180 |
(1)TiO2与C. Cl2,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
| 物质 | TiCl4 | CO | CO2 | Cl2 |
| 分压MPa | 4.59×10-2 | 1.84×10-2 | 3.70×10-2 | 5.98×10-9 |
②随着温度升高,尾气中CO的含量升高,原因是
(2)“除钒”过程中的化学方程式为
(3)“除硅、铝”过程中,分离TiCl4中含Si、Al杂质的方法是
(4)“除钒”和“除硅、铝”的顺序不能交换,理由是
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 | C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】按要求回答下列问题:
(1)以下物质中:①酒精,②熔化的KNO3,③CaCO3,④氢氧化钠溶液,⑤铜。其中属于电解质的是____ (填编号,下同),属于非电解质的是___ 。
(2)写出高炉炼铁是金属冶炼的常用方法的___ 法;用于制造光导纤维的物质的化学式___ 。
(3)FeS2(二硫化亚铁)不溶于水,可溶于适量的稀硝酸中,离子反应式如下:____FeS2+____H++____NO =____Fe2++____S↓+____NO↑+____H2O。回答下列问题:
=____Fe2++____S↓+____NO↑+____H2O。回答下列问题:
①配平此氧化还原反应方程式___ ,还原剂为___ 。
②若标准状况下生成2.24LNO,转移电子___ mol。
(1)以下物质中:①酒精,②熔化的KNO3,③CaCO3,④氢氧化钠溶液,⑤铜。其中属于电解质的是
(2)写出高炉炼铁是金属冶炼的常用方法的
(3)FeS2(二硫化亚铁)不溶于水,可溶于适量的稀硝酸中,离子反应式如下:____FeS2+____H++____NO
 =____Fe2++____S↓+____NO↑+____H2O。回答下列问题:
=____Fe2++____S↓+____NO↑+____H2O。回答下列问题:①配平此氧化还原反应方程式
②若标准状况下生成2.24LNO,转移电子
您最近一年使用:0次



