将 转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入
转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入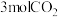 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
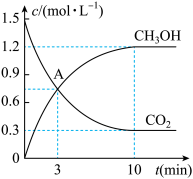
(1)在前 内,以
内,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是_______ 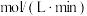 ;能加快此反应速率的措施有
;能加快此反应速率的措施有_______ (任一个措施)。
(2)a=_______ ;A点的正反应速率_______ (填“>”、“<”或“=”)逆反应速率。
(3)平衡时, 的浓度为
的浓度为_______  ;体系的压强与始反应的压强之比为
;体系的压强与始反应的压强之比为_______ 。
(4) 可以作燃料电池的燃料。
可以作燃料电池的燃料。 燃料电池是目前开发最成功的燃料电池之。
燃料电池是目前开发最成功的燃料电池之。 燃料电池由
燃料电池由 、空气(氧气)、
、空气(氧气)、 (电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
(电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
 转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入
转化成有机物可有效实现碳循环。在容积为2L的恒温恒容密闭容器中,充入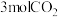 和
和 ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。
的物质的量随时间变化情况如表所示,并根据数据绘制图象如图。| 时间 | 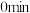 |  |  |  | 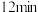 |
 | 3 | 1.5 | 09 | a | 0.6 |
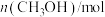 | 0 | 1.5 | 2.1 | 2.4 | 2.4 |

(1)在前
 内,以
内,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是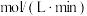 ;能加快此反应速率的措施有
;能加快此反应速率的措施有(2)a=
(3)平衡时,
 的浓度为
的浓度为 ;体系的压强与始反应的压强之比为
;体系的压强与始反应的压强之比为(4)
 可以作燃料电池的燃料。
可以作燃料电池的燃料。 燃料电池是目前开发最成功的燃料电池之。
燃料电池是目前开发最成功的燃料电池之。 燃料电池由
燃料电池由 、空气(氧气)、
、空气(氧气)、 (电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
(电解质溶液)构成。下列说法正确的是_______(填字母代号)。已知:该燃料电池的总反应为
| A.电池放电时,通入空气的电极为正极 |
B.电池放电时,每消耗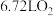 时转移 时转移 电子 电子 |
| C.电池放电时,电解质溶液的碱性逐渐减弱 |
D.负极的电极反应式为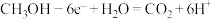 |
更新时间:2022-07-12 19:18:13
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】将CO2转化成有机物可有效实现确循环。在容积为2L的恒温恒容密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应CO2(g)+ 3H2(g) CH3OH(g) +H2O(g),测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
CH3OH(g) +H2O(g),测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
(1)a=___________ ;3~9 min内,v(CO2)=___________ mol·L-1·min-1
(2)能说明上述反应达到平衡状态的是___________ (填标号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成1 mol H2,同时生成1mol CH3OH
D.混合气体的平均相对分子质量不随时间的变化而变化
(3)上述反应6 min末时,已消耗掉的CO2的物质的量分数为___________
(4)上述反应12 min末时,混合气体中CO2(g)和H2(g)的质量之比是___________
(5)第3 min时v正(CH3OH)___________ (填“>”、“<”、“=”或“无法比较”)第9 min时v逆(CH3OH)
(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2 L的恒容密闭容器中,发生反应mX(g) nY(g),X和Y的物质的量浓度随时间的变化情况如下表。
nY(g),X和Y的物质的量浓度随时间的变化情况如下表。
①m:n=___________ 。
②c=___________ (保留两位有效数字)
 CH3OH(g) +H2O(g),测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
CH3OH(g) +H2O(g),测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH)/mol | 0 | 0.50 | 0.65 | 0.74 | 0.74 |
| n(CO2)/mol | 1 | 0.50 | 0.35 | a | 0.26 |
(1)a=
(2)能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成1 mol H2,同时生成1mol CH3OH
D.混合气体的平均相对分子质量不随时间的变化而变化
(3)上述反应6 min末时,已消耗掉的CO2的物质的量分数为
(4)上述反应12 min末时,混合气体中CO2(g)和H2(g)的质量之比是
(5)第3 min时v正(CH3OH)
(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2 L的恒容密闭容器中,发生反应mX(g)
 nY(g),X和Y的物质的量浓度随时间的变化情况如下表。
nY(g),X和Y的物质的量浓度随时间的变化情况如下表。| 时间/min | 0 | 5 | 10 | 15 | 20 |
| c(X )/mol·L-1 | 0.2 | c | 0.6 | 0.6 | 0.6 |
| c(Y)/mol·L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 |
①m:n=
②c=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在密闭容器内充入0.1mol·L-1N2和0.3mol·L-1H2。反应5min后达平衡,NH3的物质的量浓度为0.10mol•L-1。试回答问题:
(1)恒容条件下,从开始反应到建立起平衡状态,v(N2)=____ ;反应达到平衡后,第5分钟末只改变反应温度,保持其它条件不变,则改变条件后NH3的物质的量浓度不可能为__ 。
A.0.20mol·L-1 B.0.12mol·L-1 C.0.10mol·L-1 D.0.08mol·L-1
(2)其它条件不变,若只把容器改为恒压容器,加入0.2molN2和0.6molH2,达到平衡时,NH3的体积分数为m%。若向容器中继续加入0.2molN2和0.6molH2,在同样的温度下达到平衡时,NH3的体积分数为n%,则m和n的关系正确的是___ 。
A.m>n B.m<n C.m=n D.无法比较
(1)恒容条件下,从开始反应到建立起平衡状态,v(N2)=
A.0.20mol·L-1 B.0.12mol·L-1 C.0.10mol·L-1 D.0.08mol·L-1
(2)其它条件不变,若只把容器改为恒压容器,加入0.2molN2和0.6molH2,达到平衡时,NH3的体积分数为m%。若向容器中继续加入0.2molN2和0.6molH2,在同样的温度下达到平衡时,NH3的体积分数为n%,则m和n的关系正确的是
A.m>n B.m<n C.m=n D.无法比较
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】某温度下,容积同为2L的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知某温度下2HI(g) H2 (g)+I2 (g)
H2 (g)+I2 (g)  =+A kJ·mol-1 K=4.0)
=+A kJ·mol-1 K=4.0)
(1)根据上表回答问题
①c1、c3的关系式为_______
②a、b的关系式为__________
③p2、p3的关系式为__________
④a1与a2的关系式为__________
(2)甲容器中:该反应的平衡常数表达式为__________ ;
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为___ mol•L-1•min-1;
(4)丙容器中:反应开始时进行的方向是_____ (填“向左”、“向右”或“不动”)
(5)乙容器中:当反应达到平衡状态后,向容器中再充入1 mol H2,则1分钟后,正反应速率与原平衡时相比___________ 填“增大”、“不变”或“减小”)
(已知某温度下2HI(g)
 H2 (g)+I2 (g)
H2 (g)+I2 (g)  =+A kJ·mol-1 K=4.0)
=+A kJ·mol-1 K=4.0)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol HI | 1 mol H2 + 1 1mol I2 | 2 mol HI + 1 mol H2 + 1 mol I2 |
HI的浓度(mol·L ) ) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 |  |  |  |
(1)根据上表回答问题
①c1、c3的关系式为
②a、b的关系式为
③p2、p3的关系式为
④a1与a2的关系式为
(2)甲容器中:该反应的平衡常数表达式为
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为
(4)丙容器中:反应开始时进行的方向是
(5)乙容器中:当反应达到平衡状态后,向容器中再充入1 mol H2,则1分钟后,正反应速率与原平衡时相比
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组研究化学反应中的能量变化,进行了如下实验。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为_______ 。
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。
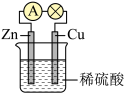
锌片上电极反应式为___________ ;铜片上能够观察到的现象是___________ ;电子流向 ___________ 填“锌片−导线−铜片”或“铜片−导线−锌片”)
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是___________ 。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。

锌片上电极反应式为
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.为了探究化学反应的热效应,某兴趣小组进行了如下实验:

(1)如图a所示,室温下,观察到甲处液面上升,乙处液面下降,则该反应是___________ (填“放热”或“吸热”)反应,写出该反应的化学方程式:___________ 。
(2)如图b所示,室温下,把装有固体A的试管放入盛有饱和澄清石灰水的烧杯中,向该试管中滴入一定量的液体B,观察到烧杯中的饱和澄清石灰水变浑浊,则该反应是___________ (填“放热”或“吸热”)反应,写出一个符合该条件的化学方程式:___________ 。
(3)如图c所示,室温下,通过仪器丙向仪器丁中的一定浓度的盐酸中加入一定浓度的氢氧化钠溶液,仪器丙的名称为___________ 。
Ⅱ.
(4)在一定温度下,容积为1 L的恒容密闭容器中某一反应中所涉及的物质仅有M、N,其物质的量随反应时间变化的曲线如图所示。下列表述中错误的是___________ 。
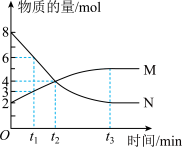
A.该反应的化学方程式为2N(g)⇌M(g)
B.0~t2,该反应的平均反应速率v(N)=4 mol•L-1•min-1
C.t3时,反应达到平衡
D.t1时,N的浓度是M的2倍
E.t3时,反应停止
Ⅲ.
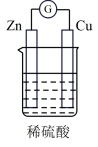
(5)铜锌原电池是人类最早研究的化学电源之一,其简易装置如图所示,可观察到的现象是锌片溶解,铜片表面产生气泡,电流计指针偏向铜电极,根据上述原理,以下各种原电池的分析正确的是___________ 。

(1)如图a所示,室温下,观察到甲处液面上升,乙处液面下降,则该反应是
(2)如图b所示,室温下,把装有固体A的试管放入盛有饱和澄清石灰水的烧杯中,向该试管中滴入一定量的液体B,观察到烧杯中的饱和澄清石灰水变浑浊,则该反应是
(3)如图c所示,室温下,通过仪器丙向仪器丁中的一定浓度的盐酸中加入一定浓度的氢氧化钠溶液,仪器丙的名称为
Ⅱ.
(4)在一定温度下,容积为1 L的恒容密闭容器中某一反应中所涉及的物质仅有M、N,其物质的量随反应时间变化的曲线如图所示。下列表述中错误的是

A.该反应的化学方程式为2N(g)⇌M(g)
B.0~t2,该反应的平均反应速率v(N)=4 mol•L-1•min-1
C.t3时,反应达到平衡
D.t1时,N的浓度是M的2倍
E.t3时,反应停止
Ⅲ.
(5)铜锌原电池是人类最早研究的化学电源之一,其简易装置如图所示,可观察到的现象是锌片溶解,铜片表面产生气泡,电流计指针偏向铜电极,根据上述原理,以下各种原电池的分析正确的是

| 选项 | A | B | C | D |
| 装置 | 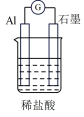 |  | 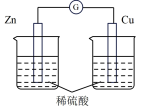 | 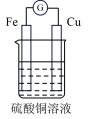 |
| 分析 | Al电极为负极,H+在该极发生还原反应 | 电流计指针偏向Al,溶液中的OH-移向Mg电极 | 电流由Cu电极流向Zn电极,Cu片表面产生气泡 | 电子由Fe电极流向Cu电极,Fe发生氧化反应 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】按要求回答问题:
(1)由SiO2制备高纯度硅的工业流程如图所示:
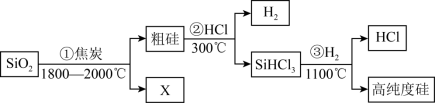
①写出SiO2转化为Si(粗)的化学方程式:____________________________________________ 。
②可以循环使用的物质为_________________________ 。
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
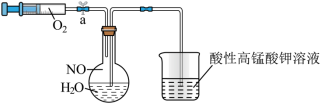
①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是____________ ,产生此现象的化学方程式为______________________________________________ 。
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式________________________________ 。
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向________ 极移动(填“正”或“负”)。
②若有 1 mol e- 流过导线,则理论上负极质量减少________ g。
③若将稀硫酸换成浓硝酸,正极电极方程式为:______________________ 。
(1)由SiO2制备高纯度硅的工业流程如图所示:

①写出SiO2转化为Si(粗)的化学方程式:
②可以循环使用的物质为
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。

①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向
②若有 1 mol e- 流过导线,则理论上负极质量减少
③若将稀硫酸换成浓硝酸,正极电极方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】磷酸亚铁锂( )稳定性好,磷酸亚铁锂电池是新能源汽车的动力电池之一,可利用钛铁矿(主要成分为
)稳定性好,磷酸亚铁锂电池是新能源汽车的动力电池之一,可利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 、
、 等杂质)来制备,工艺流程如图所示:
等杂质)来制备,工艺流程如图所示:

(1)为提高钛铁矿的溶浸效率,除了采取循环浸取延长时间外,还可以采取的措施有___________ (任写一点)。
(2)从滤液a中获得 的基本操作是
的基本操作是___________ 、___________ 、过滤、洗涤、干燥等。
(3)滤液a中钛元素主要以 形式存在,写出其水解生成钛酸沉淀的化学方程式:
形式存在,写出其水解生成钛酸沉淀的化学方程式:___________ 。
(4)离子电池工业对纳米磷酸亚铁纯度要求较高,而工业制得的磷酸亚铁晶体中含有一定量的Ti、Al等金属杂质,因此必须先对粗产品进行除杂处理。25℃条件下,某同学用磷酸亚铁样品配制了500mL溶液,所得溶液中 ,
, ,加入氢氧化钠,调整pH到2.0(假设溶液体积不变),使
,加入氢氧化钠,调整pH到2.0(假设溶液体积不变),使 恰好沉淀完全。{已知:25℃,
恰好沉淀完全。{已知:25℃, ,一般认为溶液中某离子浓度
,一般认为溶液中某离子浓度 时沉淀完全}
时沉淀完全}
①此时___________ (填“有”或“无”) 沉淀生成,理由是
沉淀生成,理由是___________ 。
②若要将 完全除去,需将pH值调整到
完全除去,需将pH值调整到___________ (保留两位有效数字)。
(5)将磷酸铁、氢氧化锂和聚丙烯按比例混合好后,置于 气氛管式炉中800℃煅烧10h,可制得
气氛管式炉中800℃煅烧10h,可制得 晶体,据此推测,聚丙烯的作用可能是
晶体,据此推测,聚丙烯的作用可能是___________ 。
(6)钛铁矿还可制备钛酸锂( ),现用钛酸锂(
),现用钛酸锂( )与磷酸亚铁锂(
)与磷酸亚铁锂( )做电极组成电池,其工作原理为
)做电极组成电池,其工作原理为 ,该电池放电时正极反应式为
,该电池放电时正极反应式为___________ 。
 )稳定性好,磷酸亚铁锂电池是新能源汽车的动力电池之一,可利用钛铁矿(主要成分为
)稳定性好,磷酸亚铁锂电池是新能源汽车的动力电池之一,可利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 、
、 等杂质)来制备,工艺流程如图所示:
等杂质)来制备,工艺流程如图所示:
(1)为提高钛铁矿的溶浸效率,除了采取循环浸取延长时间外,还可以采取的措施有
(2)从滤液a中获得
 的基本操作是
的基本操作是(3)滤液a中钛元素主要以
 形式存在,写出其水解生成钛酸沉淀的化学方程式:
形式存在,写出其水解生成钛酸沉淀的化学方程式:(4)离子电池工业对纳米磷酸亚铁纯度要求较高,而工业制得的磷酸亚铁晶体中含有一定量的Ti、Al等金属杂质,因此必须先对粗产品进行除杂处理。25℃条件下,某同学用磷酸亚铁样品配制了500mL溶液,所得溶液中
 ,
, ,加入氢氧化钠,调整pH到2.0(假设溶液体积不变),使
,加入氢氧化钠,调整pH到2.0(假设溶液体积不变),使 恰好沉淀完全。{已知:25℃,
恰好沉淀完全。{已知:25℃, ,一般认为溶液中某离子浓度
,一般认为溶液中某离子浓度 时沉淀完全}
时沉淀完全}①此时
 沉淀生成,理由是
沉淀生成,理由是②若要将
 完全除去,需将pH值调整到
完全除去,需将pH值调整到(5)将磷酸铁、氢氧化锂和聚丙烯按比例混合好后,置于
 气氛管式炉中800℃煅烧10h,可制得
气氛管式炉中800℃煅烧10h,可制得 晶体,据此推测,聚丙烯的作用可能是
晶体,据此推测,聚丙烯的作用可能是(6)钛铁矿还可制备钛酸锂(
 ),现用钛酸锂(
),现用钛酸锂( )与磷酸亚铁锂(
)与磷酸亚铁锂( )做电极组成电池,其工作原理为
)做电极组成电池,其工作原理为 ,该电池放电时正极反应式为
,该电池放电时正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】I.请根据化学能和热能、电能相关的知识,问答下列问题:
(1)下列变化中,属于放热反应的是______ (填序号)。
①液态水汽化
②Ba(OH)2•8H2O与固体NH4Cl混合
③浓H2SO4稀释
④C+H2O(g) CO+H2
CO+H2
⑤生石灰跟水反应
⑥碳酸钠粉末滴少量水
(2)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:______ 。
(3)已知:
CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1
2H2(g)+O2(g)=2H2O(1)△H2=-571.6kJ•mol-1
H2O(g)=H2(g)+ O2(g) ΔH3=+241.8kJ•mol-1
O2(g) ΔH3=+241.8kJ•mol-1
根据上述反应CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=______ kJ•mol-1。
(4)某实验小组设计用50mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行中和反应,测得的中和热为△H1。若用等浓度的醋酸代替盐酸,测得的中和热为△H2;若用浓硫酸代替盐酸,测得的中和热为△H3,下列说法正确的是______ 。
(5)某化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。______ (填“能”或“不能”)确定三种物质A2(g)、B2(g)、AB(g)中,最稳定的是AB(g)。
②根据图可知A2(g)和B2(g)生成1molAB(g)的焓变△H为______ kJ•mol-1。
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:______ (填离子或分子的化学式)。丙装置中负极反应式为______ 。
(7)当甲装置导线中转移0.3mol电子时,正极生成气体______ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3mol电子时,两电极质量相差______ g。
(8)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则d电极上的电极反应式为______ 。
(1)下列变化中,属于放热反应的是
①液态水汽化
②Ba(OH)2•8H2O与固体NH4Cl混合
③浓H2SO4稀释
④C+H2O(g)
 CO+H2
CO+H2⑤生石灰跟水反应
⑥碳酸钠粉末滴少量水
(2)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)已知:
CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1
2H2(g)+O2(g)=2H2O(1)△H2=-571.6kJ•mol-1
H2O(g)=H2(g)+
 O2(g) ΔH3=+241.8kJ•mol-1
O2(g) ΔH3=+241.8kJ•mol-1根据上述反应CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=
(4)某实验小组设计用50mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行中和反应,测得的中和热为△H1。若用等浓度的醋酸代替盐酸,测得的中和热为△H2;若用浓硫酸代替盐酸,测得的中和热为△H3,下列说法正确的是
| A.△H1>△H2>△H3 | B.△H3>△H1>△H2 |
| C.△H2>△H1>△H3 | D.△H1=△H2>△H3 |
(5)某化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。

②根据图可知A2(g)和B2(g)生成1molAB(g)的焓变△H为
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(7)当甲装置导线中转移0.3mol电子时,正极生成气体
(8)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则d电极上的电极反应式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)石墨电极(C)作___________ 极,甲中甲烷燃料电池的负极反应式为___________ 。
(2)若消耗2.24 L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为___________ L。
(3)丙中以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是___________(填字母)。
(4)若丙中以稀H2SO4为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为___________ 。
(5)以铅蓄电池为电源,Pb+PbO2+2H2SO4 2PbSO4+2H2O,铅蓄电池放电时,负极反应式为
2PbSO4+2H2O,铅蓄电池放电时,负极反应式为___________ 。

(1)石墨电极(C)作
(2)若消耗2.24 L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(3)丙中以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、An等杂质)的电解精炼。下列说法正确的是___________(填字母)。
| A.a电极为纯铜 | B.粗铜接电源正极,发生还原反应 |
| C.CuSO4溶液的浓度保持不变 | D.利用阳极泥可回收Ag、Pt、Au等金属 |
(4)若丙中以稀H2SO4为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
(5)以铅蓄电池为电源,Pb+PbO2+2H2SO4
 2PbSO4+2H2O,铅蓄电池放电时,负极反应式为
2PbSO4+2H2O,铅蓄电池放电时,负极反应式为
您最近一年使用:0次



