超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸HSbF6的制备及性质进行了探究。由三氯化锑(SbCl3)制备HSbF6的反应如下: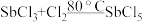 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
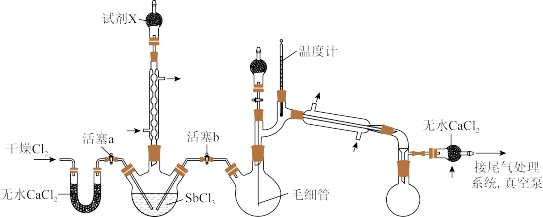
相关性质如表:
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为_______ (写化学反应方程式)。
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为_______ 。
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(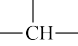 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式_______ 。
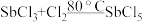 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
| 物质 | 熔点 | 沸点 | 性质 |
| SbCl3 | 73.4℃ | 220.3℃ | 极易水解 |
| SbCl5 | 3.5℃ | 140℃分解79℃/2.9kPa | 极易水解 |
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(
 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式
2022高三·全国·专题练习 查看更多[1]
(已下线)微专题28 有关工艺流程和实验探究方程式的书写-备战2023年高考化学一轮复习考点微专题
更新时间:2022-08-12 16:46:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(CN)2、(OCN)2、(SCN)2等与X2(X=F、Cl、Br、I)的性质相似,CN—、OCN—、SCN—与X—的性质相似,被称为拟卤素。完成下列反应方程式(一律要配平):
(CN)2+H2O=_____________________ ;
AgSCN+Br2=________________ ;
AgCN=_____________________ ;
BrCl+ H2O=___________________ 。
(CN)2+H2O=
AgSCN+Br2=
AgCN=
BrCl+ H2O=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列是四种状态下NaCl的图示(M、N均为惰性电极),完成下列各题。
(1)①中存在Na+和Cl-,但①不能导电,请说明理由_____ 。
(2)结合图示信息和所学知识,判断下列说法正确的是_____ 。
(3)写出③状态下发生反应的化学方程式_____ 。可用于检验N极产生气体的试剂是_____ 。
A.稀盐酸 B.氢氧化钠溶液 C.淀粉碘化钾溶液 D.硝酸银溶液
(4)由④可知M与电源的_____ (填“正极”或“负极”)相连。由③④可知电解质导电的条件是_____ 。
(5)若用“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子。如图四种变化中,能体现水“参与”“化学变化”的微观本质是
”表示氧原子。如图四种变化中,能体现水“参与”“化学变化”的微观本质是_____ 。
| ① | ② | ③ | ④ |
 |  | 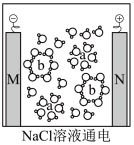 |  |
(2)结合图示信息和所学知识,判断下列说法正确的是
| A.由②③可知,a为Cl-,b为Na+ |
| B.在③中,只存在Na+和Cl-两种微粒 |
| C.①中的氯化钠晶体变为②中的a和b的过程,称为电解 |
| D.NaCl溶于水时,在H2O分子作用下,Na+和Cl-脱离固体表面进入水中,与H2O结合成自由移动的水合Na+和水合Cl- |
A.稀盐酸 B.氢氧化钠溶液 C.淀粉碘化钾溶液 D.硝酸银溶液
(4)由④可知M与电源的
(5)若用“
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子。如图四种变化中,能体现水“参与”“化学变化”的微观本质是
”表示氧原子。如图四种变化中,能体现水“参与”“化学变化”的微观本质是A.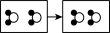 | B.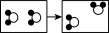 | C. | D.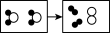 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】用NA表示阿伏加德罗常数,判断下列说法是否正确。
1.5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA。(_______)
2.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,转移的电子数目为0.2NA。(_______)
3.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA。(_______)
4.1 mol Na2O2与足量CO2充分反应转移的电子数为2NA。(_______)
5.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移电子的数目不小于3NA。(_______)
6.1 mol Cl2参加反应转移电子数一定为2NA。(_______)
7.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数小于2NA。(_______)
8.0.3 mol NO2与足量的水反应转移电子数目为0.2NA。(_______)
1.5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA。(_______)
2.0.1 mol Zn与含0.1 mol HCl的盐酸充分反应,转移的电子数目为0.2NA。(_______)
3.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA。(_______)
4.1 mol Na2O2与足量CO2充分反应转移的电子数为2NA。(_______)
5.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移电子的数目不小于3NA。(_______)
6.1 mol Cl2参加反应转移电子数一定为2NA。(_______)
7.常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数小于2NA。(_______)
8.0.3 mol NO2与足量的水反应转移电子数目为0.2NA。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。请写下列空白:
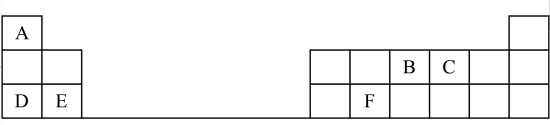
(1)A与B形成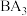 的化学式为
的化学式为___________ ;C的原子结构示意图为___________ 。
(2)B的最高价氧化物对应的水化物的化学式为___________ ;D、E的最高价氧化物对应的水化物中碱性较弱的是___________ (用化学式表示),元素C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)。
(3)E位于周期表的第三周期第___________ 族;F的氧化物与氢氧化钠溶液反应的离子方程式为___________ 。

(1)A与B形成
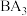 的化学式为
的化学式为(2)B的最高价氧化物对应的水化物的化学式为
(3)E位于周期表的第三周期第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.按要求填空:(用化学方程式表示)
(1)工业合成氨___________
(2)氨的催化氧化反应___________
(3)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为:___________
(4)氢氟酸不能使用玻璃瓶盛装的原因:___________
II.请自选试剂完成不同价态含硫物质的转化方程式(化学或离子均可)
(5)S(-2)→S(0)___________
(6)S(+6)→S(+4)___________
(1)工业合成氨
(2)氨的催化氧化反应
(3)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为:
(4)氢氟酸不能使用玻璃瓶盛装的原因:
II.请自选试剂完成不同价态含硫物质的转化方程式(化学或离子均可)
(5)S(-2)→S(0)
(6)S(+6)→S(+4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅是带来人类文明的重要元素之一,工业上可用石英砂制备硅单质。
(1)硅和锗(Ge)属于同主族元素。下列推测不合理的是___________ (填字母)。
a.Ge与Si的最外层电子数均为4 b.常温下 是气体
是气体
c.酸性: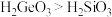 d.Si和Ge都可做半导体材料
d.Si和Ge都可做半导体材料
(2)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是___________ 。
②在以上流程中,能否将盐酸改为NaOH溶液,请说明理由:___________ 。
(3)氮化硅( )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为 。
。
①该反应中的氧化剂为___________ (填化学式)。
②若生成标准状况下16.8L CO,则生成氮化硅的质量是___________ (保留1位小数)。
(4)我国成功发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石(主要成分为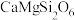 )、斜长石(主要成分为
)、斜长石(主要成分为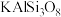 )和橄榄石(主要成分为
)和橄榄石(主要成分为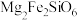 )等,橄榄石的主要成分中铁元素为
)等,橄榄石的主要成分中铁元素为___________ 价,橄榄石的主要成分的氧化物形式可表示为___________ 。辉石、斜长石及橄榄石的主要成分均属于___________ (填“氧化物”“混合物”或“硅酸盐”)。
(1)硅和锗(Ge)属于同主族元素。下列推测不合理的是
a.Ge与Si的最外层电子数均为4 b.常温下
 是气体
是气体c.酸性:
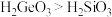 d.Si和Ge都可做半导体材料
d.Si和Ge都可做半导体材料(2)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是
②在以上流程中,能否将盐酸改为NaOH溶液,请说明理由:
(3)氮化硅(
 )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气中制得。反应的化学方程式为 。
。①该反应中的氧化剂为
②若生成标准状况下16.8L CO,则生成氮化硅的质量是
(4)我国成功发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石(主要成分为
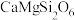 )、斜长石(主要成分为
)、斜长石(主要成分为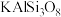 )和橄榄石(主要成分为
)和橄榄石(主要成分为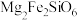 )等,橄榄石的主要成分中铁元素为
)等,橄榄石的主要成分中铁元素为
您最近一年使用:0次
【推荐1】一种用草酸泥渣(含PbC2O4和PbSO4)制备PbCrO4的工艺流程如图:
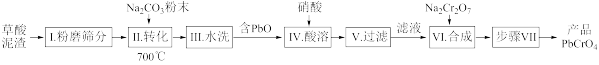
已知:①PbC2O4完全分解的化学方程式为PbC2O4 PbO+CO↑+CO2↑。②PbCrO4难溶于水。回答下列问题:
PbO+CO↑+CO2↑。②PbCrO4难溶于水。回答下列问题:
(1)泥渣“粉磨筛分”的目的是_______ ;实验室过滤操作需要的玻璃仪器有漏斗、烧杯和_____ 。
(2)用Na2CO3将难以热分解的硫酸铅转化为易分解的的碳酸铅。若在水溶液中进行,PbSO4(s)+ (aq)=PbCO3(s)+
(aq)=PbCO3(s)+ (aq),该反应的平衡常数K
(aq),该反应的平衡常数K______ 。[已知Ksp(PbCO3) =6.4×10-4,Ksp(PbSO4)=1.6×10-8]。
(3)铬酸钠在硫酸溶液中可转化为重铬酸钠,该反应的离子方程式为______ ,步骤V“合成”时发生反应的化学方程式为_________ 。
(4)铬酸铅是一种用于水彩和油彩的黄色颜料,遇到空气中的硫化氢颜色会变黑,该过程的化学方程式为________ 。

已知:①PbC2O4完全分解的化学方程式为PbC2O4
 PbO+CO↑+CO2↑。②PbCrO4难溶于水。回答下列问题:
PbO+CO↑+CO2↑。②PbCrO4难溶于水。回答下列问题:(1)泥渣“粉磨筛分”的目的是
(2)用Na2CO3将难以热分解的硫酸铅转化为易分解的的碳酸铅。若在水溶液中进行,PbSO4(s)+
 (aq)=PbCO3(s)+
(aq)=PbCO3(s)+ (aq),该反应的平衡常数K
(aq),该反应的平衡常数K(3)铬酸钠在硫酸溶液中可转化为重铬酸钠,该反应的离子方程式为
(4)铬酸铅是一种用于水彩和油彩的黄色颜料,遇到空气中的硫化氢颜色会变黑,该过程的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现用氯化铜晶体(CuCl2·2H2O,含氯化亚铁杂质)制取纯净的CuCl2·2H2O。先将其制成水溶液,后按如图步骤进行提纯:
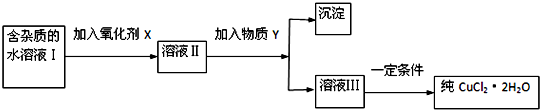
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表
请回答下列问题:
(1)现有氧化剂NaClO、H2O2、KMnO4,X加哪种好,为什么?________________________________ ,该反应的离子方程式为_________________________________ 。
(2)溶液II中除Cu2+外,还有______ 金属离子,检验试剂为______________ 。物质Y 不能为下列的________________________ 。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3 e.CaO f.NaOH
(3)常温下,除去CuCl2 溶液中的Fe2+,加入氧化剂X,使Fe2+氧化为Fe3+,然后加入物质Y 至溶液pH=4,此时c(Fe3+)=_________ mol/L,[已知Fe(OH)3 的Ksp=4×10-38]
(4)若在空气中加热固体CuCl2·2H2O,可水解生成Cu(OH)Cl,写出相关的化学方程式_______________________________________ 。

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表
金属离子 | Fe3+ | Fe2+ | Cu2+ |
氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)现有氧化剂NaClO、H2O2、KMnO4,X加哪种好,为什么?
(2)溶液II中除Cu2+外,还有
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3 e.CaO f.NaOH
(3)常温下,除去CuCl2 溶液中的Fe2+,加入氧化剂X,使Fe2+氧化为Fe3+,然后加入物质Y 至溶液pH=4,此时c(Fe3+)=
(4)若在空气中加热固体CuCl2·2H2O,可水解生成Cu(OH)Cl,写出相关的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业催化剂 K3[Fe(C2O4)3]·3H2O是翠绿色晶体,在421~553℃时,分解为Fe2O3、K2CO3、CO、CO2、H2O。实验室由草酸亚铁晶体(FeC2O4·H2O)、草酸钾(K2C2O4)、草酸(H2C2O4)和双氧水(H2O2)混合制备。请回答下列问题
(1)写出H2O2的电子式:___ 。
(2)配平该方程式:__ FeC2O4·2H2O+__ H2O2+__ K2C2O4+__ H2C2O4=__ K3[Fe(C2O4)3]·3H2O
(3)制备过程中要防止草酸被H2O2氧化,请写出草酸被H2O2氧化的化学反应方程式___ ;
(4)配合物的稳定性可以用稳定常数K来衡量,如Cu2++4NH3=[Cu(NH3)4]2+,其稳定常数表达式为:K=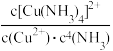 。已知K[Fe(C2O4)3]3—=1020,K[Fe(SCN)3]=2
。已知K[Fe(C2O4)3]3—=1020,K[Fe(SCN)3]=2 103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素?
103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素?___ (填“是”或“否”)若选“否”,请设计检验铁元素的方案___ 。
(1)写出H2O2的电子式:
(2)配平该方程式:
(3)制备过程中要防止草酸被H2O2氧化,请写出草酸被H2O2氧化的化学反应方程式
(4)配合物的稳定性可以用稳定常数K来衡量,如Cu2++4NH3=[Cu(NH3)4]2+,其稳定常数表达式为:K=
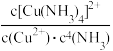 。已知K[Fe(C2O4)3]3—=1020,K[Fe(SCN)3]=2
。已知K[Fe(C2O4)3]3—=1020,K[Fe(SCN)3]=2 103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素?
103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素?
您最近一年使用:0次



