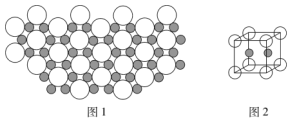
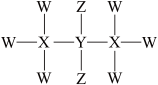前20号主族元素W、X、Y、Z、R的原子序数依次增大。W基态原子成对电子数比未成对电子数多2个,Y最外层电子数是其内层电子数的3倍,Z基态原子的3s轨道上有1个电子,Y和R位于同一主族。下列说法错误的是
A.原子半径: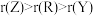 |
B.简单氢化物的稳定性: |
| C.Y的基态原子核外有8种空间运动状态不同的电子 |
| D.W形成的化合物种类繁多,可通过质谱法测定分子中的化学键 |
更新时间:2022-04-06 22:48:18
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】某有机物蒸气14.8g,充分燃烧后得到 和
和 。该有机物的质谱图如图所示,该有机物可与金属钠反应放出氢气,该有机物可能是
。该有机物的质谱图如图所示,该有机物可与金属钠反应放出氢气,该有机物可能是

 和
和 。该有机物的质谱图如图所示,该有机物可与金属钠反应放出氢气,该有机物可能是
。该有机物的质谱图如图所示,该有机物可与金属钠反应放出氢气,该有机物可能是
A.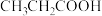 | B. |
C.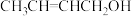 | D. |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列对有关事实的解释正确的是
| 选项 | 事实 | 解释 |
| A | SiO2的熔点比干冰高 | SiO2晶体是共价晶体,分子间作用力大 |
| B | 在CS2中的溶解度:CCl4 >H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 离子液体有难挥发性 | 离子液体的粒子全都是带电荷的离子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】W、X、Y、Z是原子序数依次增大的四种短周期主族元素,W原子最外层电子数为次外层的3倍,Z原子最外层电子数为W原子最外层电子数的一半,Y和W可形成一种淡黄色固体化合物。下列说法错误的是
A.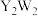 可做潜艇供氧剂 可做潜艇供氧剂 |
B.对应简单离子半径: |
C.最简单气态氢化物的稳定性: |
| D.Y、Z最高价氧化物对应的水化物可以相互反应生成盐和水 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】T、W、X、Y、Z是原子序数依次增大的前四周期元素。基态原子中,T的各能级电子数相等;X的价层电子排布式为nsnnp2n;Y的核外电子填充在8个轨道中;Z有4个未成对电子。下列说法不正确的是
| A.电负性大小:X>W>Y |
| B.最简单氢化物的沸点:W>T>Y |
| C.最高价氧化物对应水化物的酸性:W>T>Y |
| D.Y与W、Z与X均能形成原子个数比为4:3的化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列反应或事实不能用元素周期律解释的是
| A.非金属性:向无色的Na2S溶液中通入Cl2,出现黄色沉淀 |
| B.金属性:Na+KCl(熔融)=K↑+NaCl |
| C.还原性:H2S>HCl |
| D.酸性:H2SiO3<H2SO3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,实验室中常用 洗涤残留在试管壁上的N单质。下列说法错误的是
洗涤残留在试管壁上的N单质。下列说法错误的是
 洗涤残留在试管壁上的N单质。下列说法错误的是
洗涤残留在试管壁上的N单质。下列说法错误的是
A.实验室中用 洗涤残留在试管壁上的N单质,利用了N单质的物理性质 洗涤残留在试管壁上的N单质,利用了N单质的物理性质 |
| B.M、Z形成的化合物中只含有离子键,是离子化合物 |
| C.化合物W常用作氧化剂,在高温下使用氧化性增强 |
| D.化合物W全部溶于水,并加入足量盐酸可以得到两种无色无味的气体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成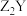 、
、 型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
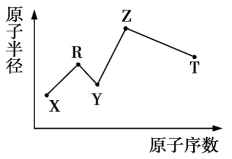
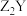 、
、 型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
A.原子半径和离子半径: |
B.最简单氢化物的沸点: |
C.最高价氧化物对应水化物的酸性: |
| D.由X、Y、Z、R四种元素组成的常见化合物中含有离子键 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列叙述中正确的是
| A.焰色试验属于化学变化 |
| B.金属的电化学腐蚀比化学腐蚀更普遍 |
| C.阴极电保护法保护钢构件,钢构件与直流电源负极相连 |
| D.钠原子核外电子排布由1s22s22p63s1→1s22s22p63p1时,原子释放能量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X元素原子的价电子排布式为3s23p1,Y元素位于元素周期表中第三周期,其原子最外层p轨道为半充满状态,则下列叙述中正确的是
| A.X为金属元素,Y为非金属元素 |
| B.X与Y属于同一主族元素 |
| C.X、Y的最外层电子数之和为8 |
| D.X、Y原子结构中的未成对电子数均为3 |
您最近一年使用:0次

 和HD
和HD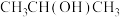 进行核磁共振分析,能得到4组峰,且峰面积之比为1:1:3:3
进行核磁共振分析,能得到4组峰,且峰面积之比为1:1:3:3