硝基苯(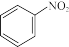 )是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
)是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
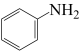
(1)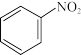 与Fe、盐酸反应生成可生物降解的苯胺(
与Fe、盐酸反应生成可生物降解的苯胺(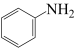 )、
)、 和
和 。
。
①理论上,1mol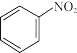 转化为
转化为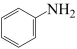 转移的电子的物质的量为
转移的电子的物质的量为_______ 。
②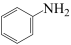 在水中的溶解度大于
在水中的溶解度大于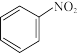 的原的原因是
的原的原因是_______ 。
(2)在酸性条件下,铁炭混合物处理污水中硝基苯时,硝基苯转化过程如下:
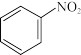

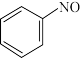

①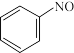 转化为
转化为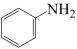 的电极反应式:
的电极反应式:_______ 。
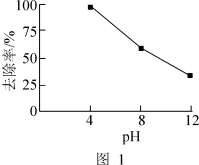
②在其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图1所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(3)向含 和苯胺(
和苯胺(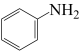 )的酸性溶液中加入双氧水,发生如下反应:
)的酸性溶液中加入双氧水,发生如下反应: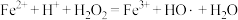
①HO·具有强氧化性,能将溶液中的苯胺氧化成 和
和 。该反应的离子方程式为
。该反应的离子方程式为_______ 。
② 也具有氧化性,设计验证苯胺是被HO·氧化而不是被
也具有氧化性,设计验证苯胺是被HO·氧化而不是被 氧化的实验方案:
氧化的实验方案:_______ 。
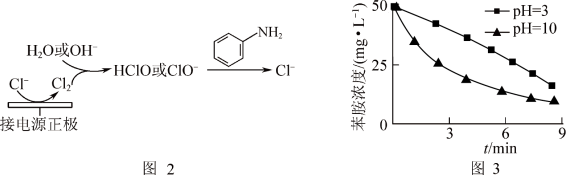
(4)利用电解原理也可以间接氧化处理含苯胺的污水,其原理如图2所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图3所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。(已知: 随着pH减小,氧化性增强)
随着pH减小,氧化性增强)
 )是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
)是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。(1)
 与Fe、盐酸反应生成可生物降解的苯胺(
与Fe、盐酸反应生成可生物降解的苯胺( )、
)、 和
和 。
。①理论上,1mol
 转化为
转化为 转移的电子的物质的量为
转移的电子的物质的量为②
 在水中的溶解度大于
在水中的溶解度大于 的原的原因是
的原的原因是(2)在酸性条件下,铁炭混合物处理污水中硝基苯时,硝基苯转化过程如下:





①
 转化为
转化为 的电极反应式:
的电极反应式:②在其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图1所示。pH越大,硝基苯的去除率越低的原因是

(3)向含
 和苯胺(
和苯胺( )的酸性溶液中加入双氧水,发生如下反应:
)的酸性溶液中加入双氧水,发生如下反应: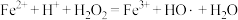
①HO·具有强氧化性,能将溶液中的苯胺氧化成
 和
和 。该反应的离子方程式为
。该反应的离子方程式为②
 也具有氧化性,设计验证苯胺是被HO·氧化而不是被
也具有氧化性,设计验证苯胺是被HO·氧化而不是被 氧化的实验方案:
氧化的实验方案:(4)利用电解原理也可以间接氧化处理含苯胺的污水,其原理如图2所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图3所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是
 随着pH减小,氧化性增强)
随着pH减小,氧化性增强)
更新时间:2022-05-27 16:09:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知下列反应:
①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是_______ 。
(2)判断Cl2与Na2S能否反应?_______ (填“否”或书写离子反应方程式)。
(3)判断I2与NaBr能否反应?_______ (填“否”或书写离子反应方程式)。
(4)已知实验室制取氯气反应为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,由此分析:MnO2在反应中
MnCl2+Cl2↑+2H2O,由此分析:MnO2在反应中_______ 电子,所含元素化合价_______ ,发生_______ 反应。
(5)在硫酸溶液中,NaClO3和Na2SO3能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为_______ 。
A.Cl2O7 B.ClO2 C.Cl2O D.Cl2
①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是
(2)判断Cl2与Na2S能否反应?
(3)判断I2与NaBr能否反应?
(4)已知实验室制取氯气反应为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,由此分析:MnO2在反应中
MnCl2+Cl2↑+2H2O,由此分析:MnO2在反应中(5)在硫酸溶液中,NaClO3和Na2SO3能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为
A.Cl2O7 B.ClO2 C.Cl2O D.Cl2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是__________________ 。
(2) 的俗名
的俗名____________ ,在食品行业中常用于___________ ,其电离方程式___________ 。
(3)明矾的化学式为___________ ,明矾可做净水剂的理由是______________ 。
(4) 、
、 、
、 为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是______________ ,工业上冶炼铁的原理为 。该反应中氧化剂是
。该反应中氧化剂是___________ (填化学式),碳元素被____________ (填“氧化”或“还原”) 。
(5)84消毒液(NaClO)和洁厕灵(HCl)混合会产生有毒气体,不能混合使用,用离子方程式表示其理由:________________ 。
(1)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(2)
 的俗名
的俗名(3)明矾的化学式为
(4)
 、
、 、
、 为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是 。该反应中氧化剂是
。该反应中氧化剂是(5)84消毒液(NaClO)和洁厕灵(HCl)混合会产生有毒气体,不能混合使用,用离子方程式表示其理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面一段材料并回答问题。
(1)K2FeO4中铁元素的化合价为_______ 。
(2)制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确的是_______ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化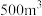 水,至少需要K2FeO4的质量为
水,至少需要K2FeO4的质量为_______ kg。
(5)高铁酸钠Na2FeO4是一种新型的净水剂,可以通过下述反应制取:
①该反应中氧化剂是_______ (用化学式表示,下同),_______ 元素被氧化,还原产物为_______ 。
②用双线桥法在方程式中标出电子转移的情况:_______ 。
(6)将K2FeO4与水反应的化学方程式补充完整_______ 。
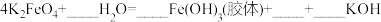
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气 K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 K2FeO4与水反应还能产生具有强吸附性的  胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放 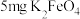 ,即可达到卫生标准 ,即可达到卫生标准 |
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化
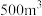 水,至少需要K2FeO4的质量为
水,至少需要K2FeO4的质量为(5)高铁酸钠Na2FeO4是一种新型的净水剂,可以通过下述反应制取:

①该反应中氧化剂是
②用双线桥法在方程式中标出电子转移的情况:
(6)将K2FeO4与水反应的化学方程式补充完整
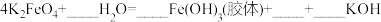
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图,C、D、E、F、X、Y都是惰性电极,A、B为电源,丙为精炼铜装置。接通电源一段时间后,X极液体颜色变深[ 胶粒带正电荷]。
胶粒带正电荷]。
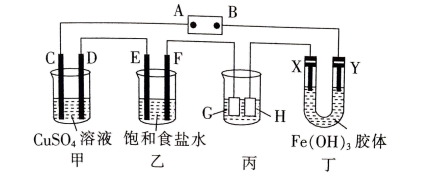
(1)A为电源的___________ (填“正极”或“负极”)。
(2)若甲中装有100mL0.5
 溶液,工作一段时间后,
溶液,工作一段时间后, 恰好完全被消耗,停止通电,此时,测得溶液的pH=
恰好完全被消耗,停止通电,此时,测得溶液的pH=___________ (假设溶液的体积不变)。
(3)通电后,E极的电极反应式为___________ ;检验F极产物的方法是___________ 。
(4)G和H极分别是___________ (填“粗铜”或“纯铜”,下同)和___________ 。
(5)若装置中的溶液都足量,当电路中有0.02mol电子转移时,乙中产生的气体在标准状况下的体积为___________ mL;C、D、G、H极中质量增加的是___________ 极,丙中两极质量变化的绝对值的关系是___________ (填标号)。
a.G极变化大 b.H极变化大 c.两极变化一样大 d.无法确定
 胶粒带正电荷]。
胶粒带正电荷]。
(1)A为电源的
(2)若甲中装有100mL0.5

 溶液,工作一段时间后,
溶液,工作一段时间后, 恰好完全被消耗,停止通电,此时,测得溶液的pH=
恰好完全被消耗,停止通电,此时,测得溶液的pH=(3)通电后,E极的电极反应式为
(4)G和H极分别是
(5)若装置中的溶液都足量,当电路中有0.02mol电子转移时,乙中产生的气体在标准状况下的体积为
a.G极变化大 b.H极变化大 c.两极变化一样大 d.无法确定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学设计了甲烷燃料电池并探究某些工业电解原理(如图所示),其中乙装置为探究氯碱工业原理(X为阳离子交换膜,C为石墨电极),丙装置为探究粗铜精炼原理。请回答下列问题:
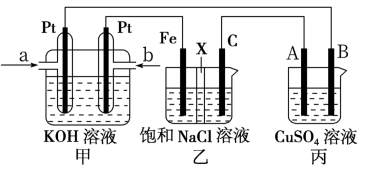
(1)从 b口通入的气体发生的电极反应为______________________________ 。
(2)写出乙中发生的总反应的离子方程式为________________________________ 。
(3)当b口消耗标况下2.24L的气体时,则A极增重质量为__________________

(1)从 b口通入的气体发生的电极反应为
(2)写出乙中发生的总反应的离子方程式为
(3)当b口消耗标况下2.24L的气体时,则A极增重质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
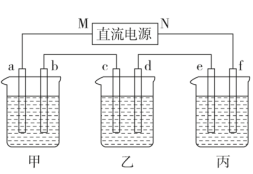
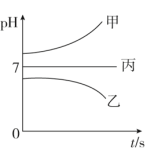
接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:
(1)M为电源的___________ (填“正”或“负”)极,电极b上发生的电极反应为___________ 。
(2)电极e上生成的气体在标准状况下的体积为___________ 。
(3)写出乙烧杯中的电解反应:___________ 。
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解仍继续进行,原因___________ 。
(5)若直流电源换为甲烷氧气燃料(电解质溶液是KOH溶液)电池,那么甲烷燃料电池负极的电极反应为___________ 。
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO 、OH- 、OH- |
在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。

接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:

(1)M为电源的
(2)电极e上生成的气体在标准状况下的体积为
(3)写出乙烧杯中的电解反应:
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解仍继续进行,原因
(5)若直流电源换为甲烷氧气燃料(电解质溶液是KOH溶液)电池,那么甲烷燃料电池负极的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】处理工业废气中的 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。
(1)碱液吸收法。
 可用
可用 溶液吸收,主要反应为:
溶液吸收,主要反应为:

①下列措施能提高尾气中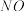 和
和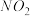 去除率的有
去除率的有_______ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量 溶液
溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是_______ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)催化还原法。
 能在催化剂作用下催化脱除烟气中的
能在催化剂作用下催化脱除烟气中的 ,反应为:
,反应为: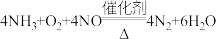 当该反应有
当该反应有 电子转移时,脱除的
电子转移时,脱除的 气体的物质的量为
气体的物质的量为_______ 。
(3)氧化吸收法。
① 氧化
氧化 结合水洗,可产生
结合水洗,可产生 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
② 催化
催化 分解产生
分解产生 ,
, 将
将 氧化为
氧化为 ,反应机理见下图所示。写出③的离子方程式:
,反应机理见下图所示。写出③的离子方程式:_______ ; 脱除率随温度升高呈现下降趋势的主要原因是
脱除率随温度升高呈现下降趋势的主要原因是_______ 。
 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。(1)碱液吸收法。
 可用
可用 溶液吸收,主要反应为:
溶液吸收,主要反应为:

①下列措施能提高尾气中
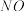 和
和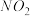 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量
 溶液
溶液②吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是(2)催化还原法。
 能在催化剂作用下催化脱除烟气中的
能在催化剂作用下催化脱除烟气中的 ,反应为:
,反应为: 当该反应有
当该反应有 电子转移时,脱除的
电子转移时,脱除的 气体的物质的量为
气体的物质的量为(3)氧化吸收法。
①
 氧化
氧化 结合水洗,可产生
结合水洗,可产生 和
和 ,该反应的化学方程式为
,该反应的化学方程式为②
 催化
催化 分解产生
分解产生 ,
, 将
将 氧化为
氧化为 ,反应机理见下图所示。写出③的离子方程式:
,反应机理见下图所示。写出③的离子方程式: 脱除率随温度升高呈现下降趋势的主要原因是
脱除率随温度升高呈现下降趋势的主要原因是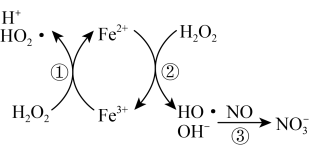
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)请从下列试剂中选择合适的完成指定转化(试剂可重复选用)。
试剂:稀盐酸、 溶液、
溶液、 溶液、
溶液、 溶液、浓硫酸,
溶液、浓硫酸, 溶液
溶液
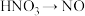 的离子方程式:
的离子方程式:_______ 。
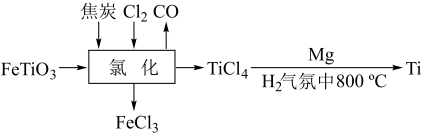
(2)钛铁矿( )在高温下经氯化得到四氯化钛,再制取金属钛的流程如图。写出“氯化”的化学方程式:
)在高温下经氯化得到四氯化钛,再制取金属钛的流程如图。写出“氯化”的化学方程式:__________ 。
(3)在一定条件下,某些化学反应可用下面框图示。请回答下列问题

①若 为一种单质,
为一种单质, 、
、 均为气体且
均为气体且 、
、 均能使澄清石灰水变浑浊,则
均能使澄清石灰水变浑浊,则 为
为____________ 。写出 与
与 在一定条件下反应的化学方程式:
在一定条件下反应的化学方程式:__________ 。
②若 是一种极易溶于水的气体,且水溶液为碱性,
是一种极易溶于水的气体,且水溶液为碱性, 的电子式为
的电子式为__________ :D属于盐,且向A溶液中加入硝酸银溶液后产生不溶于稀硝酸的白色沉淀, 的化学式为
的化学式为____________ 。
(4)在一定条件下, 可将
可将 转化为无污染的物质。
转化为无污染的物质。 与
与 在一定条件下反应,求消耗
在一定条件下反应,求消耗 氨气转移电子的物质的量是
氨气转移电子的物质的量是______ mol。
(1)请从下列试剂中选择合适的完成指定转化(试剂可重复选用)。
试剂:稀盐酸、
 溶液、
溶液、 溶液、
溶液、 溶液、浓硫酸,
溶液、浓硫酸, 溶液
溶液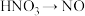 的离子方程式:
的离子方程式:(2)钛铁矿(
 )在高温下经氯化得到四氯化钛,再制取金属钛的流程如图。写出“氯化”的化学方程式:
)在高温下经氯化得到四氯化钛,再制取金属钛的流程如图。写出“氯化”的化学方程式:
(3)在一定条件下,某些化学反应可用下面框图示。请回答下列问题

①若
 为一种单质,
为一种单质, 、
、 均为气体且
均为气体且 、
、 均能使澄清石灰水变浑浊,则
均能使澄清石灰水变浑浊,则 为
为 与
与 在一定条件下反应的化学方程式:
在一定条件下反应的化学方程式:②若
 是一种极易溶于水的气体,且水溶液为碱性,
是一种极易溶于水的气体,且水溶液为碱性, 的电子式为
的电子式为 的化学式为
的化学式为(4)在一定条件下,
 可将
可将 转化为无污染的物质。
转化为无污染的物质。 与
与 在一定条件下反应,求消耗
在一定条件下反应,求消耗 氨气转移电子的物质的量是
氨气转移电子的物质的量是
您最近一年使用:0次




