降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
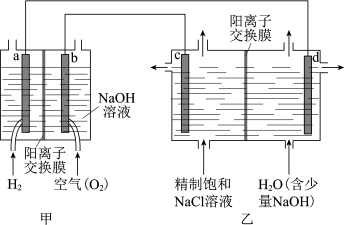
①a极为_______ (填“正”或“负”)极。
②乙装置中电解饱和NaCl溶液的化学方程式为。_______ 。
③下列说法正确的是_______ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
④实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为_______ 。下列生产措施有利于提高Cl2产量、降低阳极O2含量的是_______ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用Cl-浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_______ 。
(1)我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。

①a极为
②乙装置中电解饱和NaCl溶液的化学方程式为。
③下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
④实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用Cl-浓度高的精制饱和食盐水为原料
(2)降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
20-21高二上·北京西城·期末 查看更多[9]
天津市武清区杨村第一中学2023-2024学年高三上学期第三次质量检测化学试题吉林省永吉县第四中学2022-2023学年高二上学期期末考试化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题吉林省长春市清蒲中学2021-2022学年高二上学期期末考试化学试题江西省临川一中暨临川一中实验学校2021-2022学年高二上学期期末考试化学试题北京三中2021-2022学年高二上学期期中考试化学试题北京师范大学第二附属中学未来科技城学校2021-2022学年高二上学期期中考试化学试题江西省南昌市第二中学2020-2021学年高二上学期期末考试化学试题北京市西城区2020-2021学年高二上学期期末考试化学试题
更新时间:2022-04-12 18:28:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图所示,若电解5 min时铜电极质量增加2.16g,试回答:
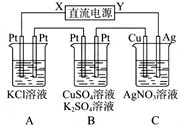
(1)电源电极X名称为______ 。
(2)pH变化:A______ ,B ______ ,C ______ 。
(3)通电5min时,B中共收集224mL气体(标准状况),溶液体积为200mL,(设电解前后溶液不变)则通电前CuSO4溶液的物质的量浓度为______ 。
(4)若A中KCl溶液的体积也是200mL,电解后,溶液的pH是______ (设前后体积无变化)。

(1)电源电极X名称为
(2)pH变化:A
(3)通电5min时,B中共收集224mL气体(标准状况),溶液体积为200mL,(设电解前后溶液不变)则通电前CuSO4溶液的物质的量浓度为
(4)若A中KCl溶液的体积也是200mL,电解后,溶液的pH是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸。A、B分别为铂片,压在滤纸两端,R、S为电池的电极。M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。
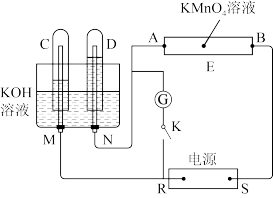
请回答下列问题:
(1)R为___________ (填“正”或“负”)极。
(2)通电一段时间后,M、N电极对应的电解质溶液的pH___________ (填“变大”、“变小”或“不变”);B附近发生的电极反应式为___________ 。
(3)滤纸上的紫色点向___________ (填“A”或“B”)方向移动。
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为___________ (填“正”或“负”)极,电极反应式为___________ 。
Ⅱ.通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
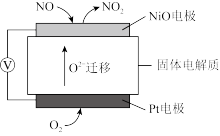
(5)Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
(6)写出NiO电极的电极反应式:___________ 。

请回答下列问题:
(1)R为
(2)通电一段时间后,M、N电极对应的电解质溶液的pH
(3)滤纸上的紫色点向
(4)当C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间后,C、D中的气体逐渐减少,C中的电极为
Ⅱ.通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

(5)Pt电极上发生的是
(6)写出NiO电极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
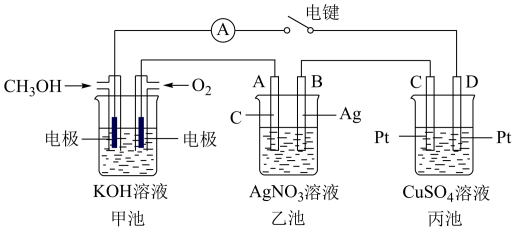
(1)甲池为__________ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式 为______________________________________________ 。
(2)乙池中B电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为__________________________________________ 。
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为______ mL(标准状况)。
(4)丙池中,C上的电极反应式为____________________________________ 。

(1)甲池为
(2)乙池中B电极为
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中,C上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如下图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
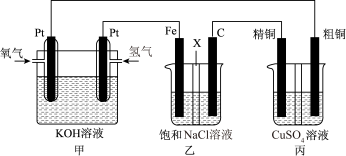
根据要求回答相关问题:
(1)通入氧气的电极为________ (填“正极”或“负极”),负极的电极反应式为______________ 。
(2)铁电极为________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______________ 。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________ 区。(填“铁极”或“石墨极”)
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将________ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为________ ;丙装置中阴极析出铜的质量为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
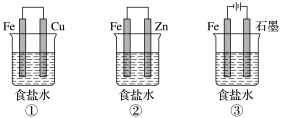
为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_______________________ 。
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
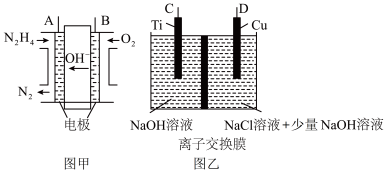
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为____________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是一个化学过程的示意图。已知甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O请回答:
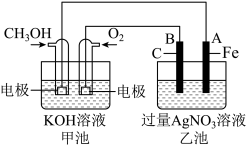
(1)甲池是_______ (填“原电池”或“电解池”),通入O2的电极作为_______ 极,该电极反应式为_______ 。
(2)乙池是_______ (填“原电池”或“电解池”),B电极名称为_______ 极,电极反应式为_______ 。
(3)甲池中溶液的pH_______ (填“增大”、“减小”或“不变”);乙池中溶液的pH_______ (填“增大”、“减小”或“不变”)。
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是_______ mol,甲池中理论上消耗O2_______ mL(标准状况下)。

(1)甲池是
(2)乙池是
(3)甲池中溶液的pH
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是
您最近一年使用:0次



