(1)制备K2FeO4。
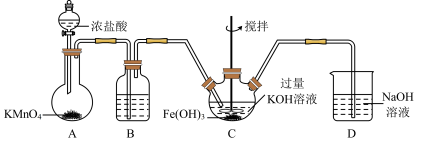
①C为制备K2FeO4装置,KOH溶液过量的原因是
②D为尾气处理装置,发生反应的离子方程式为
(2)探究K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。 |
②方案Ⅱ得出氧化性:Cl2
 (填“>”或“<”)
(填“>”或“<”)(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下,配平及完成上述离子方程式
_______
 +_______H+=_______O2↑+_______ Fe3++_______
+_______H+=_______O2↑+_______ Fe3++_______现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为
相似题推荐
 ):
):
常温溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离 |  |  |  |  |
开始沉淀时( )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时(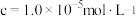 )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
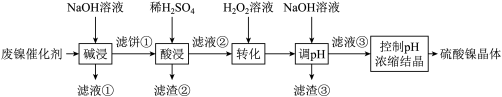
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子可能是
(3)“转化”中可替代
 的物质是
的物质是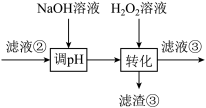
(4)将废镍催化剂a克按流程制成硫酸镍晶体,(镍元素损失10%)并溶于水中配成250ml溶液,取其中25ml于锥形瓶,加入足量的氯化钡溶液充分反应,产生b克沉淀,则废镍催化剂中镍元素的质量分数为
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍锅电池正极材料的NiOOH。写出该反应的离子方程式
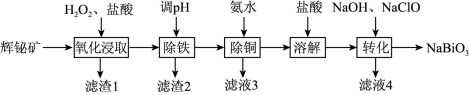
已知:
i.Bi3+易水解;NaBiO3难溶于冷水
ii.“氧化浸取”时,铋元素转化为Bi3+,硫元素转化为硫单质
iii.Cu(OH)2(s)+4NH3(g)
 Cu[(NH3)4]2+(aq)+2OH-(aq) K=4.4×10-7
Cu[(NH3)4]2+(aq)+2OH-(aq) K=4.4×10-7iv.该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Bi3+ |
| 开始沉淀的pH | 7.6 | 2.7 | 4.8 | 4.5 |
| 沉淀完全的pH | 9.6 | 3.7 | 6.4 | 5.5 |
(1)为抑制“氧化浸取”时Bi3+水解,可采取的措施是
(2)“滤渣1”的主要成分是
(3)“氧化浸取”时,FeS转化为Fe3+的离子方程式是
(4)“除铁”时,调节溶液pH值的范围是
(5)“除铜”时发生反应:Cu2+(aq)+4NH3(g)
 Cu[(NH3)4]2+(aq) K=2×1013,则Ksp[Cu(OH)2]=
Cu[(NH3)4]2+(aq) K=2×1013,则Ksp[Cu(OH)2]=(6)“转化”时,生成NaBiO3的离子方程式是
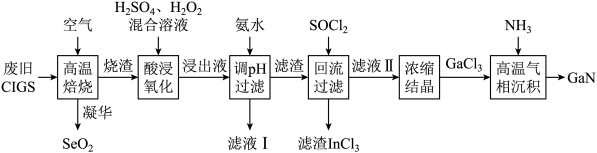
(1)硒(Se)与硫为同族相邻元素,Se在元素周期表中的位置为
(2)镓(Ga)和铟(In)位于元素周期表第ⅢA族,CuIn0.5Ga0.5Se2中Cu的化合价为
(3)“酸浸氧化”发生的主要氧化还原反应为Cu2O+H2O2+H2SO4→CuSO4+H2O(未配平),参加反应的氧化剂与还原剂的质量比为
(4)加入氨水时开始会生成蓝色沉淀,反应的离子方程式为
(5)“滤渣”与SOCl2混合前需要洗涤、干燥,检验滤渣中
 是否洗净的操作为
是否洗净的操作为(6)“高温气相沉积”过程中发生的化学反应方程式为
【推荐1】实验小组用如图装置探究Cl2、Fe3+、I2的氧化性强弱(夹持装置和加热装置已省略,气密性已检验)。
已知:I2遇淀粉溶液变蓝

实验过程:
I.打开弹簧夹K1和K2,通入一段时间N2,再将导管插入B中,继续通入N2一段时间,然后夹紧K1;
Ⅱ.打开活塞a,滴加一定量浓盐酸后关闭活塞a,给A加热;
Ⅲ.当B中的溶液变为黄色时,停止加热,夹紧K2;
IV.打开活塞b,将少量B中溶液滴入C中,关闭活塞b。
(1)操作I中通入一段时间N2的目的是
(2)浸有NaOH溶液的棉花的作用是
(3)B中溶液变黄说明氧化性Cl2>Fe3+,反应的离子方程式是
(4)为探究Fe3+和I2的氧化性强弱,甲、乙、丙三位同学分别完成了上述实验,并检测B中黄色溶液和C中混合溶液中的部分微粒,结果如表所示(忽略空气中O2的影响)。
B中部分微粒 | C中部分微粒 | |
甲 | 既有Fe3+又有Fe2+ | 有I2 |
乙 | 有Fe3+无Fe2+ | 有I2 |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
①检验B中黄色溶液中含有Fe3+的试剂是
②进一步检验IL的实验操作及现象是
③能证明该实验条件下氧化性Fe3+>I2的有
不能证明的请说明理由
④已知碘原子的原子结构示意图为 ,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
,从原子结构角度解释碘原子的得电子能力弱于氯原子的原因
| 步骤1 | 步骤2 | 步骤3 | |
| 试剂 | 适量NaBiO3 | 过量的H2O2溶液 | 适量KI-淀粉混合液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 现象A |
②铋酸钠(NaBiO3)无色,难溶于水;
③淀粉溶液遇到I2变成蓝色。
(1)NaBiO3中Bi的化合价为
(2)请配平步骤2发生反应的化学方程式
 KMnO4+
KMnO4+ H2O2+
H2O2+ H2SO4→
H2SO4→ K2SO4+
K2SO4+ MnSO4+
MnSO4+ O2↑+
O2↑+ ____。
____。(3)步骤2中过量的H2O2可以氧化KI,则步骤3对应的现象A为
(4)由上述现象可得NaBiO3、H2O2、MnO
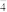 、I2的氧化性由强到弱的顺序为
、I2的氧化性由强到弱的顺序为 )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
(1)
 中S元素的化合价为
中S元素的化合价为(2)三颈烧瓶中发生反应的离子方程式为
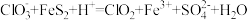 (未配平)。
(未配平)。①该反应中被氧化的元素为
②配平该离子方程式:
(3)设计实验证明ClO2的氧化性比
 的强:
的强:(4)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为
回答下列问题
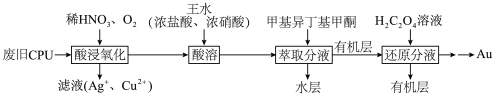
(1)“酸浸氧化”中,为了提高反应速率,可以采取的措施是
(2)“酸浸氧化”中,通入氧气的目的是
(3)“酸溶”时,Pt、Au分别转化为H2PtCl6和HAuCl4,同时有NO生成。Pt溶解的化学方程式是
(4)“萃取分液”后的“水层”中可回收的金属是
(5)从“还原分液”后的“有机层”中回收甲基异丁基甲酮,采用的方法是
(6)理论上消耗1mol草酸(H2C2O4)可得到Au的质量为
(7)提取“滤液”中的Ag+会涉及反应AgCl(s)+2NH3
 [Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为
[Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为  Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
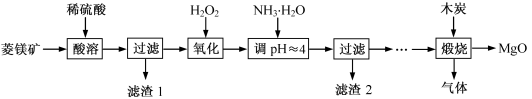
(1)MgCO3与稀硫酸反应的离子方程式为
(2)加入H2O2氧化时,发生反应的化学方程式为
(3)滤渣2的成分是
(4)煅烧过程存在以下反应:
2MgSO4+C
 2MgO+2SO2↑+CO2↑;
2MgO+2SO2↑+CO2↑;MgSO4+C
 MgO+SO2↑+CO↑;
MgO+SO2↑+CO↑;MgSO4+3C
 MgO+S↑+3CO↑。
MgO+S↑+3CO↑。利用如图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是
②A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:
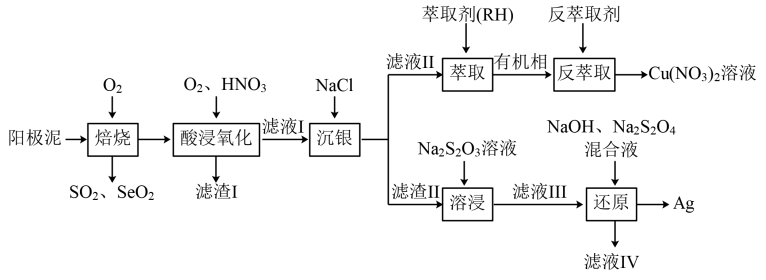
已知:①该工艺中萃取与反萃取原理为:2RH+Cu2+⇌R2Cu+2H+;
②
 在碱性条件下很稳定,有很强的络合能力,与Ag+形成配离子Ag++2
在碱性条件下很稳定,有很强的络合能力,与Ag+形成配离子Ag++2 ⇌[Ag(S2O3)2]3-,常温下该反应的平衡常数
⇌[Ag(S2O3)2]3-,常温下该反应的平衡常数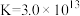 。
。回答下列问题:
(1)试列举可加快“焙烧”速率的措施:
(2)“滤渣I”的主要成分是
(3)“沉银”时证明银离子沉淀完全的操作是
(4)萃取后得到有机相的操作方法是
(5)“溶浸”中发生的反应为AgCl(s)+2
 (aq)⇌[Ag(S2O3)2]3-(aq)+Cl-(aq)该反应中平衡常数K′=
(aq)⇌[Ag(S2O3)2]3-(aq)+Cl-(aq)该反应中平衡常数K′=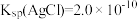 ]。
]。(6)“滤液IV”中含有Na2SO3,则“还原”中发生反应的离子方程式为

滴定过程:向预处理结束的溶液中加入适量蒸馏水和硫酸磷酸混合酸,滴加数滴二苯胺磺酸钠,用重铬酸钾标准溶液滴定,记录终点体积V。
已知:i.钨酸钠(Na2WO4)可用作指示剂,若钨由+6价变为+5价,则溶液变为蓝色。
ii.Sn2+和Ti3+均具有还原性。
iii.氧化性顺序为Cr2O72->Fe3+>WO42-。
iV.二苯胺磺酸钠可用作氧化还原指示剂,本身无色,被氧化后呈现紫红色。
请回答下列问题:
(1)①过程需要加入过量的
(2)②过程后的浅黄色溶液中铁的存在形式为
(3)④过程中K2Cr2O7的作用为
(4)滴定时,滴定管应选用
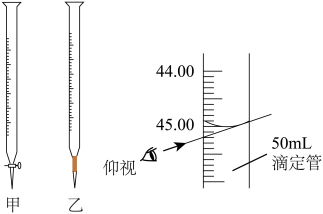
(5)滴定过程中,以二苯胺磺酸钠为指示剂,滴定终点观察到的现象为
(6)现称取0.4g铁矿石进行测定,滴定时共消耗45.00mL0.01mol·L-1K2Cr2O7溶液,则该铁矿石中铁的质量分数为
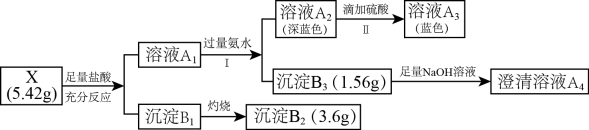
其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为
(3)步骤I中生成沉淀B3的离子方程式为
(4)步骤II中溶液由深蓝色转变为蓝色的原因是
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式
②确定X的化学式为

已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5℃,微溶于水。在较高的盐酸浓度下,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]而溶于乙醚;当盐酸浓度降低时,该化合物解离。
完成下列填空:
(1)操作A的名称是
(2)滴定前,加入适量溶液B进行酸化,则B可能是
a.H2SO3-H3PO4 b. H2SO4-H3PO4
c. HNO3-H3PO4 d. HI-H3PO4
(3)滴定达到终点时,消耗0.1000 mol·L-1 K2Cr2O7溶液6.00 mL(生成物中Cr元素为+3价)。根据该实验数据,试样X中c(Fe3+)为
(4)上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是_______。
| A.稀释被测试样 | B.减少被测试样取量 |
| C.增加平行测定次数 | D.降低滴定剂浓度 |
II.利用下图装置和试剂可以测定铁铝合金样品中的铝含量。

请回答:
(5)下列有关该实验的说法中正确的是_______。
| A.由于恒压分液漏斗的存在,该装置不能进行气密性检查 |
| B.读数前需将量气管C上下移动使B、C中的液面相平 |
| C.反应完成后生成的氢气都要转移至装置B中 |
| D.需要控制NaOH的量以防止产生气体过多超过量气装置的量程 |



