已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,回答下题。
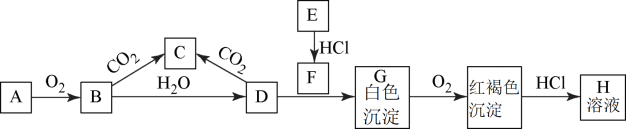
(1)A与水反应的离子反应方程式为:____ 。
(2)写出B转化成C的化学方程式____ 。该反应中的氧化剂是____ ,还原剂是____ ,0.1molB参与该反应,转移电子的数目为____ 。
(3)描述G放置在空气中的颜色变化____ ,化学方程式为:____ 。
(4)写出金属铝与D溶液反应的化学方程式____ 。

(1)A与水反应的离子反应方程式为:
(2)写出B转化成C的化学方程式
(3)描述G放置在空气中的颜色变化
(4)写出金属铝与D溶液反应的化学方程式
更新时间:2022-08-19 20:20:30
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,N常用来杀菌消毒。请按要求填空:

(1)淡黄色物质M是___________ (填化学式),物质N是___________ (填化学式)。
(2)写出M与水反应的离子方程式为___________ 。
(3) 与
与 反应的化学反应方程式为
反应的化学反应方程式为___________ 。
(4)除去下列括号中少量杂质,写出相关化学方程式或离子方程式:
① 固体(
固体( )化学方程式
)化学方程式___________ 。
② 溶液(
溶液( )离子方程式
)离子方程式___________ 。

(1)淡黄色物质M是
(2)写出M与水反应的离子方程式为
(3)
 与
与 反应的化学反应方程式为
反应的化学反应方程式为(4)除去下列括号中少量杂质,写出相关化学方程式或离子方程式:
①
 固体(
固体( )化学方程式
)化学方程式②
 溶液(
溶液( )离子方程式
)离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。已知A的气态氢化物能与其最高价氧化物的水化物反应生成盐,B原子最外层电子数是其电子层数的3倍,C+和D3+的电子层结构相同,B与E属于同一主族。
(1)E在元素周期表中的位置是_______ 。
(2)上述元素形成的最高价氧化物的水化物碱性最强的物质是_______ (填化学符号)。
(3)由上述元素中的一种或几种组成的物质甲可以发生如下反应:
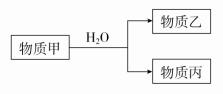
①若丙的水溶液是强碱性溶液,则甲为_______ 或_______ (填化学式)。
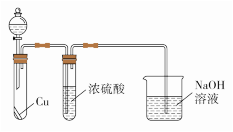
②若乙遇空气变为红棕色,物质丙为一种强酸,则物质甲与水反应的化学方程式为_______ 。有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确。用如上图装置进行实验时,分液漏斗中应加入_______ (填试剂名称)。实验过程中,浓硫酸中未发现有气体逸出且溶液变为红棕色,由此得出的结论是_______ 。
(4)某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如图转化关系图,图中A、B、C、D是由短周期元素组成的物质。并用于研究的性质及其变化。

请回答:若A为单质,其焰色试验为黄色,C为淡黄色固体。
①C中阴阳离子个数比为_______ 。
②下列说法正确的是_______ (填字母)。
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(5)若A为能使红色石蕊试纸变蓝的气体,C为红棕色气体。A与C反应生成E和水,E是空气中含量最多的气体,写出A与C发生反应的化学方程式_______ 。当生成19.6gE时,转移电子的物质的量为_______ mol。
(1)E在元素周期表中的位置是
(2)上述元素形成的最高价氧化物的水化物碱性最强的物质是
(3)由上述元素中的一种或几种组成的物质甲可以发生如下反应:


①若丙的水溶液是强碱性溶液,则甲为
②若乙遇空气变为红棕色,物质丙为一种强酸,则物质甲与水反应的化学方程式为
(4)某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如图转化关系图,图中A、B、C、D是由短周期元素组成的物质。并用于研究的性质及其变化。

请回答:若A为单质,其焰色试验为黄色,C为淡黄色固体。
①C中阴阳离子个数比为
②下列说法正确的是
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(5)若A为能使红色石蕊试纸变蓝的气体,C为红棕色气体。A与C反应生成E和水,E是空气中含量最多的气体,写出A与C发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学社团小组设计了如图所示装置,验证CO2跟Na2O2反应时需要与水接触。完成下列填空:
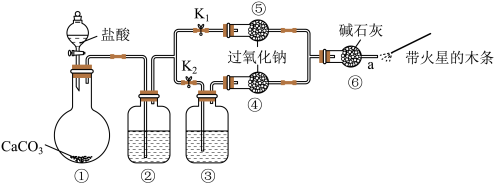
(1)装置①中反应的离子方程式_______ 。
(2)装置②中的试剂是_______ ,装置③中的试剂是_______ (均选填字母)。
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4 d.水
(进行实验)
步骤1,打开K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处;
步骤2:打开K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条实验现象分别是步骤1_______ (选填字母),步骤2现象_______ (选填字母)。
A.带火星的木条复燃 B.带火星的木条不复燃
(实验反思)
(4)Na2O2与CO2反应的化学方程式是_______ 。关于该反应,下列叙述中正确的有_______ (选填字母)。
A.有离子键、共价键的断裂与生成
B.CO2是氧化剂,Na2O2是还原剂
C.反应物和生成物中都含离子化合物
D.转移2mol电子,生成气体体积为22.4L
(5)有同学提出质疑:上述实验不足以证明有水存在时Na2O2与CO2发生了化学反应。其理由是_______ 。

(1)装置①中反应的离子方程式
(2)装置②中的试剂是
a.饱和NaHCO3溶液 b.饱和Na2CO3溶液 c.浓H2SO4 d.水
(进行实验)
步骤1,打开K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处;
步骤2:打开K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条实验现象分别是步骤1
A.带火星的木条复燃 B.带火星的木条不复燃
(实验反思)
(4)Na2O2与CO2反应的化学方程式是
A.有离子键、共价键的断裂与生成
B.CO2是氧化剂,Na2O2是还原剂
C.反应物和生成物中都含离子化合物
D.转移2mol电子,生成气体体积为22.4L
(5)有同学提出质疑:上述实验不足以证明有水存在时Na2O2与CO2发生了化学反应。其理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
(1)元素b的一种核素可以测定文物年代,该核素是___________ (填化学符号),e在元素周期表中所在的位置是___________ 。
(2)a、c、d三种元素形成一种化合物的电子式为___________ ,该化合物含有的化学键类型___________ (填“离子键”、“极性键”、“非极性键”)。
(3)写出单质f与d的最高价氧化物对应水化物反应的离子反应方程式___________ 。
(4)元素g、h、i的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (用化学式表示)。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | h | i | ||||||||||||
| j |
(2)a、c、d三种元素形成一种化合物的电子式为
(3)写出单质f与d的最高价氧化物对应水化物反应的离子反应方程式
(4)元素g、h、i的最高价氧化物对应水化物的酸性由强到弱的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。

(1)写出下列物质的化学式A:_______________ ,Q:_____________ ,W:__________________ 。
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:_______________________
②R与B溶液反应时的离子方程式:___________________________________
③D与盐酸反应的离子方程式:_______________________________________
(3)简述检验气体C的方法:___________________________________________

(1)写出下列物质的化学式A:
(2)按要求写出下列反应方程式:
①H在潮湿空气中变成M的过程中的化学方程式:
②R与B溶液反应时的离子方程式:
③D与盐酸反应的离子方程式:
(3)简述检验气体C的方法:
您最近一年使用:0次
【推荐3】工业上常用绿矾( )作还原剂
)作还原剂
(1)检验久置绿矾是否变质可用试剂_______ 。
(2)①工业上常用 溶液刻蚀铜电路板,反应的离子方程式为
溶液刻蚀铜电路板,反应的离子方程式为_______ 。
腐蚀废液含 、
、 、
、 ,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如下:
,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如下:

②操作I中使用的玻璃仪器除烧杯、玻璃棒外还有_______ ;腐蚀废液中加入过量铁粉的目的_______ 。
③固体A中含有_______ ;操作II的过程是:蒸发至出现一层晶膜、_______ 、过滤、洗涤、常温晾干。
④反应I中生成 沉淀同时有
沉淀同时有 和水生成,反应的离子方程式为
和水生成,反应的离子方程式为_______ 。
(3)绿矾可用于缺铁性贫血的补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量 溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论
溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论_______ 。(已知: 遇铁氰化钾溶液产生蓝色沉淀)
遇铁氰化钾溶液产生蓝色沉淀)
(4)取镁铝合金两等份,分别加入足量稀盐酸和NaOH溶液,合金全部溶解并得到标准状况下H2分别为5.6L和3.36L。试计算:
①每份该合金中铝的物质的量_______ ;
②该合金中镁铝物质的量之比_______ 。
 )作还原剂
)作还原剂(1)检验久置绿矾是否变质可用试剂
(2)①工业上常用
 溶液刻蚀铜电路板,反应的离子方程式为
溶液刻蚀铜电路板,反应的离子方程式为腐蚀废液含
 、
、 、
、 ,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如下:
,某小组欲从腐蚀废液中回收铜及制绿矾,工艺流程如下:
②操作I中使用的玻璃仪器除烧杯、玻璃棒外还有
③固体A中含有
④反应I中生成
 沉淀同时有
沉淀同时有 和水生成,反应的离子方程式为
和水生成,反应的离子方程式为(3)绿矾可用于缺铁性贫血的补铁剂,医生建议与维生素C同服。某同学探究维生素C的作用,取少量
 溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论
溶液于试管中,加入维生素C片2片,并振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论 遇铁氰化钾溶液产生蓝色沉淀)
遇铁氰化钾溶液产生蓝色沉淀)(4)取镁铝合金两等份,分别加入足量稀盐酸和NaOH溶液,合金全部溶解并得到标准状况下H2分别为5.6L和3.36L。试计算:
①每份该合金中铝的物质的量
②该合金中镁铝物质的量之比
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学设计如下图所示装置(气密性已检查)制备Fe(OH)2白色沉淀。
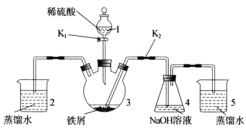
请填写下列空白:
(1)仪器1的名称是______ 。装置5的作用是______ 。
(2)实验开始时,关闭K2、打开K1,反应一段时间后,再打开K2、关闭K1,发现装置3中溶液不能进入装置4中。请改进装置,使溶液能进入装置4中:______ 。
(3)装置改进后,将装置3中反应后溶液压入装置4中,在装置4中立即析出白色絮状沉淀,迅速变为灰绿色,最终变为红褐色。请写出装置4中涉及到的化学方程式___ 、___ ,若始终没有观察到白色沉淀,从实验操作过程分析可能的原因是___ 。

请填写下列空白:
(1)仪器1的名称是
(2)实验开始时,关闭K2、打开K1,反应一段时间后,再打开K2、关闭K1,发现装置3中溶液不能进入装置4中。请改进装置,使溶液能进入装置4中:
(3)装置改进后,将装置3中反应后溶液压入装置4中,在装置4中立即析出白色絮状沉淀,迅速变为灰绿色,最终变为红褐色。请写出装置4中涉及到的化学方程式
您最近一年使用:0次
【推荐2】在常温下, 与水并不起反应,但在高温下,
与水并不起反应,但在高温下, 与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原性铁粉和棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“
与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原性铁粉和棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“ 与水蒸气的反应实验”。请回答下列问题:
与水蒸气的反应实验”。请回答下列问题:

(1)仪器A的作用是_______ 。
(2)硬质玻璃管B中发生反应的化学方程式为_______ 。
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是_______ 。
(4)无水硫酸铜粉末变蓝色,黑色氧化铜变红说明铁跟水蒸气反应生成的气体为_______ (填化学式)。
(5)某同学利用反应后的固体物质进行如下实验:

①某同学发现实验中加入过量新制氯水,放置一段时间后,深红色会逐渐褪去,褪色后的溶液中继续滴加 溶液,又出现红色,则褪色的原因可能是
溶液,又出现红色,则褪色的原因可能是_______ 。
②该同学想用高锰酸钾酸性溶液检验淡黄色溶液中是否含有 离子,写出检验反应的离子方程式
离子,写出检验反应的离子方程式_______ 。
③该同学想用淡黄色溶液制 溶液,可加入过量的
溶液,可加入过量的_______ ,写出该反应离子反应方程式_______ 。
(6)以物质的类别为横坐标,化合价为纵坐标绘制的图象叫价类图。如下图是铁的价类图,Y物质为_______ ,写出Y在潮湿的空气中转化为图中同类别物质的化学方程式_______ 。

 与水并不起反应,但在高温下,
与水并不起反应,但在高温下, 与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原性铁粉和棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“
与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原性铁粉和棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“ 与水蒸气的反应实验”。请回答下列问题:
与水蒸气的反应实验”。请回答下列问题:
(1)仪器A的作用是
(2)硬质玻璃管B中发生反应的化学方程式为
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是
(4)无水硫酸铜粉末变蓝色,黑色氧化铜变红说明铁跟水蒸气反应生成的气体为
(5)某同学利用反应后的固体物质进行如下实验:

①某同学发现实验中加入过量新制氯水,放置一段时间后,深红色会逐渐褪去,褪色后的溶液中继续滴加
 溶液,又出现红色,则褪色的原因可能是
溶液,又出现红色,则褪色的原因可能是②该同学想用高锰酸钾酸性溶液检验淡黄色溶液中是否含有
 离子,写出检验反应的离子方程式
离子,写出检验反应的离子方程式③该同学想用淡黄色溶液制
 溶液,可加入过量的
溶液,可加入过量的(6)以物质的类别为横坐标,化合价为纵坐标绘制的图象叫价类图。如下图是铁的价类图,Y物质为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】健康人体内含铁元素大约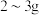 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:_____ ;试剂2的化学式为_____ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_____ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:______ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入______ ,防止 被氧化。
被氧化。
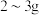 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近一年使用:0次



