钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题。
(1)K和Cr属于同一周期,且基态原子核外最外层电子构型相同,但金属K的熔点比金属Cr低,试解释原因_______ 。
(2)① 晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为
晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为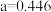 nm,晶胞中K、I、O分别处于顶角、体心、面心位置如图所示。K与O间的最短距离为
nm,晶胞中K、I、O分别处于顶角、体心、面心位置如图所示。K与O间的最短距离为______ nm,与K紧邻的O个数为________ 。
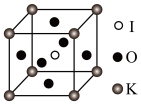
②在 晶胞结构的另一种表示中,I处于各顶角位置,则K处于
晶胞结构的另一种表示中,I处于各顶角位置,则K处于______ 位置,O处于______ 位置。
(3)五氮阴离子盐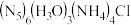 的晶体密度为
的晶体密度为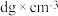 ,其立方晶胞参数为anm,晶胞中含有y个[
,其立方晶胞参数为anm,晶胞中含有y个[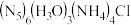 ]单元,该单元的相对质量为M,则y的计算表达式为
]单元,该单元的相对质量为M,则y的计算表达式为______ 。
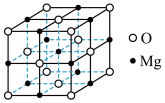
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为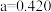 nm,则
nm,则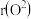 为
为______ nm。MnO也属于NaCl型结构,晶胞参数为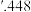 nm,则
nm,则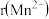 为
为______ nm。
(1)K和Cr属于同一周期,且基态原子核外最外层电子构型相同,但金属K的熔点比金属Cr低,试解释原因
(2)①
 晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为
晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为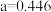 nm,晶胞中K、I、O分别处于顶角、体心、面心位置如图所示。K与O间的最短距离为
nm,晶胞中K、I、O分别处于顶角、体心、面心位置如图所示。K与O间的最短距离为
②在
 晶胞结构的另一种表示中,I处于各顶角位置,则K处于
晶胞结构的另一种表示中,I处于各顶角位置,则K处于(3)五氮阴离子盐
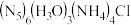 的晶体密度为
的晶体密度为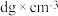 ,其立方晶胞参数为anm,晶胞中含有y个[
,其立方晶胞参数为anm,晶胞中含有y个[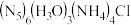 ]单元,该单元的相对质量为M,则y的计算表达式为
]单元,该单元的相对质量为M,则y的计算表达式为(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为
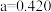 nm,则
nm,则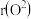 为
为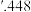 nm,则
nm,则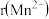 为
为
更新时间:2022-08-16 16:15:13
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】利用失效钒电解液[主要成分是 、
、 及
及 ]回收制备
]回收制备 ,其工艺流程如图所示:
,其工艺流程如图所示:

已知:部分含钒物质在水溶液中的主要存在形式:
(1) 钒元素的化合价为
钒元素的化合价为_______ 。
(2)“氧化”时, 转化为
转化为 ,
, 转化为
转化为 ,则参加反应的
,则参加反应的 与
与 物质的量之比为
物质的量之比为_______ 。
(3)“调节 ”时,应控制范围为
”时,应控制范围为_______ 。
(4)若“沉钒”前溶液中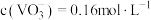 ,忽略溶液体积变化,为使钒元素的沉降率达到
,忽略溶液体积变化,为使钒元素的沉降率达到 ,则“沉钒”后溶液中
,则“沉钒”后溶液中
_______  [已知:常温下,
[已知:常温下,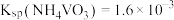 ]。
]。
(5)“沉钒”后,滤液中主要含有的离子有 、
、 ,还有
,还有_______ 。
(6)“煅烧”时, 受热分解,发生非氧化还原反应,其化学方程式为
受热分解,发生非氧化还原反应,其化学方程式为_______ 。
(7)工业上用 在高温下还原
在高温下还原 制取金属钒。
制取金属钒。
①基态铁原子与基态钒原子的未成对电子的数目比为_______ 。
②单质钒晶体的晶胞结构如图所示。已知晶胞的边长为 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 。则晶体密度为
。则晶体密度为_______  (列出表达式即可)。
(列出表达式即可)。

 、
、 及
及 ]回收制备
]回收制备 ,其工艺流程如图所示:
,其工艺流程如图所示:
已知:部分含钒物质在水溶液中的主要存在形式:
 |  | 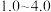 | 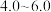 |  | 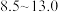 | 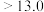 |
| 主要存在形式 |  |  | 多钒酸根 |  | 多钒酸根 |  |
 钒元素的化合价为
钒元素的化合价为(2)“氧化”时,
 转化为
转化为 ,
, 转化为
转化为 ,则参加反应的
,则参加反应的 与
与 物质的量之比为
物质的量之比为(3)“调节
 ”时,应控制范围为
”时,应控制范围为(4)若“沉钒”前溶液中
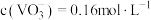 ,忽略溶液体积变化,为使钒元素的沉降率达到
,忽略溶液体积变化,为使钒元素的沉降率达到 ,则“沉钒”后溶液中
,则“沉钒”后溶液中
 [已知:常温下,
[已知:常温下,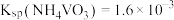 ]。
]。(5)“沉钒”后,滤液中主要含有的离子有
 、
、 ,还有
,还有(6)“煅烧”时,
 受热分解,发生非氧化还原反应,其化学方程式为
受热分解,发生非氧化还原反应,其化学方程式为(7)工业上用
 在高温下还原
在高温下还原 制取金属钒。
制取金属钒。①基态铁原子与基态钒原子的未成对电子的数目比为
②单质钒晶体的晶胞结构如图所示。已知晶胞的边长为
 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 。则晶体密度为
。则晶体密度为 (列出表达式即可)。
(列出表达式即可)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氮元素可形成很多重要的化合物,其中叠氮化钠(NaN3)被广泛应用于汽车安全气囊。叠氮化钠的制取方法是:①金属钠与液态氨反应得NaNH2,②NaNH2与N2O按物质的量2:1反应可生成NaN3、NaOH和一种气体。
(1)请写出反应②的化学方程式为:___ 。
(2)比较NH 和NH3的键角∠HNH的大小:NH
和NH3的键角∠HNH的大小:NH
____ NH3(填“>”或“<”或“=”),请用价层电子对互斥规律解释____ 。
(3)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+Fe2O3=3Na2O+2Fe+9N2;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如图所示):
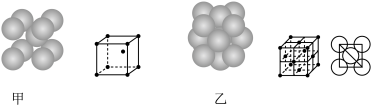
晶胞甲中铁原子的配位数为:___ ,晶胞乙中铁原子的堆积方式为:___ 。晶胞乙中铁原子半径为a pm,NA表示阿伏加德罗常数,摩尔质量为Mg/mol。则该晶体的密度可表示为:___ g/cm3。
(1)请写出反应②的化学方程式为:
(2)比较NH
 和NH3的键角∠HNH的大小:NH
和NH3的键角∠HNH的大小:NH
(3)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+Fe2O3=3Na2O+2Fe+9N2;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如图所示):

晶胞甲中铁原子的配位数为:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】钛酸锌(ZnTiO3)是一种抗菌涂料,应用于人造骨骼等生物移植技术。回答下列问题:
(1)基态Zn原子的电子占据能量最高的能层符号为_____________ ,与Zn同周期的所有副族元素的基态原子中,最外层电子数与Zn相同的元素有___________ 种
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C____ B(选填“>或“<”);第一电离能N>O,原因是__________________________________________ 。
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
① 的空间构型为
的空间构型为_____________ ,其中硫原子采用____________ 杂化。
②与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_________________ (任写一种即可)
(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有___________ 个。
②该化合物的化学式为_________________________________ 。
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为__________________ g/cm3(列式即可)
(1)基态Zn原子的电子占据能量最高的能层符号为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
①
 的空间构型为
的空间构型为②与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有
②该化合物的化学式为
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。
(1)该合金的化学式为__________________ ;
(2)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为:______________________________________ 。
(3)下列关于该贮氢材料及氢气的说法中,正确的是_________ ( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(4)晶体铜是面心立方堆积,在铜的一个晶胞中,把顶点上的铜原子换成Au,可得一种合金,该合金也具有储氢功能,储氢时,氢原子进入到Au和Cu原子构成的的四面体空隙中,则达到最大储氢量的化学式为_____________ 。
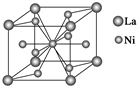
(1)该合金的化学式为
(2)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为:
(3)下列关于该贮氢材料及氢气的说法中,正确的是
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(4)晶体铜是面心立方堆积,在铜的一个晶胞中,把顶点上的铜原子换成Au,可得一种合金,该合金也具有储氢功能,储氢时,氢原子进入到Au和Cu原子构成的的四面体空隙中,则达到最大储氢量的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】原子序数依次增大的短周期主族元素a、b、c、d、e中,a的最外层电子数为其周期数的2倍;b的-2价离子比d的-2价离子少8个电子;c的+1价离子比e的-1价离子少8个电子。
回答下列问题:
(1)元素a为_________ (填元素符号,后同),c为____________ 。
(2)由这些元素形成的双原子分子为_____________________ (填化学式)。
(3)这些元素的单质或由它们形成的AB型化合物中,其晶体类型属于共价晶体的是___________ (填物质名称),属于金属晶体的是_____________ (填化学式,下同),属于离子晶体的是__________ ,属于分子晶体的是____________ 。
回答下列问题:
(1)元素a为
(2)由这些元素形成的双原子分子为
(3)这些元素的单质或由它们形成的AB型化合物中,其晶体类型属于共价晶体的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)请写出表中元素N的基态原子电子排布式___________ 。
(2)C、 D、E三种元素的第一电离能由大到小的顺序为___________ (用元素符号表示关系)。
(3)元素B、G形成的单质熔点更高的是________ (填化学式),原因是___________ 。
(4)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是________ (填“极性”或“非极性”)分子。根据等电子原理: 中氮原子的杂化类型是
中氮原子的杂化类型是______ ,1 molC2H2 分子中含有π键的数目为________ mol。
(5)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________ (填序号),CS2分子的空间构型是________ 。
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为________ 。
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | ||||||||||||||||
试回答下列问题:
(1)请写出表中元素N的基态原子电子排布式
(2)C、 D、E三种元素的第一电离能由大到小的顺序为
(3)元素B、G形成的单质熔点更高的是
(4)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
 中氮原子的杂化类型是
中氮原子的杂化类型是(5)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
您最近一年使用:0次




