在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+与CrO 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
(1)溶液中c(Ag+)=_______ 。
(2)溶液中c(CrO )=
)=_______ (写出具体计算过程)。
 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl-恰好沉淀完全时(浓度等于1.0×10-5mol/L),(已知25℃时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)。求:(1)溶液中c(Ag+)=
(2)溶液中c(CrO
 )=
)=
更新时间:2022-09-16 22:14:49
|
相似题推荐
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)在25℃下,向浓度均为0.1 mol∙L−1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_______ 沉淀(填化学式),生成该沉淀的离子方程式为_______ 。(已知25℃时,Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20)
(2)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol∙L−1盐酸、③0.1 mol∙L−1氯化镁溶液、④0.1 mol∙L−1硝酸银溶液中,c(Ag+)由大到小的顺序为:_______
(3)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
=_______ 。
(4)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为_______ mol∙L−1。
(5)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是_______

A.加入Na2SO4可使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol∙L−1盐酸、③0.1 mol∙L−1氯化镁溶液、④0.1 mol∙L−1硝酸银溶液中,c(Ag+)由大到小的顺序为:
(3)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
 =
=(4)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
(5)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是

A.加入Na2SO4可使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)在25℃下,向浓度均为0.1 mol∙L−1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_______ 沉淀(填化学式),生成该沉淀的离子方程式为_______ 。(已知25℃时,Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20)
(2)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol∙L−1盐酸、③0.1 mol∙L−1氯化镁溶液、④0.1 mol∙L−1硝酸银溶液中,c(Ag+)由大到小的顺序为:_______
(3)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
=_______ 。
(4)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为_______ mol∙L−1。
(5)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是_______

A.加入Na2SO4可使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol∙L−1盐酸、③0.1 mol∙L−1氯化镁溶液、④0.1 mol∙L−1硝酸银溶液中,c(Ag+)由大到小的顺序为:
(3)已知:Ksp(AgBr)=5.4×10−13,Ksp(AgCl)=1.8×10−10,向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
 =
=(4)已知在25℃时,Ksp[Mg(OH)2]=3.2×10−11。25℃时,向0.02 mol∙L−1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
(5)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是

A.加入Na2SO4可使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.b点有BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】按要求填空:
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至______ 。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_________ ,由水电离出的c(OH-)=________ mol·L-1。
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为_____ 。
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10﹣38,Cu(OH)2的溶度积Ksp=3.0×10﹣20,通常认为残留在溶液中的离子浓度小于1×10﹣5 mol•L﹣1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L﹣1,则:
(1)Cu(OH)2开始沉淀时溶液的pH为_____
(2)Fe3+完全沉淀时溶液的pH为_____
(3)通过计算确定上述方案_____ (填“可行”或“不可行”);理由_____ 。
(1)Cu(OH)2开始沉淀时溶液的pH为
(2)Fe3+完全沉淀时溶液的pH为
(3)通过计算确定上述方案
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】已知常温下PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3 mol·L-1,Pb(NO3)2溶液与KI溶液混合可形成PbI2沉淀。现将浓度为2×10-3 mol·L-1的Pb(NO3)2溶液与一定浓度的KI溶液等体积混合,则生成沉淀所需KI溶液的最小浓度为______ 。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】按要求填空:
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至______ 。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_________ ,由水电离出的c(OH-)=________ mol·L-1。
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为_____ 。
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为
您最近一年使用:0次

 为指示剂,以
为指示剂,以 标准溶液滴定溶液中
标准溶液滴定溶液中 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中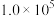
 )时,溶液中
)时,溶液中 为
为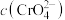 等于
等于 、AgCl的
、AgCl的 分别为
分别为 和
和 )。
)。


