氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______ (选填编号)。
a.高炉炼铁 b.腐蚀印刷电路板 c.高温煅烧石灰石 d.燃放烟花炮竹
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关系”可用下图表示。
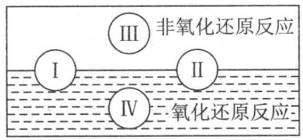
试写出有水参加且符合反应类型IV的一个化学方程式:_______ 。
(3)工业上利用 和
和 反应来制取单质
反应来制取单质 。
。
①配平下列化学方程式并标明电子转移的方向和数目:_______ 。
_____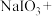 _____NaHSO3→_____
_____NaHSO3→_____
②该反应还原剂是____ ,____ 元素被还原,若生成1mol氧化产物则转移电子数目为___ NA。
(4)已知: 、
、 、
、 、
、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
_______ I-(填“ ”或“
”或“ ”),完成该反应
”),完成该反应_______ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a.高炉炼铁 b.腐蚀印刷电路板 c.高温煅烧石灰石 d.燃放烟花炮竹
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关系”可用下图表示。

试写出有水参加且符合反应类型IV的一个化学方程式:
(3)工业上利用
 和
和 反应来制取单质
反应来制取单质 。
。①配平下列化学方程式并标明电子转移的方向和数目:
_____
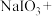 _____NaHSO3→_____
_____NaHSO3→_____
②该反应还原剂是
(4)已知:
 、
、 、
、 、
、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
 ”或“
”或“ ”),完成该反应
”),完成该反应
更新时间:2022-09-24 08:45:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)(Ⅰ)
(1)反应(Ⅰ)中氧化剂是___ 。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g) 2NO2(g) ΔH(Ⅱ)
2NO2(g) ΔH(Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)中ΔH___ 0(填“>”或“<”),保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,混合气体的颜色__ (填“变深”或“变浅”)。

(1)反应(Ⅰ)中氧化剂是
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)
 2NO2(g) ΔH(Ⅱ)
2NO2(g) ΔH(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)中ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单后硫S,可实现废物利用,保护环境,写出其中一个反应的化学方程式___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“铜绿”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、 、
、 作用产生的,化学式为[
作用产生的,化学式为[ ],“铜绿”能跟酸反应生成铜盐、
],“铜绿”能跟酸反应生成铜盐、 和
和 ,某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
,某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
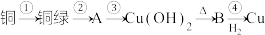
(1)从物质分类标准看, 属于
属于___________ , 属于
属于___________ 。(填字母)
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式___________ 。
(3)写出④的化学方程式___________ 。
(4)请写出铜绿与盐酸反应的化学方程式:___________ 。
(5)上述转化过程中属于置换反应的是___________ (填序号,下同),属于氧化还原反应的是___________ 。
(6)王军同学觉得上述转化,步骤繁琐,浪费资源,设计以下流程,请你帮他补充完整:___________
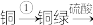 ___________
___________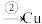
 、
、 作用产生的,化学式为[
作用产生的,化学式为[ ],“铜绿”能跟酸反应生成铜盐、
],“铜绿”能跟酸反应生成铜盐、 和
和 ,某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
,某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。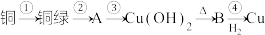
(1)从物质分类标准看,
 属于
属于 属于
属于A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式
(3)写出④的化学方程式
(4)请写出铜绿与盐酸反应的化学方程式:
(5)上述转化过程中属于置换反应的是
(6)王军同学觉得上述转化,步骤繁琐,浪费资源,设计以下流程,请你帮他补充完整:
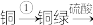 ___________
___________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】配平下列反应的化学方程式,标出电子转移方向和数目,并回答有关问题:
Na2Cr2O7+KI+HCl →CrCl3 +NaCl +KCl+I2 +__________ __________ 。
(1)上面反应中氧化剂是____ ,被氧化的元素是___ 。
(2)HCl的作用___ 。
(3)若反应过程中有0.50molI2被氧化出来,且有__ mol电子发生了转移。
Na2Cr2O7+KI+HCl →CrCl3 +NaCl +KCl+I2 +
(1)上面反应中氧化剂是
(2)HCl的作用
(3)若反应过程中有0.50molI2被氧化出来,且有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为建设美丽浙江,浙江省政府开展“五水共治”。
(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2。工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:_______________ 。
(2)某地污水中的有机污染物主要成分是三氯乙烯 (C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式_________________ 。
(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2。工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:
(2)某地污水中的有机污染物主要成分是三氯乙烯 (C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质检验、分离、提纯和制备是化学实验中的常见操作。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是_______ (用离子方程式表示)。
(2)检验食盐中所含阳离子的实验操作名称是_______ 。
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是_______ 。
(4)除去Cl2中混有的HCl气体所用的试剂是_______ 。
(5)实验室制备氯气的化学反应方程式为_______ 请在方程式中标出电子转移的方向和数目。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是
(2)检验食盐中所含阳离子的实验操作名称是
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是
(4)除去Cl2中混有的HCl气体所用的试剂是
(5)实验室制备氯气的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的离子方程式。
(1)FeBr2溶液与Cl2反应
①Cl2少量:___________ ;
②n(FeBr2)∶n(Cl2)=1∶1:___________ ;
③Cl2过量:___________ 。
类似该反应的还有FeI2溶液与Cl2的反应。
(2)NH4HCO3溶液与NaOH溶液反应
①NaOH少量:___________ ;
②NaOH足量:___________ 。
类似该反应的还有NH4HSO4溶液或NH4Al(SO4)2溶液与NaOH溶液的反应。
(1)FeBr2溶液与Cl2反应
①Cl2少量:
②n(FeBr2)∶n(Cl2)=1∶1:
③Cl2过量:
类似该反应的还有FeI2溶液与Cl2的反应。
(2)NH4HCO3溶液与NaOH溶液反应
①NaOH少量:
②NaOH足量:
类似该反应的还有NH4HSO4溶液或NH4Al(SO4)2溶液与NaOH溶液的反应。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4,极易溶于水)是常见的水处理剂,其原理如图所示。

【资料】向胶体中加入电解质后,胶体因失去稳定性使分散质粒子聚集而产生沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
(1)K2FeO4中铁元素的化合价为___________ 。
(2)过程①中活性菌表现了___________ (填“氧化”或“还原”)性,该过程的还原产物是___________ (填离子符号);过程③属于___________ (填“物理”或“化学”)变化。
(3)根据上述原理,K2FeO4作水处理剂时,其主要作用有___________ (填两个)。
(4)可用次氯酸钾在碱性条件下与氢氧化铁反应得到K2FeO4,写出制备K2FeO4的离子方程式___________ ;由此可知,在碱性条件下 的氧化性
的氧化性___________ (填“>”、“=”或“<”) 。
。

【资料】向胶体中加入电解质后,胶体因失去稳定性使分散质粒子聚集而产生沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
(1)K2FeO4中铁元素的化合价为
(2)过程①中活性菌表现了
(3)根据上述原理,K2FeO4作水处理剂时,其主要作用有
(4)可用次氯酸钾在碱性条件下与氢氧化铁反应得到K2FeO4,写出制备K2FeO4的离子方程式
 的氧化性
的氧化性 。
。
您最近一年使用:0次
【推荐3】过氧化氢(H2O2,氧显-1价)俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。

根据下列反应回答问题:
A.Ag2O+H2O2=2Ag+O2↑+H2O
B.2H2O2=2H2O+O2↑
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2分别表现_______ 性质。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序____ 。
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为____ 。


根据下列反应回答问题:
A.Ag2O+H2O2=2Ag+O2↑+H2O
B.2H2O2=2H2O+O2↑
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2分别表现
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为
您最近一年使用:0次



