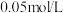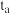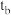某化学兴趣小组进行以下实验探究:
I.设计实验探究反应速率的测定和比较
实验步骤:
取一套装置(装置如图所示),加入40mL1mol•L-1的硫酸,测量收集10mLH2所需的时间。
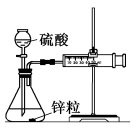
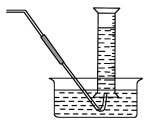
(1)取另一套装置,加入40mL4mol•L-1的硫酸,测量收集10mLH2所需的时间。
实验现象:锌跟硫酸反应产生气泡,收集10mL气体,(2)所用时间比(1)所用时间____ (填“长”或“短”)。
实验结论:4mol•L-1硫酸与锌反应比1mol•L-1硫酸与锌反应速率____ (填“大”或“小”)。
注意事项:①锌粒的颗粒(即表面积)大小_____ 。
②40mL的硫酸要迅速加入。
(2)II.探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
I.设计实验探究反应速率的测定和比较
实验步骤:
取一套装置(装置如图所示),加入40mL1mol•L-1的硫酸,测量收集10mLH2所需的时间。


(1)取另一套装置,加入40mL4mol•L-1的硫酸,测量收集10mLH2所需的时间。
实验现象:锌跟硫酸反应产生气泡,收集10mL气体,(2)所用时间比(1)所用时间
实验结论:4mol•L-1硫酸与锌反应比1mol•L-1硫酸与锌反应速率
注意事项:①锌粒的颗粒(即表面积)大小
②40mL的硫酸要迅速加入。
(2)II.探究用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素,所用HNO3浓度为1.00mol•L-1、2.00mol•L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298K、308K。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T(K) | 大理石规格 | HNO3浓度(mol•L-1) | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (1)实验①和②探究HNO3浓度对该反应速率的影响 (2)实验①和 (3)实验①和 |
| ② | ||||
| ③ | 粗颗粒 | |||
| ④ |
更新时间:2022-09-19 23:13:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某小组拟用含稀硫酸的KMnO4溶液与H2C2O4 (弱酸)溶液的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,设计了下表的实验方案并记录了实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20mol/LH2C2O4溶液、0.010mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
【实验内容及记录】
(1)表格中“乙”需要测的物理量为_______ 。
(2)实验①②探究的是_______ 对化学反应速率的影响。
(3)若②③探究浓度对反应速率的影响,表格中a=_______ ,③中加入amL蒸馏水的目的是_______ 。
(4)实验②④探究的是_______ 对化学反应速率的影响。
(5)实验室有一瓶混有泥沙的草酸样品,利用下列反应的原理来测定其含量。
①配平化学方程式:_______ 。
 ②具体操作为:
②具体操作为:
a.配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。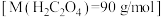
b.滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol/L KMnO4标准溶液装入_______ (填“酸式”或“碱式”)滴定管,进行滴定操作。判断滴定达到终点的现象是_______ 。
c.计算:重复上述操作2次,记录实验数据如下表。此样品的纯度为_______ 。
③误差分析:下列操作会导致测定结果偏高的是_______ 。
A.未用KMnO4标准溶液润洗滴定管 B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 D.观察读数时,滴定前仰视,滴定后俯视
【实验内容及记录】
| 物理量编号 | V(0.20mol/LH2C2O4溶液) | V(蒸馏水)/ | V(0.010mol/L KMnO4溶液)/mL | m( MnSO4固体)/g | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 0 | 25 | |
| ③ | 1.0 | a | 4.0 | 0 | 25 | |
| ④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
(2)实验①②探究的是
(3)若②③探究浓度对反应速率的影响,表格中a=
(4)实验②④探究的是
(5)实验室有一瓶混有泥沙的草酸样品,利用下列反应的原理来测定其含量。
①配平化学方程式:
 ②具体操作为:
②具体操作为:a.配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。
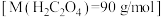
b.滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol/L KMnO4标准溶液装入
c.计算:重复上述操作2次,记录实验数据如下表。此样品的纯度为
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.01 |
| 2 | 1.00 | 20.99 |
| 3 | 0.00 | 21.10 |
A.未用KMnO4标准溶液润洗滴定管 B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 D.观察读数时,滴定前仰视,滴定后俯视
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高锰酸钾是一种重要的化学试剂,利用高锰酸钾完成以下两个实验:
I.探究测定草酸晶体( )中的x值。
)中的x值。
第一步:称取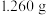 纯草酸晶体,将其制成
纯草酸晶体,将其制成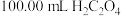 水溶液为待测液。
水溶液为待测液。
第二步:取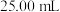 待测液放入锥形瓶中,再加入适量的稀
待测液放入锥形瓶中,再加入适量的稀 。
。
第三步:用浓度 的
的 标准溶液滴定上述溶液,达终点时消耗
标准溶液滴定上述溶液,达终点时消耗 。
。
(1)在第三步中发生离子方程式为:_____________________

请配平上述离子方程式。
(2)①如图可以用于装酸性高锰酸钾标准溶液的是___________ (选“甲、乙”)。
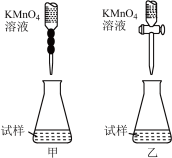
②滴定到达终点的判断标志是____________________________________________ 。
③下列操作可能造成测得x值偏小的是___________ 。
A.滴定终点读数时俯视 B.滴定过程中加入少量蒸馏水冲洗瓶锥形瓶壁
C.没有润洗锥形瓶 D.滴定前有气泡,滴定后气泡消失
④通过上述数据,求得
__________ 。
Ⅱ.探究酸性 和
和 反应的影响因素。当反应开始时,通过压力传感技术收集锥形瓶内压强数据,并绘制出压强一时间曲线如图,
反应的影响因素。当反应开始时,通过压力传感技术收集锥形瓶内压强数据,并绘制出压强一时间曲线如图, 时间段内反应速率变快的因素分析:
时间段内反应速率变快的因素分析:
甲同学:该反应放热,体系温度升高,成为主导影响因素
乙同学:根据自己的解析认为“ 对反应可能起催化剂的作用”,并设计以下实验方案进行验证:
对反应可能起催化剂的作用”,并设计以下实验方案进行验证:
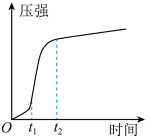
(3)根据实验设计,你推测实验②中再向试管中加入的某种固体是___________ 。
(4)若观察到___________ ,则乙同学分析的影响因素是合理的。
I.探究测定草酸晶体(
 )中的x值。
)中的x值。第一步:称取
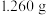 纯草酸晶体,将其制成
纯草酸晶体,将其制成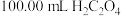 水溶液为待测液。
水溶液为待测液。第二步:取
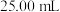 待测液放入锥形瓶中,再加入适量的稀
待测液放入锥形瓶中,再加入适量的稀 。
。第三步:用浓度
 的
的 标准溶液滴定上述溶液,达终点时消耗
标准溶液滴定上述溶液,达终点时消耗 。
。(1)在第三步中发生离子方程式为:

请配平上述离子方程式。
(2)①如图可以用于装酸性高锰酸钾标准溶液的是

②滴定到达终点的判断标志是
③下列操作可能造成测得x值偏小的是
A.滴定终点读数时俯视 B.滴定过程中加入少量蒸馏水冲洗瓶锥形瓶壁
C.没有润洗锥形瓶 D.滴定前有气泡,滴定后气泡消失
④通过上述数据,求得

Ⅱ.探究酸性
 和
和 反应的影响因素。当反应开始时,通过压力传感技术收集锥形瓶内压强数据,并绘制出压强一时间曲线如图,
反应的影响因素。当反应开始时,通过压力传感技术收集锥形瓶内压强数据,并绘制出压强一时间曲线如图, 时间段内反应速率变快的因素分析:
时间段内反应速率变快的因素分析:甲同学:该反应放热,体系温度升高,成为主导影响因素
乙同学:根据自己的解析认为“
 对反应可能起催化剂的作用”,并设计以下实验方案进行验证:
对反应可能起催化剂的作用”,并设计以下实验方案进行验证:
实验编号 | 实验温度/ | 试管中所加试剂及其用量/L | 再向试管中加入某种固体 | 溶液褪至无色所需时间/ | |||
|
|
|
| ||||
① | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 无 |
|
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | ________ |
|
(3)根据实验设计,你推测实验②中再向试管中加入的某种固体是
(4)若观察到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氧化硫是国内外允许使用的一种食品添加剂,可用于食物的增白、防腐等,但必须严格遵守国家有关标准使用。某学习小组设计了如图装置用于制取SO2并验证其性质。

(1)仪器 名称为
名称为_______ 。
(2)若装置 中为品红的乙醇溶液,实验开时后,
中为品红的乙醇溶液,实验开时后, 中无明显现象,装置
中无明显现象,装置 红色褪去,则使品红的水溶液褪色的微粒不是
红色褪去,则使品红的水溶液褪色的微粒不是_______ 。(填化学式)
(3)实验开始后,装置 中反应的离子方程式
中反应的离子方程式_______ 。
(4)实验开始后,发现装置 中的溶液迅速变黄,继续通入
中的溶液迅速变黄,继续通入 ,装置
,装置 中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: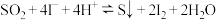 。
。
探究Ⅰ:探究浓度对上述可逆反应的影响
限选试剂: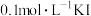 溶液、
溶液、 溶液、
溶液、 溶液、蒸馏水、浓硝酸、浓盐酸(
溶液、蒸馏水、浓硝酸、浓盐酸( 体积已折算为标准状况下体积)。
体积已折算为标准状况下体积)。
探究Ⅱ:探究 在
在 溶液体系中的反应产物
溶液体系中的反应产物
有同学提出上述可逆反应生成的 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。
(5)综上可知, 在
在 溶液中发生了歧化反应,其反应的离子方程式为
溶液中发生了歧化反应,其反应的离子方程式为_______ 。

(1)仪器
 名称为
名称为(2)若装置
 中为品红的乙醇溶液,实验开时后,
中为品红的乙醇溶液,实验开时后, 中无明显现象,装置
中无明显现象,装置 红色褪去,则使品红的水溶液褪色的微粒不是
红色褪去,则使品红的水溶液褪色的微粒不是(3)实验开始后,装置
 中反应的离子方程式
中反应的离子方程式(4)实验开始后,发现装置
 中的溶液迅速变黄,继续通入
中的溶液迅速变黄,继续通入 ,装置
,装置 中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:
中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应: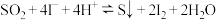 。
。探究Ⅰ:探究浓度对上述可逆反应的影响
限选试剂:
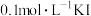 溶液、
溶液、 溶液、
溶液、 溶液、蒸馏水、浓硝酸、浓盐酸(
溶液、蒸馏水、浓硝酸、浓盐酸( 体积已折算为标准状况下体积)。
体积已折算为标准状况下体积)。| 影响因素 | 编号 | 操作 | 现象 |
 | i | 取 ① ① | 溶液变为浅黄色 |
| ii | 取 溶液于锥形瓶中,向其中通入 溶液于锥形瓶中,向其中通入 | 溶液迅速变黄 | |
 | iii | 取 溶液和 溶液和 ② ② | 溶液迅速变黄 |
| iv | 取 溶液和 溶液和 ③ ③ | 溶液迅速变黄,且出现乳黄色浑浊 |
 在
在 溶液体系中的反应产物
溶液体系中的反应产物有同学提出上述可逆反应生成的
 可与
可与 发生反应:
发生反应: 。为进一步探究体系中的产物,完成下列实验方案。
。为进一步探究体系中的产物,完成下列实验方案。| 方案 | 操作 | 预期现象 | 结论 |
| i | 取适量装置 中浊液,向其中滴加几滴④ 中浊液,向其中滴加几滴④ | 无明显变化 | 浊液中无 |
| ii | 将装置 中浊液进行分离 中浊液进行分离 | 得淡黄色固体和澄清溶液 | |
| 取适量分离后的澄清溶液于试管中,⑤ | ⑥ | ⑦ |
 在
在 溶液中发生了歧化反应,其反应的离子方程式为
溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】(一)某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)写出草酸与高锰酸钾反应的离子方程式____________ 。
(2)通过实验A、B,可探究出________ (填外部因素)的改变对化学反应速率的影响,其中V1=_______ 、T1=______ ;通过实验______ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_____ 。
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=____ mol·L-1·min-1。
(二)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2):
(1)上表试管Ⅰ中应添加的试剂为5滴____________ 。
(2)结论是_________ ,实验Ⅲ的目的是__________ 。
| 实验 序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)通过实验A、B,可探究出
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=
(二)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2):
| 试管 | Ⅰ | Ⅱ | Ⅲ |
| 滴加试剂 | 5滴_______ | 5滴0.1mol·L-1CuCl2 | 5滴0.3mol·L-1NaCl |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生小气泡 | 无气泡产生 |
(2)结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验。
【实验原理】
(1)请完成上述实验设计,其中:a=___________ ,b=___________ 。
(2)探究温度对化学反应速率的影响,应选择___________ (填实验编号),实验结论为___________ 。
(3)利用实验①中的数据,计算用KMnO4表示的化学反应速率为___________ (保留两位有效数字)。
(4)该小组同学根据经验绘制了实验②中n(Mn2+)随时间变化的趋势如图甲所示,但查阅资料发现该实验过程中n(Mn2+)随时间变化的实际趋势如图乙所示。

该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验。
I.该小组同学提出的假设是___________ 。
II.若该小组同学提出的假设成立,应观察到的现象是___________ 。
【实验原理】

| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 3mol/L H2SO4溶液 | 0.05mol/L KMnO4溶液 | |||
| ① | 25 | 3.0 | a | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 | b | 2.0 | 3.0 | |
(1)请完成上述实验设计,其中:a=
(2)探究温度对化学反应速率的影响,应选择
(3)利用实验①中的数据,计算用KMnO4表示的化学反应速率为
(4)该小组同学根据经验绘制了实验②中n(Mn2+)随时间变化的趋势如图甲所示,但查阅资料发现该实验过程中n(Mn2+)随时间变化的实际趋势如图乙所示。

该小组同学根据图乙所示信息提出了新的假设,并设计以下实验方案继续进行实验。
| 实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 溶液褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 3mol/L H2SO4溶液 | 0.05mol/L KMnO4溶液 | ||||
| ④ | 25 | 2.0 | 3.0 | 2.0 | 30 | MnSO4 | d |
II.若该小组同学提出的假设成立,应观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
(1)用三支试管各取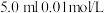 的酸性
的酸性 溶液,再分别滴入
溶液,再分别滴入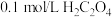 溶液,实验报告如下。
溶液,实验报告如下。
①实验1、3研究的是______ 对反应速率的影响。
②表中
______  。
。
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为 与
与 的
的______ 。
②乙同学认为随着反应的进行,因______ ,故速率加快。
(3)为比较 、
、 对
对 分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:
分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:

①装置乙中仪器A的名称为______ 。
②定性分析如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。但该方案有缺陷,应如何改进:______ 。
③定量分析:如图乙所示,实验时以收集到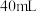 体为准,忽略其他可能影响实验的因素实验中需要测量的数据是
体为准,忽略其他可能影响实验的因素实验中需要测量的数据是______ 。
(1)用三支试管各取
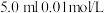 的酸性
的酸性 溶液,再分别滴入
溶液,再分别滴入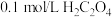 溶液,实验报告如下。
溶液,实验报告如下。| 实验编号 |  酸性 酸性 溶液 溶液 | 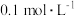  溶液 溶液 | 水 | 反应温度/ | 反应时间/s |
| 1 | 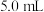 | 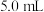 | 0 | 20 | 125 |
| 2 | 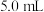 | V | 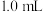 | 20 | 320 |
| 3 | 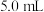 | 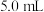 | 0 | 50 | 30 |
②表中

 。
。(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为
 与
与 的
的②乙同学认为随着反应的进行,因
(3)为比较
 、
、 对
对 分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:
分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:
①装置乙中仪器A的名称为
②定性分析如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。但该方案有缺陷,应如何改进:
③定量分析:如图乙所示,实验时以收集到
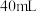 体为准,忽略其他可能影响实验的因素实验中需要测量的数据是
体为准,忽略其他可能影响实验的因素实验中需要测量的数据是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学小组制取氯酸钾并进行有关探究实验。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:
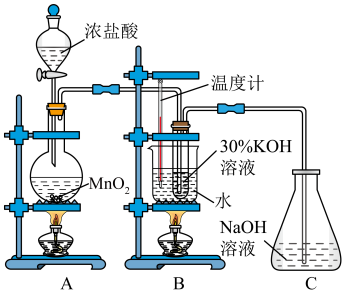
(1)装置C中盛装NaOH溶液仪器的名称是___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)若装置B中加热温度过低,所得主要氧化产物为___________ (填化学式)。已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置B所得溶液中提取氯酸钾晶体的实验操作是___________ 、___________ 、过滤、干燥。

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
①3号试管实验中x的值为___________ ;1号试管实验的作用是___________ 。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为___________ 。
③由该系列实验可得出的结论是___________ 。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:

(1)装置C中盛装NaOH溶液仪器的名称是
(2)装置A中发生反应的化学方程式为
(3)若装置B中加热温度过低,所得主要氧化产物为

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 4.0 | 0 |
| 取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为
③由该系列实验可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】碘酸钙 是无色斜方晶体,可由
是无色斜方晶体,可由 等原料制得。实验室制取
等原料制得。实验室制取 的实验流程如图:
的实验流程如图:

已知:①碘酸是易溶于水、不溶于有机溶剂的强酸;
②碘酸氢钾 与碱中和生成正盐;
与碱中和生成正盐;
③ 是一种难溶于水的白色固体,在碱性条件下不稳定。
是一种难溶于水的白色固体,在碱性条件下不稳定。
制备装置如图:

(1)仪器a的名称为_______ 。
(2)仪器b的作用是_______ 和导出生成的 。
。
(3)该实验中三颈烧瓶适宜的加热方式为_______ 。
(4)为加快三颈烧瓶中的反应速率,可采取的措施是_______ 。
 是无色斜方晶体,可由
是无色斜方晶体,可由 等原料制得。实验室制取
等原料制得。实验室制取 的实验流程如图:
的实验流程如图:
已知:①碘酸是易溶于水、不溶于有机溶剂的强酸;
②碘酸氢钾
 与碱中和生成正盐;
与碱中和生成正盐;③
 是一种难溶于水的白色固体,在碱性条件下不稳定。
是一种难溶于水的白色固体,在碱性条件下不稳定。制备装置如图:

(1)仪器a的名称为
(2)仪器b的作用是
 。
。(3)该实验中三颈烧瓶适宜的加热方式为
(4)为加快三颈烧瓶中的反应速率,可采取的措施是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以黄铜矿(主要成分是 ,含少量
,含少量 )和软锰矿(主要成分是
)和软锰矿(主要成分是 ,含少量
,含少量 )为原料制备纳米材料MnO和
)为原料制备纳米材料MnO和 的工艺如下:
的工艺如下:

已知:MnO易被氧化。
请回答下列问题:
(1)“粉碎过筛”的目的是_______ ;“固体1”的主要成分除S外,还有_______ (填化学式)。
(2)“除杂”时除掉的离子为_______ (填离子符号)。
(3)“沉锰”时生成 的离子方程式为
的离子方程式为_______ 。
(4)在实验室完成“操作A”时,Ar的作用是_______ 。
(5)“蒸氨”时发生的是_______ (填“氧化还原反应”或“非氧化还原反应”);“还原”时,每生成1mol ,消耗
,消耗_______ mol (
( 被氧化为
被氧化为 )。
)。
(6)已知黄铜矿中硫元素的质量分数为a%,杂质中不含硫元素和铜元素。wkg这种黄铜矿经上述转化最终得到bg ,则铜的提取率为
,则铜的提取率为_______ %(填含a、b、w的表达式)。
注: 。
。
 ,含少量
,含少量 )和软锰矿(主要成分是
)和软锰矿(主要成分是 ,含少量
,含少量 )为原料制备纳米材料MnO和
)为原料制备纳米材料MnO和 的工艺如下:
的工艺如下:
已知:MnO易被氧化。
请回答下列问题:
(1)“粉碎过筛”的目的是
(2)“除杂”时除掉的离子为
(3)“沉锰”时生成
 的离子方程式为
的离子方程式为(4)在实验室完成“操作A”时,Ar的作用是
(5)“蒸氨”时发生的是
 ,消耗
,消耗 (
( 被氧化为
被氧化为 )。
)。(6)已知黄铜矿中硫元素的质量分数为a%,杂质中不含硫元素和铜元素。wkg这种黄铜矿经上述转化最终得到bg
 ,则铜的提取率为
,则铜的提取率为注:
 。
。
您最近一年使用:0次

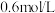

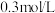 稀
稀