如图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为Cl2、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。

(1)写出有关物质的化学式:B_______ ,F_______ 。
(2)指出MnO2在相关反应中的作用:反应①中是_______ 剂,反应②中是_______ 剂。
(3)若反应①是在加热条件下进行,则A是_______ ;若反应①是在常温条件下进行,则A是_______ 。
(4)写出B与MnO2共热生成D的化学方程式_______ 。
(5)将新制氯水分成两份,向其中一份中滴入NaHCO3溶液,离子方程式是:_______ ,向第二份中滴入紫色石蕊溶液,现象是:_______ ,工业上制取漂白粉的化学方程式是:_______ 。

(1)写出有关物质的化学式:B
(2)指出MnO2在相关反应中的作用:反应①中是
(3)若反应①是在加热条件下进行,则A是
(4)写出B与MnO2共热生成D的化学方程式
(5)将新制氯水分成两份,向其中一份中滴入NaHCO3溶液,离子方程式是:
更新时间:2022-09-25 17:26:36
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。

已知:A、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是____________ ;Y中含有的化学键类型为____________ 。
(2)写出N的化学式__________ ;并任写一种N的主要用途_______________ 。
(3)写出下列反应的离子方程式:
反应①__________________ 。
反应③__________________ 。

已知:A、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是
(2)写出N的化学式
(3)写出下列反应的离子方程式:
反应①
反应③
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】化合物A为一种常见金属元素与一种常见非金属元素组成的化合物,阳离子与阴离子的个数比为2:3。K为常见固态非金属单质,J为常见气态单质。其余为化合物,其中I、F在常温下为液态,C、D为刺激性气体,H无色无味气体,B为白色胶状沉淀,L为氯碱工业中的常见产品。F的浓溶液与K加热可生成D和H。(部分生成物未标出)
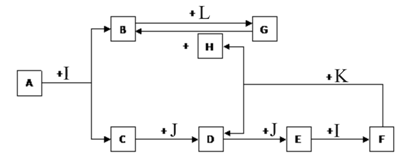
(1)写出下列物质的化学式:E_____________ J_____________
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:_______________________
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式_____________
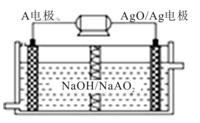
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是_____
A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=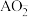 +2H2O
+2H2O
D.正极的电极反应式为:O2+2H2O+4e-=4OH-

(1)写出下列物质的化学式:E
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是

A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=
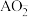 +2H2O
+2H2OD.正极的电极反应式为:O2+2H2O+4e-=4OH-
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】下列物质存在如下图所示的转化关系(反应条件、部分产物未标出),已知某物质X是一种正盐,E是强酸
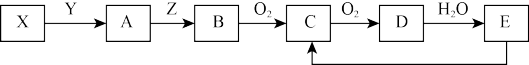
试回答下列问题:
(1)若Y为强酸,且B为黄色固体单质
①从组成物质的元素化合价变化角度预测C可能具有的性质_______________
②一定条件下E转化为C有多种途径,写出其中一种转化的化学反应方程式_______________________ 。
(2)若Y为强碱,且B为空气中含量最高的气态单质
①写出实验室制取A的化学方程式______________________________________ 。
②若A→B的转化常用来检验Z气体管道的是否漏气,用该方法检验的现象是____________________ ,其化学反应方程式_________________________________________ 。
③C、D都是大气污染物,它们对环境造成的危害表现在_______ 。
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.引起水体富营养化
④将x mL C、y mL D混合于同一试管中,将试管倒置于水中,同时通入z mL O2充分反应后,试管内气体全部消失,则x:y:z不可能是_______________
A 1:1:1 B 2:1:1
C 3:7:4 D 1:5:2
(3)无论Y为强酸或强碱均符合上述转化,则物质X的化学式_______________

试回答下列问题:
(1)若Y为强酸,且B为黄色固体单质
①从组成物质的元素化合价变化角度预测C可能具有的性质
②一定条件下E转化为C有多种途径,写出其中一种转化的化学反应方程式
(2)若Y为强碱,且B为空气中含量最高的气态单质
①写出实验室制取A的化学方程式
②若A→B的转化常用来检验Z气体管道的是否漏气,用该方法检验的现象是
③C、D都是大气污染物,它们对环境造成的危害表现在
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.引起水体富营养化
④将x mL C、y mL D混合于同一试管中,将试管倒置于水中,同时通入z mL O2充分反应后,试管内气体全部消失,则x:y:z不可能是
A 1:1:1 B 2:1:1
C 3:7:4 D 1:5:2
(3)无论Y为强酸或强碱均符合上述转化,则物质X的化学式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。

请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是_________ ;乙装置的作用是______ 。
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________ g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示_____________ 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________ mol。

(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:______ 。
 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
请回答下列问题:
(1)①甲装置用于制备氯气,其反应的化学方程式是
②该兴趣小组用100mL 12mol/L盐酸与 8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为下图(不考虑氯气和水的反应)。①图中曲线I表示
②所取石灰乳中含有Ca(OH)2的物质的量为

(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,以下为制备两种消毒剂的方法,请回答下列问题:
(1)实验室沿用舍勒的方法制取 时选用图中装置
时选用图中装置_______ (填“A”或“B”),反应的离子方程式为_______ ,装置B中管f的作用是_______ 。
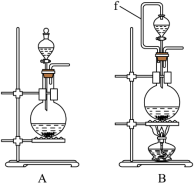
(2)实验室制取干燥、纯净的 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→_______ (填字母)。
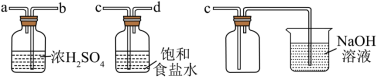
(3)反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
【提出猜想】
猜想1: 降低,氧化剂
降低,氧化剂_______ (填化学式)氧化性减弱。
猜想2:_______ 减弱。
猜想3: 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。
【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
【实验拓展】经过探究,小组同学认为硫酸、 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式:_______ 。
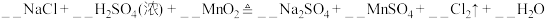
(1)实验室沿用舍勒的方法制取
 时选用图中装置
时选用图中装置
(2)实验室制取干燥、纯净的
 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→
(3)反应停止后,实验小组检验烧瓶中还有
 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。【提出猜想】
猜想1:
 降低,氧化剂
降低,氧化剂猜想2:
猜想3:
 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
| 序号 | 实验操作 | 有、无氯气 | 结论 |
| 1 | 加入浓硫酸,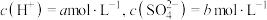 | 有氯气 | 猜想1正确 |
| 2 | 加入氯化钠固体,使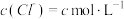 | 有氯气 | 猜想2正确 |
| 3 | 加入浓硫酸和 固体,使 固体,使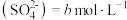 | 猜想3正确 |
 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式: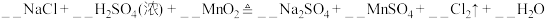
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】硫酰氯(SO2Cl2)和亚硫酰氯(SOCl2)都是重要的化工试剂,均易水解。
(1)甲同学在实验室利用SO2和Cl2在活性炭催化作用下制取SO2Cl2,装置如图所示。

①B装置中冷凝管进水口是___________ (填“m”或“n”)。B中干燥管盛有的物质是___________ 。
②欲制取少量SO2Cl2,选择上图装置(可重复选用),其连接顺序为:a、___________ 、h(用小写字母表示)。
③去除C装置会降低SO2和Cl2的利用率,可能的原因是___________ 。(用化学方程式表示)
(2)SOCl2水解后无残留物,较SO2Cl2是更好的脱水剂。乙同学设计实验利用SOCl2和ZnCl2·xH2O制取无水ZnCl2。
①解释SOCl2在该实验中的作用是___________ 。
②实验室常用NaOH溶液吸收SOCl2,该反应的离子方程式是___________ 。
(3)乙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丙同学认为该实验可能发生副反应使产品不纯。
两同学设计如下实验判断副反应的可能性:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水溶解,将溶液平分至五支试管,分别进行以下实验,其中能得出合理结论的是___________ 。
A.加入过量稀HNO3,再滴加几滴AgNO3溶液
B.加入少量稀HNO3,再滴加几滴BaCl2溶液
C.滴加几滴BaCl2溶液
D.滴加几滴酸性KMnO4溶液
E.滴加几滴KSCN溶液后,再滴加几滴氯水
(1)甲同学在实验室利用SO2和Cl2在活性炭催化作用下制取SO2Cl2,装置如图所示。

①B装置中冷凝管进水口是
②欲制取少量SO2Cl2,选择上图装置(可重复选用),其连接顺序为:a、
③去除C装置会降低SO2和Cl2的利用率,可能的原因是
(2)SOCl2水解后无残留物,较SO2Cl2是更好的脱水剂。乙同学设计实验利用SOCl2和ZnCl2·xH2O制取无水ZnCl2。
①解释SOCl2在该实验中的作用是
②实验室常用NaOH溶液吸收SOCl2,该反应的离子方程式是
(3)乙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丙同学认为该实验可能发生副反应使产品不纯。
两同学设计如下实验判断副反应的可能性:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水溶解,将溶液平分至五支试管,分别进行以下实验,其中能得出合理结论的是
A.加入过量稀HNO3,再滴加几滴AgNO3溶液
B.加入少量稀HNO3,再滴加几滴BaCl2溶液
C.滴加几滴BaCl2溶液
D.滴加几滴酸性KMnO4溶液
E.滴加几滴KSCN溶液后,再滴加几滴氯水
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】某小组同学在实验室制备、收集氯气,并进行一系列的探究,请回答下列问题。
(1)制备 。写出装置I中发生的离子反应方程式
。写出装置I中发生的离子反应方程式_______ 。
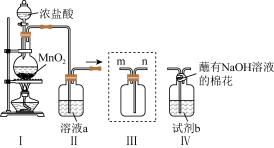
(2)氯水相关性质探究。
①若装置IV中试剂b为 ,将IV接在II之后制得氯水,则II中的溶液a为
,将IV接在II之后制得氯水,则II中的溶液a为_______ 。
②若装置IV中试剂b为 ,可制得
,可制得 的
的 溶液(
溶液( 可溶于
可溶于 溶液,且不与
溶液,且不与 反应)。用此溶液来探究氯水中是哪一种粒子有漂白性,则溶液a为
反应)。用此溶液来探究氯水中是哪一种粒子有漂白性,则溶液a为_______ 。II和IV之间接III,此时气体应该从_______ 口进入III,III的作用是_______ 。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明氯水中有漂白性的是HClO。
溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明氯水中有漂白性的是HClO。
③验证氢水中HClO光照分解的产物。将装置IV广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。
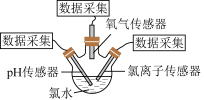
若能够证明氯水中HClO在光照下发生了分解反应,则图中纵坐标可以表示的物理量是_______ (填字母)。
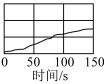
a.氯水的pH b.氢离子的浓度 c.氯离子的浓度
d.氧气的体积分数 e.溶液的颜色 f.导电性
④在氯水中加入少量的 ,黄绿色逐渐变浅。请写出总反应的离子方程式
,黄绿色逐渐变浅。请写出总反应的离子方程式_______ 。
(3)实验后发现I中有大量的固体剩余,在I中溶液中加入Zn,有大量气泡生成。通过此实验可判断
____ (填“是”或“不是”)碱性氧化物。请写出 与FeO在硫酸溶液中反应的离子方程式
与FeO在硫酸溶液中反应的离子方程式_______ 。
(1)制备
 。写出装置I中发生的离子反应方程式
。写出装置I中发生的离子反应方程式
(2)氯水相关性质探究。
①若装置IV中试剂b为
 ,将IV接在II之后制得氯水,则II中的溶液a为
,将IV接在II之后制得氯水,则II中的溶液a为②若装置IV中试剂b为
 ,可制得
,可制得 的
的 溶液(
溶液( 可溶于
可溶于 溶液,且不与
溶液,且不与 反应)。用此溶液来探究氯水中是哪一种粒子有漂白性,则溶液a为
反应)。用此溶液来探究氯水中是哪一种粒子有漂白性,则溶液a为 的
的 溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明氯水中有漂白性的是HClO。
溶液,分别滴在三张红色纸条上,可观察到只有滴加新制氯水的红色纸条褪色,证明氯水中有漂白性的是HClO。③验证氢水中HClO光照分解的产物。将装置IV广口瓶中的氯水转移至三颈瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈瓶中(如图),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

若能够证明氯水中HClO在光照下发生了分解反应,则图中纵坐标可以表示的物理量是

a.氯水的pH b.氢离子的浓度 c.氯离子的浓度
d.氧气的体积分数 e.溶液的颜色 f.导电性
④在氯水中加入少量的
 ,黄绿色逐渐变浅。请写出总反应的离子方程式
,黄绿色逐渐变浅。请写出总反应的离子方程式(3)实验后发现I中有大量的固体剩余,在I中溶液中加入Zn,有大量气泡生成。通过此实验可判断

 与FeO在硫酸溶液中反应的离子方程式
与FeO在硫酸溶液中反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知下列反应,(反应所需的其他条件和各物质的化学计量数均已略去):
① A+B
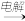 M+D+E; ② M+E®A+F+B
M+D+E; ② M+E®A+F+B
请针对以下两种不同情况回答:
(1)若A是一种钠盐,反应①是化学工业上制取单质E和化合物M的重要方法。则A的电子式为____________ ;反应②的离子方程式为________________________ ;在酸性条件下,若将化合物F加到Fe2+的溶液中,溶液从浅绿色变成黄色,反应的离子方程式为________________________ 。
(2)若A是一种含氧酸盐,可用于实验室中检验水的存在。1个A的酸根离子中共含有50个电子,其中含有一种元素X,X的原子的最外层电子数是电子层数的2倍,则X在元素周期表中的位置是________ 周期____ 族。X单质的熔点是112.8°C,则X单质的晶体类型属于____________ 晶体。X与碳单质在一定条件下可以生成CX2的化合物,其分子结构类似于CO2,则CX2属于_________ 分子(填“极性”或“非极性”)。反应②的化学方程式为:___________________________ ;
① A+B

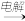 M+D+E; ② M+E®A+F+B
M+D+E; ② M+E®A+F+B请针对以下两种不同情况回答:
(1)若A是一种钠盐,反应①是化学工业上制取单质E和化合物M的重要方法。则A的电子式为
(2)若A是一种含氧酸盐,可用于实验室中检验水的存在。1个A的酸根离子中共含有50个电子,其中含有一种元素X,X的原子的最外层电子数是电子层数的2倍,则X在元素周期表中的位置是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】甲、乙两个研究性学习小组探究氯水的性质 ,甲组同学在一次实验中发现:把新制氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时溶液的红色突然消失。
(1)将氯气通入水中发生反应的离子方程式为_______ 。
(2)探究“溶液的红色突然消失”的原因:
①猜想 a:是氯水中的盐酸和次氯酸中和了 NaOH,使酚酞由红色变成无色; b:是_______ 。
②设计实验:往已褪色的溶液中连续滴加 NaOH 溶液至过量,若现象为_______ ,则证明“猜想 a”正确;若现象为_______ ,则证明“猜想 b”正确。
乙组同学设计了三组实验进行探究
(3)证明氯水中含有 Cl-的是实验_______ (填序号)
(4)实验①中溶液变红是由于溶液中含有_______ (填微粒符号,下同);
(5)同学们根据“H2O2 在催化剂作用下可发生分解”的性质,认为实验③中现象不能说明 Cl2 将 H2O2 氧化,为证实 Cl2 将 H2O2 氧化,可继续补充实验:_______ (填操作、现象)。
(1)将氯气通入水中发生反应的离子方程式为
(2)探究“溶液的红色突然消失”的原因:
①猜想 a:是氯水中的盐酸和次氯酸中和了 NaOH,使酚酞由红色变成无色; b:是
②设计实验:往已褪色的溶液中连续滴加 NaOH 溶液至过量,若现象为
乙组同学设计了三组实验进行探究
| 实验① | 实验② | 实验③ | |
| 实验操作 (试管中溶液均为 1 mL,均滴入 5 滴氯水) |  |  |  |
| 实验现象 | 石蕊溶液先变红,后褪色 | 产生白色沉淀 | 产生大量无色气泡 |
(4)实验①中溶液变红是由于溶液中含有
(5)同学们根据“H2O2 在催化剂作用下可发生分解”的性质,认为实验③中现象不能说明 Cl2 将 H2O2 氧化,为证实 Cl2 将 H2O2 氧化,可继续补充实验:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】乳酸亚铁晶体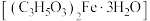 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
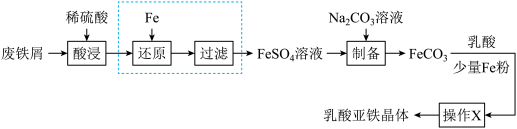
(1)“酸浸”时, 单质发生反应的离子方程式有
单质发生反应的离子方程式有___________ 。
(2)向酸浸液中滴加___________ (填化学式)溶液可判断是否要进行“还原”、“过滤”操作;在实验室中进行过滤操作需要的玻璃仪器有___________ 。
(3)制备过程中将 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。
①该反应的离子方程式为___________ 。
②若 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是___________ (用化学方程式表示)。
(4) 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是___________ 。
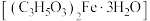 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
(1)“酸浸”时,
 单质发生反应的离子方程式有
单质发生反应的离子方程式有(2)向酸浸液中滴加
(3)制备过程中将
 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。①该反应的离子方程式为
②若
 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是(4)
 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】硝酸铝是一种常见常见媒染剂。工业上用含铝废料(主要含Al、Al2O3、Fe3O4、SiO2等)制取硝酸铝晶体[Al(NO3)3·9H2O]及铝单质的流程如下:
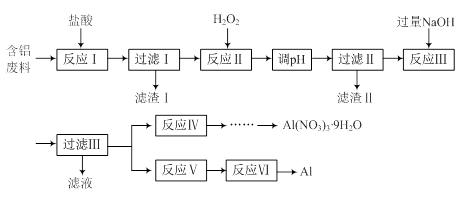
(1)写出反应Ⅰ中Fe3O4参加反应的离子方程式:_____ 。
(2)写出反应Ⅱ的离子方程式:_____ 。
(3)该流程中有一处设计不合理,请指出并加以改正:_____ 。
(4)写出反应Ⅵ的化学方程式:_____ 。

(1)写出反应Ⅰ中Fe3O4参加反应的离子方程式:
(2)写出反应Ⅱ的离子方程式:
(3)该流程中有一处设计不合理,请指出并加以改正:
(4)写出反应Ⅵ的化学方程式:
您最近一年使用:0次
【推荐3】磷酸铁被广泛用于作电极材料,以下为制备磷酸铁的工艺流程图,回答问题:

(1)氧化槽中发生反应的离子方程式为_______ 。
(2)过滤器采用真空状态的优点为:_______ 。
(3)洗涤槽中热水主要是洗涤磷酸铁表面残留的_______ (填写离子符号),检验磷酸铁是否洗涤干净的实验操作:_______ 。
(4)为研究 溶液与金属反应,某同学设计如下实验流程图,并记录相关现象
溶液与金属反应,某同学设计如下实验流程图,并记录相关现象

实验1中生成红褐色沉淀和气体的化学方程式是_______ 。
实验2的现象红色褪去,该同学提出猜想:
①氯水与 反应,使生成硫氰合铁的络合反应逆向进行。
反应,使生成硫氰合铁的络合反应逆向进行。
②你还可能提出的猜想是(结合化学平衡原理答题):_______ 。
该同学预设计如下实验流程图来验证猜想,其中A是_______ ;B是_______ (填写化学式)。


(1)氧化槽中发生反应的离子方程式为
(2)过滤器采用真空状态的优点为:
(3)洗涤槽中热水主要是洗涤磷酸铁表面残留的
(4)为研究
 溶液与金属反应,某同学设计如下实验流程图,并记录相关现象
溶液与金属反应,某同学设计如下实验流程图,并记录相关现象
实验1中生成红褐色沉淀和气体的化学方程式是
实验2的现象红色褪去,该同学提出猜想:
①氯水与
 反应,使生成硫氰合铁的络合反应逆向进行。
反应,使生成硫氰合铁的络合反应逆向进行。②你还可能提出的猜想是(结合化学平衡原理答题):
该同学预设计如下实验流程图来验证猜想,其中A是

您最近一年使用:0次



