阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______ kg。
(5)高铁酸钠 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
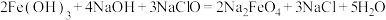
①该反应中氧化剂是_____ (用化学式表示,下同),____ 元素被氧化,还原产物为____ 。
②用双线桥法在方程式中标出电子转移的情况:_____ 。
(6)将 与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目
与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目____ 。
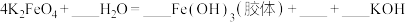
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气  通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用 胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5mg  ,即可达到卫生标准 ,即可达到卫生标准…… |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为(5)高铁酸钠
 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: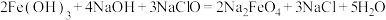
①该反应中氧化剂是
②用双线桥法在方程式中标出电子转移的情况:
(6)将
 与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目
与水反应的化学方程式补充完整并用双线桥表示出电子转移的方向和数目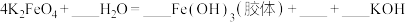
更新时间:2022-10-11 23:17:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】碘是人体不可缺少的元素,为了防止碘缺乏病,人们食用加碘盐。加碘盐就是在精盐中添加一定量的KIO3。某研究性学习小组利用下列反应原理检验某加碘盐中是否含碘:KIO3+KI+H2SO4—→K2SO4+I2+H2O。
(1)配平上述化学方程式并用双线桥表示反应中的电子转移情况。____________ 当有0.1 mol KIO3参加反应时,转移电子的数目为_________ 。
(2)向KI-H2SO4溶液中加入适量碘盐,充分振荡,将生成的碘单质与K2SO4溶液分离,实验操作方法是_________ ,主要仪器名称是_________ ,所需试剂是______ (填序号)。
A.酒精B.氯化钡溶液C.四氯化碳D.淀粉溶液
(3)通过上述实验,判断食盐中含碘的证据是__________________ 。
(1)配平上述化学方程式并用双线桥表示反应中的电子转移情况。
(2)向KI-H2SO4溶液中加入适量碘盐,充分振荡,将生成的碘单质与K2SO4溶液分离,实验操作方法是
A.酒精B.氯化钡溶液C.四氯化碳D.淀粉溶液
(3)通过上述实验,判断食盐中含碘的证据是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】1828年,德国化学家维勒在制备无机盐氰酸铵( )时得到尿素
)时得到尿素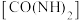 。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
(1)将上述元素按原子半径由小到大的顺序排列________ 。(用元素符号表示)
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式________ 。
(3) 性质与
性质与 相似,也可与硫酸反应生成
相似,也可与硫酸反应生成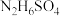 ,则
,则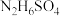 中存在的作用力为
中存在的作用力为________ ,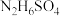 与强碱溶液反应的离子方程式为
与强碱溶液反应的离子方程式为________
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( )。
)。
①写出反应的化学方程式,并用单线桥标出电子转移方向与数目________ 。
②还原产物是________ ,若反应中有 个电子发生转移,参与反应的氨的质量为
个电子发生转移,参与反应的氨的质量为________ g。
 )时得到尿素
)时得到尿素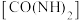 。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:(1)将上述元素按原子半径由小到大的顺序排列
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式
(3)
 性质与
性质与 相似,也可与硫酸反应生成
相似,也可与硫酸反应生成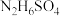 ,则
,则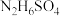 中存在的作用力为
中存在的作用力为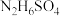 与强碱溶液反应的离子方程式为
与强碱溶液反应的离子方程式为(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 )。
)。①写出反应的化学方程式,并用单线桥标出电子转移方向与数目
②还原产物是
 个电子发生转移,参与反应的氨的质量为
个电子发生转移,参与反应的氨的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】研究氮的循环和转化对生产、生活有重要的价值。
Ⅰ.氨是重要的化工原料。
(1)写出实验室制氨气的化学方程式_______ 。
(2)某工厂用氨制硝酸的流程如下图所示:

①上述转化中,属于氮的固定的是_______ (填“i”“ii”或“iii”)。
②“合成塔”中发生反应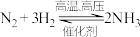 。已知断裂1mol相应化学键需要的能量如下:
。已知断裂1mol相应化学键需要的能量如下:
若反应生成2mol ,可
,可_______ (填“吸收”或“放出”)热量_______ kJ。
③写出“吸收塔”中反应的化学方程式 、
、_______ 。
④“吸收塔”排出的尾气中含有NO、 等氮氧化物,可用
等氮氧化物,可用 将其催化还原成不污染环境的气体,写出
将其催化还原成不污染环境的气体,写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
II.含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下图:

(3)过程Ⅲ发生反应的化学方程式为_______ 。
(4)根据图1和图2,判断使用亚硝化菌的最佳条件为_______ 。
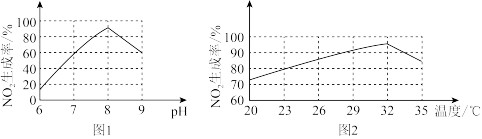
Ⅰ.氨是重要的化工原料。
(1)写出实验室制氨气的化学方程式
(2)某工厂用氨制硝酸的流程如下图所示:

①上述转化中,属于氮的固定的是
②“合成塔”中发生反应
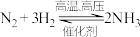 。已知断裂1mol相应化学键需要的能量如下:
。已知断裂1mol相应化学键需要的能量如下:| 化学键 | H—H | N—H |  |
| 能量 | 436kJ | 391kJ | 946kJ |
若反应生成2mol
 ,可
,可③写出“吸收塔”中反应的化学方程式
 、
、④“吸收塔”排出的尾气中含有NO、
 等氮氧化物,可用
等氮氧化物,可用 将其催化还原成不污染环境的气体,写出
将其催化还原成不污染环境的气体,写出 与
与 反应的化学方程式
反应的化学方程式II.含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下图:

(3)过程Ⅲ发生反应的化学方程式为
(4)根据图1和图2,判断使用亚硝化菌的最佳条件为
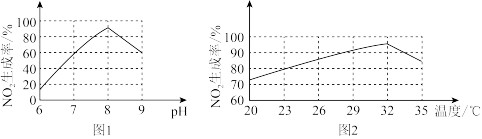
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列方程式的书写
(1) 溶液显碱性的离子方程式
溶液显碱性的离子方程式_______
(2)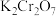 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式_______
(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式_______
(4)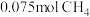 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(1)
 溶液显碱性的离子方程式
溶液显碱性的离子方程式(2)
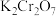 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式
(4)
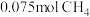 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氰化物电镀的废液中含多种金属离子与氰离子(CN-)的络离子,如Cu(CN) 。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
(1)氰离子和次氯酸根的反应可按氰离子中的氮呈负氧化态(负价),碳呈正氧化态(正价)进行_______ 。
□CN-+□ClO-+□OH-=□+□+□+□H2O
(2)_______
□Cu(CN) +□ClO-+□OH-=□+□+□+□+□
+□ClO-+□OH-=□+□+□+□+□
在本反应中的得失电子数相等,是_______ 个电子?
 。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:(1)氰离子和次氯酸根的反应可按氰离子中的氮呈负氧化态(负价),碳呈正氧化态(正价)进行
□CN-+□ClO-+□OH-=□+□+□+□H2O
(2)
□Cu(CN)
 +□ClO-+□OH-=□+□+□+□+□
+□ClO-+□OH-=□+□+□+□+□在本反应中的得失电子数相等,是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】(1)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有______ 性。(填氧化性或还原性)
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3 CO2↑。该反应的氧化剂是____ ,当16g 硫参加反应时,转移的电子数为__________ 。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。上述反应中,若有10个铝原子参与反应,则转移的电子数为__________ 个,用“双线桥法”标明反应中电子转移的方向和数目_________ 。
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3 CO2↑。该反应的氧化剂是
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。上述反应中,若有10个铝原子参与反应,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:________________ 。若有0.75mol 电子转移,则被还原的氧化剂粒子数为_______ 。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl 的是______ (填序号)。
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN 溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______________ 。
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl 的是
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN 溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】目前新能源技术被不断利用,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___________ 。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:
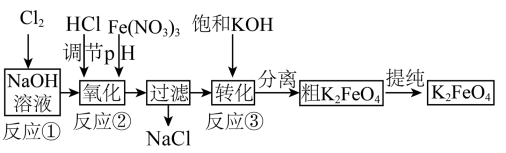
①写出反应①的离子方程式___________ 。
②请写出生产流程中“转化”(反应③)的化学方程式___________ 。
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)___________ Ksp(Na2FeO4)(填“>”“<”或“=”)。
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___________ 溶液。
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是___________ 。
(4) 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
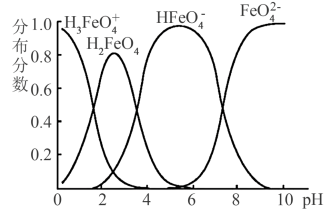
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO 的分布分数的变化情况是
的分布分数的变化情况是___________ 。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___________ 转化为___________ 。(填化学式)
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:

①写出反应①的离子方程式
②请写出生产流程中“转化”(反应③)的化学方程式
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4
 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是(4)
 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
 的分布分数的变化情况是
的分布分数的变化情况是②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列物质的化学式 :
硝酸钡___________ ;硫酸铝___________ ;硫酸钠___________ ;氢氧化铜___________ ;碳酸钙___________ ;氯化铵___________ 。
硝酸钡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅氟酸(化学式为H2SiF6)是一种强酸,其中Si的化合价为_______ ,其电离方程式为_______ 。
您最近一年使用:0次
【推荐3】氧化还原反应原理在研究物质性质及方面具有重要价值。
(1)化合价是学习氧化还原反应的基础。在括号中写出以下几种物质中加点元素的化合价。
NaC lO_______ ;H2O 2_______ ;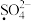
_______ ;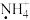
_______ ;
(2)废水脱氮工艺中有一种方法是在废水中加入过量NaClO使 完全转化为
完全转化为 该反应可表示为:
该反应可表示为: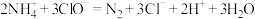 。
。
①该反应中氧化剂是_______ (离子符号表示)。
②反应中被氧化的离子与被还原的离子的数目之比为_______ 。
③反应中每生成1个 分子,转移
分子,转移_______ 个电子。
(1)化合价是学习氧化还原反应的基础。在括号中写出以下几种物质中加点元素的化合价。
Na
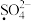
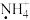
(2)废水脱氮工艺中有一种方法是在废水中加入过量NaClO使
 完全转化为
完全转化为 该反应可表示为:
该反应可表示为: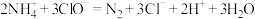 。
。①该反应中氧化剂是
②反应中被氧化的离子与被还原的离子的数目之比为
③反应中每生成1个
 分子,转移
分子,转移
您最近一年使用:0次



