I.智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为: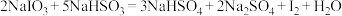
(1)反应中_______ 元素被氧化,_______ 是氧化剂。
(2)用单线桥标出电子转移方向和数目_______ 。
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为_______ 。
II.有一种“地康法”制取氯气的反应原理如图所示:
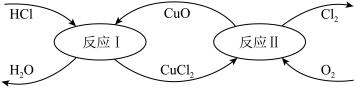
(4)反应I的离子方程式为_______ 。
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种: 、
、 、
、 、
、 、NaI、HI。已知该反应中
、NaI、HI。已知该反应中 只发生了如下过程:
只发生了如下过程: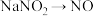 ;写出该反应的化学方程式
;写出该反应的化学方程式_______ 。
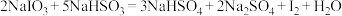
(1)反应中
(2)用单线桥标出电子转移方向和数目
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为
II.有一种“地康法”制取氯气的反应原理如图所示:

(4)反应I的离子方程式为
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种:
 、
、 、
、 、
、 、NaI、HI。已知该反应中
、NaI、HI。已知该反应中 只发生了如下过程:
只发生了如下过程: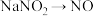 ;写出该反应的化学方程式
;写出该反应的化学方程式
更新时间:2022-10-12 15:51:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请写出下列反应的离子方程式:
(1)H2SO4和活泼金属(如Fe):____ 。
(2)H2SO4和金属氧化物(如MgO):____ 。
(3)H2SO4和碱[如Mg(OH)2]:____ 。
(4)H2SO4和盐(如Na2CO3):____ 。
(1)H2SO4和活泼金属(如Fe):
(2)H2SO4和金属氧化物(如MgO):
(3)H2SO4和碱[如Mg(OH)2]:
(4)H2SO4和盐(如Na2CO3):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂成)制备ZnSO4·7H2O的流程如图。
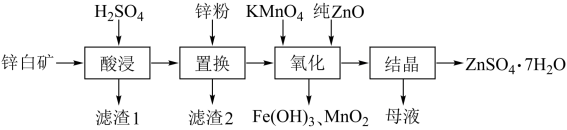
“氧化”一步中,发生反应的离子方程式为___ 。

“氧化”一步中,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海水是一个巨大的化学资源宝库。回答下列问题:
(1)海水提溴工艺中,发生反应: ,该反应中氧化剂是
,该反应中氧化剂是__________ ,它在反应中__________ (填“得到”或“失去”)电子;现有 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是_________  。
。
(2)利用化学沉淀法可以去除粗盐中的杂质离子( 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为__________ ,滴加 溶液略微过量的目的是
溶液略微过量的目的是__________ 。
(3)在常温下,将氯气通入 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为__________ ,该漂白液的有效成分是__________ (填名称)。
(1)海水提溴工艺中,发生反应:
 ,该反应中氧化剂是
,该反应中氧化剂是 标准状况下的
标准状况下的 参加该反应,则理论上可转化
参加该反应,则理论上可转化 的物质的量是
的物质的量是 。
。(2)利用化学沉淀法可以去除粗盐中的杂质离子(
 等)。向某粗盐水滴加过量
等)。向某粗盐水滴加过量 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 溶液略微过量的目的是
溶液略微过量的目的是(3)在常温下,将氯气通入
 溶液中,可以得到一种漂白液,上述反应的化学方程式为
溶液中,可以得到一种漂白液,上述反应的化学方程式为
您最近一年使用:0次
【推荐1】消毒剂在生活中应用广泛,Na2FeO4、Cl2、ClO2、H2O2、NaClO是生活中不同领域的消毒剂。根据下列反应回答问题
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.16HCl+2KMnO4=5Cl2↑+2MnCl2+2KCl+8H2O
C.2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O
D.2KClO3+4HCl=2ClO2↑+2KCl+Cl2↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是___________ (填序号)。

(2)反应A中,氧化产物与还原产物的质量之比为___________ ;。
(3)用双线桥表示反应C电子转移的方向和数目:___________
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、 、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。反应后溶液的酸性
、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。反应后溶液的酸性___________ (填“增强”或“减弱”)。
A.2H2O2
 2H2O+O2↑
2H2O+O2↑B.16HCl+2KMnO4=5Cl2↑+2MnCl2+2KCl+8H2O
C.2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O
D.2KClO3+4HCl=2ClO2↑+2KCl+Cl2↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是

(2)反应A中,氧化产物与还原产物的质量之比为
(3)用双线桥表示反应C电子转移的方向和数目:
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、
 、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。反应后溶液的酸性
、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。反应后溶液的酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,_____ 是氧化剂,______ 是还原剂;_____ 是还原产物,_______ 是氧化产物。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中均有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦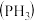 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:___________ 。
(2)羟基磷灰石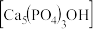 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
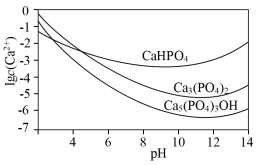
①图中所示3种钙盐,其中在人体中最稳定的存在形式是___________ (填化学式)。
②实验室制备羟基磷灰石时,应将___________ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到___________ 中。
(3)氮的氧化物对大气污染比较严重,一定条件下可用 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式:___________ ,该反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为___________ ,每消耗1mol ,同时转移
,同时转移___________ mol电子。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦
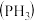 ,写出磷化铝与水反应的化学方程式:
,写出磷化铝与水反应的化学方程式:(2)羟基磷灰石
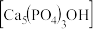 是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
(3)氮的氧化物对大气污染比较严重,一定条件下可用
 消除污染,请写出
消除污染,请写出 与
与 反应的化学方程式:
反应的化学方程式: ,同时转移
,同时转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某化学小组利用如图装置完成系列实验。完成下列填空:
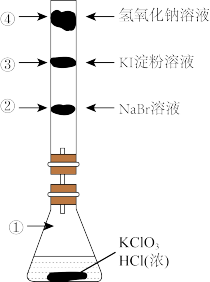
(1)锥形瓶①中利用 与浓盐酸制备氯气。写出化学方程式,并用单线桥法标出电子的转移方向和数目
与浓盐酸制备氯气。写出化学方程式,并用单线桥法标出电子的转移方向和数目_______ 。
_______=_______KCl+_______
锥形瓶中可以观察到_______ 的现象。
(2)一段时间后,棉花团②的颜色变为橙色,反应的化学方程式为: 。该反应的氧化产物是
。该反应的氧化产物是_______ 。(填化学式)
(3)棉花团③的现象是_______ 。
(4)本实验所涉及的物质中,还原性比 强的微粒是
强的微粒是_______ (填化学式)。推测 与
与 反应的可能性,解释原因:
反应的可能性,解释原因:_______ 。将KI浓溶液与 混合,未发生反应,分析可能的原因:
混合,未发生反应,分析可能的原因:_______ 。

(1)锥形瓶①中利用
 与浓盐酸制备氯气。写出化学方程式,并用单线桥法标出电子的转移方向和数目
与浓盐酸制备氯气。写出化学方程式,并用单线桥法标出电子的转移方向和数目_______=_______KCl+_______
锥形瓶中可以观察到
(2)一段时间后,棉花团②的颜色变为橙色,反应的化学方程式为:
 。该反应的氧化产物是
。该反应的氧化产物是(3)棉花团③的现象是
(4)本实验所涉及的物质中,还原性比
 强的微粒是
强的微粒是 与
与 反应的可能性,解释原因:
反应的可能性,解释原因: 混合,未发生反应,分析可能的原因:
混合,未发生反应,分析可能的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】建筑工地常用的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
(1)配平上述化学方程式,并用双线桥表示电子转移情况____ 。
(2)上述反应的氧化剂是____ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
(4)某厂废液中,含有2%~5%的 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为______ 。
(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为______ 。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O(1)配平上述化学方程式,并用双线桥表示电子转移情况
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别
 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。| A.③⑤ | B.②④ | C.②⑤ | D.①②③⑤ |
 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)实验室制取氯气反应的化学方程式为:_________ ;
①在该反应中,氧化剂与还原剂的物质的量之比是_________ ;
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是________ NA。
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目_________ ;
②浓盐酸在该反应中表现的性质是__________ (填序号) ;
;
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是___________ (填化学式);
④上述反应产生0.1molCl2时,转移电子的物质的量为___________ 。
①在该反应中,氧化剂与还原剂的物质的量之比是
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目
②浓盐酸在该反应中表现的性质是
 ;
;A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是
④上述反应产生0.1molCl2时,转移电子的物质的量为
您最近一年使用:0次
【推荐1】据所学知识填空:
(1)在下列反应中,HCl做还原剂的是___________ ,HCl做氧化剂的是__________ 。
①CaCO3+2HCl=CaCl2+CO2↑+H2O
②Fe+2HCl=FeCl2+H2↑
③PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O
④KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
⑤CuO+2HCl=CuCl2+H2O
(2)在横线上补充所需的离子或分子,并配平方程式__________ 。
________Mn2++______ +_____H2O=______MnO2↓+_______Cl2↑+________
+_____H2O=______MnO2↓+_______Cl2↑+________
(3)用双线桥表示下列反应中电子转移方向和数目:__________ 。
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(4)已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,该反应中还原剂是_______ ;若收集到lmol的CO2时,消耗氧化剂________ mol,有________ mol电子发生转移。
(5)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO—、OH—、 、Cl—、H2O,写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl—、H2O,写出碱性条件下制高铁酸钾的离子反应方程式:_________________ 。
(1)在下列反应中,HCl做还原剂的是
①CaCO3+2HCl=CaCl2+CO2↑+H2O
②Fe+2HCl=FeCl2+H2↑
③PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O
④KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
⑤CuO+2HCl=CuCl2+H2O
(2)在横线上补充所需的离子或分子,并配平方程式
________Mn2++______
 +_____H2O=______MnO2↓+_______Cl2↑+________
+_____H2O=______MnO2↓+_______Cl2↑+________(3)用双线桥表示下列反应中电子转移方向和数目:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(4)已知:2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,该反应中还原剂是
(5)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO—、OH—、
 、Cl—、H2O,写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl—、H2O,写出碱性条件下制高铁酸钾的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
I.根据反应8NH3+3Cl2=6NH4Cl+N2,当有34gNH3参加反应时,被氧化的物质的质量为__ g,生成的还原产物的质量为__ g。
II.(1)在反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中,用氧化还原反应的知识分析:__ 是氧化剂,__ 是还原剂,氧化剂与还原剂个数之比为__ ,用“双线桥法”表示反应中电子转移的方向和数目:___ 。
(2)写出该反应的离子方程式:___ 。
III.由Mn2+、Bi3+、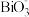 、
、 、H+、H2O组成的一个氧化还原系统中,发生BiO
、H+、H2O组成的一个氧化还原系统中,发生BiO →Bi3+的反应过程,该反应配平后正确的离子方程式为
→Bi3+的反应过程,该反应配平后正确的离子方程式为___ 。
I.根据反应8NH3+3Cl2=6NH4Cl+N2,当有34gNH3参加反应时,被氧化的物质的质量为
II.(1)在反应:K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中,用氧化还原反应的知识分析:
(2)写出该反应的离子方程式:
III.由Mn2+、Bi3+、
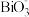 、
、 、H+、H2O组成的一个氧化还原系统中,发生BiO
、H+、H2O组成的一个氧化还原系统中,发生BiO →Bi3+的反应过程,该反应配平后正确的离子方程式为
→Bi3+的反应过程,该反应配平后正确的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】含氮化合物(NOx、NO 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。___________ 。用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程式为___________ 。
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图:___________ 。酸化废水与铁粉反应的离子方程式是___________ 。
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是___________ 。
 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
已知:3Fe2++ +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。
(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、___________ 。
(5)加入稀硫酸的作用是___________ 。
(6)水样中NO 的含量为
的含量为___________ mol·L-1(用含c1、c2、V1、V2、V的代数式表示)。
 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。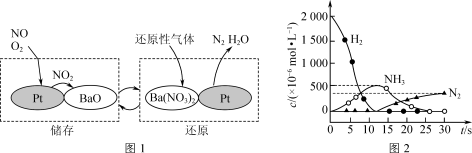
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图: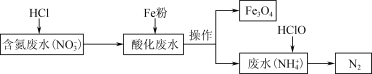
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除
 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。已知:3Fe2++
 +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、
(5)加入稀硫酸的作用是
(6)水样中NO
 的含量为
的含量为
您最近一年使用:0次



