回答下列问题
(1)按如图所示操作,充分反应后:
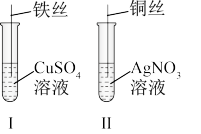
①Ⅰ中发生反应的离子方程式为_______ ;
②Ⅱ中铜丝上观察到的现象是_______ ;
③结合Ⅰ、Ⅱ实验现象可知 、
、 、
、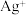 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、 、
、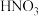 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是_______ ;若反应方程式中转移了0.3mol电子,则氧化产物的质量是_______ 。
(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:_____
_______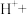 _______
_______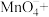 _______
_______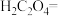 _______
_______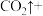 _______
_______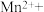 _______
_______
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到的现象是
③结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、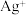 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)某一反应体系中有反应物和生成物共5种物质:S、
 、
、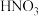 、NO、
、NO、 。该反应物中还原产物是
。该反应物中还原产物是(3)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:
_______
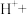 _______
_______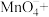 _______
_______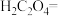 _______
_______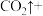 _______
_______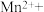 _______
_______
更新时间:2022-10-15 00:00:04
|
相似题推荐
【推荐1】(1)按如图所示操作,充分反应后:
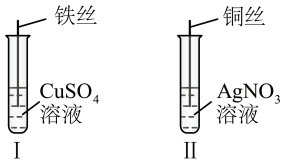
①Ⅱ中发生反应的离子方程式为________ ;
②结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______ 。
(2)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中氧化性强弱顺序为__________ ,盐酸所起的作用是________ ,当有10个Cl2生成时,有______ 个还原剂被氧化。
(3)反应2H2O+Cl2+SO2=H2SO4+2HCl中还原性强弱顺序为_______ 。并用双线桥法标出该反应中电子转移________ 。

①Ⅱ中发生反应的离子方程式为
②结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中氧化性强弱顺序为
(3)反应2H2O+Cl2+SO2=H2SO4+2HCl中还原性强弱顺序为
您最近一年使用:0次
【推荐2】从化合价的角度认识氯的化合物。
(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂是___ ,氧化产物是___ ,氧化剂和还原剂的物质的量之比为__ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___ Cl2(填>、<或=)。
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是___ (填字母序号)。
a.FeSO4 b.O3 c.KMnO4 d.SO2
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如图:

请将流程中发生的两个反应的离子方程式补充完整:
反应①: ClO
ClO +
+ SO2=
SO2= SO
SO +
+
___
反应②: ClO2+
ClO2+ H2O2+
H2O2+ =
= ClO
ClO +
+ O2↑+
O2↑+ H2O
H2O___
(1)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中,氧化剂是
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中,可将ClO
),需将其转化为Cl-除去,下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.FeSO4 b.O3 c.KMnO4 d.SO2
(2)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。Mathieson方法制备亚氯酸钠的流程如图:

请将流程中发生的两个反应的离子方程式补充完整:
反应①:
 ClO
ClO +
+ SO2=
SO2= SO
SO +
+
反应②:
 ClO2+
ClO2+ H2O2+
H2O2+ =
= ClO
ClO +
+ O2↑+
O2↑+ H2O
H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识回答下列问题:
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取 H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为_______ 。
②有同学认为 2
2 3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:
3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:_______ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中)
对人类健康会产生危害,为了降低饮用水中) 的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下
的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下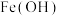 2还原
2还原 生成
生成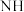 3,反应中氧化剂和还原剂物质的量之比为
3,反应中氧化剂和还原剂物质的量之比为_______ ;方案二,在碱性条件下,用铝粉处理,已知反应时Al与 为5∶3,且Al转化为
为5∶3,且Al转化为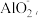 被氧化的元素是
被氧化的元素是_______ ,还原产物是_______ ,请写出反应的离子方程式:_______ 。
(3)已知 3+可以氧化
3+可以氧化 2,则向
2,则向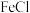 3和
3和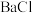 2中通入
2中通入 2会产生白色沉淀,该沉淀是
2会产生白色沉淀,该沉淀是_______ (填化学式)。
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取
 H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
H2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为②有同学认为
 2
2 3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:
3也有还原性,可以选择其作为试剂验证) H2O2氧化性。该观点是否可行,说明理由:(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中)
对人类健康会产生危害,为了降低饮用水中) 的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下
的浓度,某饮用水研究人员提出两种处理方案:方案一,碱性条件下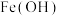 2还原
2还原 生成
生成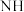 3,反应中氧化剂和还原剂物质的量之比为
3,反应中氧化剂和还原剂物质的量之比为 为5∶3,且Al转化为
为5∶3,且Al转化为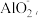 被氧化的元素是
被氧化的元素是(3)已知
 3+可以氧化
3+可以氧化 2,则向
2,则向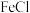 3和
3和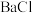 2中通入
2中通入 2会产生白色沉淀,该沉淀是
2会产生白色沉淀,该沉淀是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③Cu ④蔗糖 ⑤NH3 ⑥KNO3溶液 ⑦CO2 ⑧熔融的KCl ⑨石墨。填空回答(填序号):以上物质中能导电的是______________ ;属于电解质的是__________ ;属于非电解质的是______________ ;
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O_______
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________ 。
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是_______ ;既有氧化性又有还原性的是_______ 。
(2)在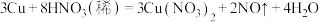 反应中:
反应中:
①_______ 是还原剂,_______ 是还原产物。(填写化学式)
②用单线桥法标出该反应电子转移的方向和数目:_______
③反应中稀硝酸表现出的性质是_______ 。(填写字母)
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。
①该反应中,发生还原反应的过程是_______ →_______ 。
②写出该反应的化学方程式:_______ 。
(1)在
 、
、 、
、 、
、 、S微粒中只有氧化性的是
、S微粒中只有氧化性的是(2)在
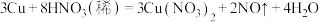 反应中:
反应中:①
②用单线桥法标出该反应电子转移的方向和数目:
③反应中稀硝酸表现出的性质是
a.还原性 b.酸性 c.氧化性。
(3)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 ;已知该反应中
;已知该反应中 只发生如下过程:
只发生如下过程: 。
。①该反应中,发生还原反应的过程是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空
(1)铁屑加入硝酸银溶液中反应的离子方程式为___________________________ 。
(2)醋酸(CH3COOH)与烧碱溶液反应的离子方程式为________________________ 。
(3)NaHSO4是一种____________ (填“酸、碱、盐”),用电离方程式解释该物质水溶液呈酸性的原因:___________________________________ 。
(4)配平下列方程式:______ SO +
+____ IO +
+_______ H+=______ SO +
+______ I2+ ____ H2O。
(5)一定条件下,RO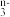 和氟气可发生如下反应:RO
和氟气可发生如下反应:RO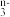 +F2+2OH-=RO
+F2+2OH-=RO +2F-+H2O,从而可知在RO
+2F-+H2O,从而可知在RO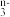 中,元素R的化合价是
中,元素R的化合价是 ___________ 。
(1)铁屑加入硝酸银溶液中反应的离子方程式为
(2)醋酸(CH3COOH)与烧碱溶液反应的离子方程式为
(3)NaHSO4是一种
(4)配平下列方程式:
 +
+ +
+ +
+(5)一定条件下,RO
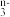 和氟气可发生如下反应:RO
和氟气可发生如下反应:RO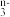 +F2+2OH-=RO
+F2+2OH-=RO +2F-+H2O,从而可知在RO
+2F-+H2O,从而可知在RO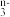 中,元素R的化合价是
中,元素R的化合价是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】把 通入浓氨水中,发生如下反应:
通入浓氨水中,发生如下反应: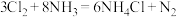
(1)用双线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的 与
与 的分子数之比为:
的分子数之比为:_______ 。
(3)若反应中有 克氨发生氧化反应,则反应中有生成氮气的质量为
克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠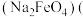 铁为
铁为 价
价 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: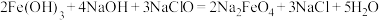
_________ 元素被氧化,还原产物为_________ 。
 通入浓氨水中,发生如下反应:
通入浓氨水中,发生如下反应: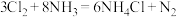
(1)用双线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的
 与
与 的分子数之比为:
的分子数之比为:(3)若反应中有
 克氨发生氧化反应,则反应中有生成氮气的质量为
克氨发生氧化反应,则反应中有生成氮气的质量为(4)高铁酸钠
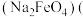 铁为
铁为 价
价 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取: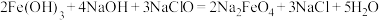
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有下列三个在溶液中发生的氧化还原反应:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(1)Fe2+、I-、Cl-、Cr3+的还原性由强到弱依次是___________ 。
(2)③反应中HCl的作用_____ ;氧化剂和起还原剂作用的HCl的数目之比_____
(3)向FeI2溶液中通入少量Cl2反应的离子方程式为___________ 。
(4)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O 还原成Cr3+,反应的离子方程式为
还原成Cr3+,反应的离子方程式为___________ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(1)Fe2+、I-、Cl-、Cr3+的还原性由强到弱依次是
(2)③反应中HCl的作用
(3)向FeI2溶液中通入少量Cl2反应的离子方程式为
(4)+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O
 还原成Cr3+,反应的离子方程式为
还原成Cr3+,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知反应:①SO2+H2O=H2SO3;②2SO2+O2=2SO3;③SO2+2H2S=3S↓+2H2O。
(1)上述反应中不属于氧化还原反应的是_____ ;SO2做还原剂的是_____ ,SO2做氧化剂的是______ 。
(2)反应③中,参与反应的氧化剂与还原剂的质量比是______ 。
(3)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现__________ 性。
(1)上述反应中不属于氧化还原反应的是
(2)反应③中,参与反应的氧化剂与还原剂的质量比是
(3)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现
您最近一年使用:0次



