下列关于化学反应速率的说法中,正确的是
①用铁片与稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
③决定化学反应速率的主要因素是反应物的浓度
④汽车尾气中的NO与CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦使用催化剂,使反应的活化能降低,反应速率加快
⑧光是影响某些化学反应速率的外界条件之一
⑨增加反应物的用量,一定会增大化学反应速率
①用铁片与稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
③决定化学反应速率的主要因素是反应物的浓度
④汽车尾气中的NO与CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦使用催化剂,使反应的活化能降低,反应速率加快
⑧光是影响某些化学反应速率的外界条件之一
⑨增加反应物的用量,一定会增大化学反应速率
| A.①②⑤⑨ | B.④⑥⑦⑧ | C.④⑥⑦⑨ | D.③④⑥⑦ |
更新时间:2022-10-30 16:12:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验或措施、现象、结论均正确的是
| 实验或措施 | 现象 | 结论 | |
| A | 将纯水加热到95℃ | pH<7 | 加热可导致水呈酸性 |
| B | 用4mL0.01mol·L-1的H2C2O4分别与2mL0.1mol·L-1的酸性KMnO4溶液和2mL0.2mol·L-1的酸性KMnO4溶液反应 | 0.2mol·L-1的酸性KMnO4溶液褪色快 | 研究浓度对反应速率的影响 |
| C | 将石蜡油分解产生的气体通入溴的CCl4溶液中 | 溶液褪色 | 产生的气体是乙烯 |
| D | 向1mL0.1mol·L-1MgCl2溶液中滴加1~2滴NaOH溶液,再滴加2滴0.1mol·L-1FeCl3溶液 | 先产生白色沉淀,后沉淀变为红褐色 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列四种酸溶液,均能跟锌片反应,其中最初反应速率最快的是( )
| A.10℃20mL3mol/L的盐酸溶液 | B.20℃30mL3mol/L的盐酸溶液 |
| C.20℃20mL4mol/L的醋酸溶液 | D.20℃10mL2mol/L的硫酸溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在反应: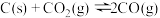 中,可使反应速率增大的措施是
中,可使反应速率增大的措施是
①压缩体积以增大压强②升高温度③体积不变,通入 ④增加碳的量⑤移出
④增加碳的量⑤移出 ⑥体积不变,通入
⑥体积不变,通入 ⑦恒温恒压,通入
⑦恒温恒压,通入
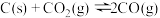 中,可使反应速率增大的措施是
中,可使反应速率增大的措施是①压缩体积以增大压强②升高温度③体积不变,通入
 ④增加碳的量⑤移出
④增加碳的量⑤移出 ⑥体积不变,通入
⑥体积不变,通入 ⑦恒温恒压,通入
⑦恒温恒压,通入
| A.①②④⑥ | B.①②③⑤⑦ | C.①②⑥ | D.①②③④⑥ |
您最近一年使用:0次
【推荐2】下列有关说法正确的是( )
| A.Hg(l)+H2SO4(aq)===HgSO4(aq)+H2(g)常温下不能自发进行,说明ΔH<0 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
| C.锌与稀硫酸反应时加入少量硫酸铜,反应加快的原因是Cu2+水解增大了H+浓度 |
| D.对于N2(g)+3H2(g)⇌2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应速率增大、逆反应速率减小,平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列措施一定能加快所对应反应的反应速率的是
| 选项 | 反应 | 措施 |
| A |  稀硫酸与锌反应 稀硫酸与锌反应 | 再加入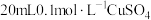 溶液 溶液 |
| B | 常温下,铁片与 硫酸反应 硫酸反应 | 将反应体系温度升高5℃ |
| C | 大理石与 盐酸反应 盐酸反应 | 将 盐酸换成 盐酸换成 硫酸 硫酸 |
| D |  溶液与 溶液与 盐酸反应 盐酸反应 | 再加入一定量 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:反应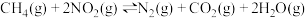 的正反应是放热反应。下列关于该反应的说法正确的是
的正反应是放热反应。下列关于该反应的说法正确的是
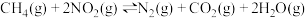 的正反应是放热反应。下列关于该反应的说法正确的是
的正反应是放热反应。下列关于该反应的说法正确的是A. 的能量一定高于 的能量一定高于 的 的 |
| B.升高温度,正反应速率加快,逆反应速率减慢 |
| C.当反应达到平衡时,正反应速率、逆反应速率均为0 |
D.单位时间内,若消耗 的同时生成 的同时生成 ,则化学反应达到平衡状态 ,则化学反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
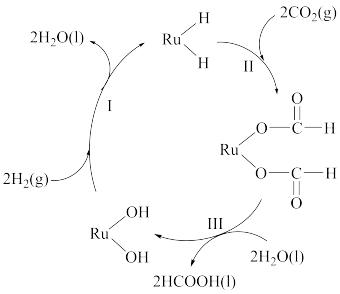
【推荐1】 的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将
的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将 转化为有机原料甲酸的反应机理如图所示。下列说法错误的是
转化为有机原料甲酸的反应机理如图所示。下列说法错误的是
 的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将
的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将 转化为有机原料甲酸的反应机理如图所示。下列说法错误的是
转化为有机原料甲酸的反应机理如图所示。下列说法错误的是
| A.已知反应Ⅱ为决速步骤,则反应Ⅱ的活化能最高 |
| B.催化剂不能改变该反应的反应热 |
C.该反应的总方程式为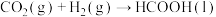 |
| D.反应过程中既有极性键的生成,又有非极性键的生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列事实与括号中物质的性质对应关系不正确的是
| A.将鲜花至于装满氯气的集气瓶中褪色(氯气具有漂白性) |
| B.蔗糖遇浓硫酸会变黑膨胀(浓硫酸有强氧化性和脱水性) |
| C.双氧水中加入FeCl3溶液有气体快速放出(Fe3+能催化H2O2分解) |
| D.葡萄糖与银氨溶液共热,有银镜现象(葡萄糖有还原性) |
您最近一年使用:0次

 的盐酸和醋酸反应,测得容器内压强随时间的变化曲线如下图。下列说法
的盐酸和醋酸反应,测得容器内压强随时间的变化曲线如下图。下列说法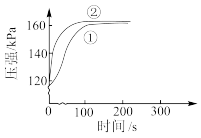
 溶液完全中和上述两种酸溶液,盐酸消耗NaOH溶液的体积更大
溶液完全中和上述两种酸溶液,盐酸消耗NaOH溶液的体积更大 2N2(g)+CO2(g)+2H2O(l)△H<0,进行过程中CH4的转化率随时间变化的关系。若要改变起始条件,使反应过程按曲线b进行,可采取的措施是
2N2(g)+CO2(g)+2H2O(l)△H<0,进行过程中CH4的转化率随时间变化的关系。若要改变起始条件,使反应过程按曲线b进行,可采取的措施是
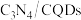 ),能利用太阳光高效分解水,原理如图所示。下列说法不正确的是
),能利用太阳光高效分解水,原理如图所示。下列说法不正确的是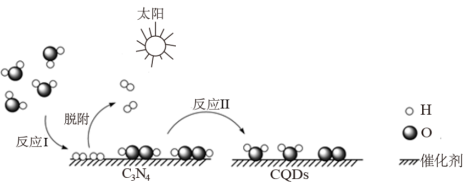
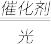 2H2O+O2↑
2H2O+O2↑

