下列实验或措施、现象、结论均正确的是
| 实验或措施 | 现象 | 结论 | |
| A | 将纯水加热到95℃ | pH<7 | 加热可导致水呈酸性 |
| B | 用4mL0.01mol·L-1的H2C2O4分别与2mL0.1mol·L-1的酸性KMnO4溶液和2mL0.2mol·L-1的酸性KMnO4溶液反应 | 0.2mol·L-1的酸性KMnO4溶液褪色快 | 研究浓度对反应速率的影响 |
| C | 将石蜡油分解产生的气体通入溴的CCl4溶液中 | 溶液褪色 | 产生的气体是乙烯 |
| D | 向1mL0.1mol·L-1MgCl2溶液中滴加1~2滴NaOH溶液,再滴加2滴0.1mol·L-1FeCl3溶液 | 先产生白色沉淀,后沉淀变为红褐色 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
更新时间:2022-05-25 20:18:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列措施可加快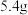 铝粉与
铝粉与 稀硫酸反应速率,同时又不影响生成
稀硫酸反应速率,同时又不影响生成 的量的是
的量的是
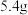 铝粉与
铝粉与 稀硫酸反应速率,同时又不影响生成
稀硫酸反应速率,同时又不影响生成 的量的是
的量的是A.加入少量 粉末 粉末 | B.适当升高反应温度 |
| C.将稀硫酸换成等物质的量的浓硫酸 | D.将铝粉换成等质量的铝片 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列装置或操作能达到实验目的的是


| A.甲:定量测定化学反应速率 |
| B.乙:制作简单燃料电池 |
| C.丙:探究浓度对化学反应速率的影响 |
D.丁:开关由N改置于M时, 合金的腐蚀速率减小 合金的腐蚀速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向25mL0.1mol·L-1某二元弱酸H2R溶液中加入NaOH固体或通入HCl。已知:HR-的电离平衡常数(Ka=10-n)大于水解平衡常数。下列有关叙述正确的是
| A.在加入NaOH固体或通入HCl的过程中,水的电离程度均一直减小 |
| B.pH=7时,c(HR-)+c(R2-)+c(OH-)=c(H+)+c(Na+) |
| C.在NaHR溶液中,有关微粒浓度大小关系为c(HR-)>c(H2R)>c(R2-) |
| D.加入NaOH固体至pH=n,此时存在c(H+)+c(Na+)=c(OH-)+3c(HR-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.10 的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示,下列说法正确的是
的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示,下列说法正确的是
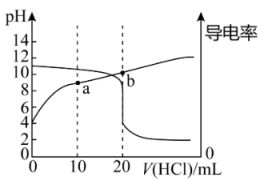
 的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示,下列说法正确的是
的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示,下列说法正确的是
A.BOH的Kb约为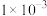 |
B.a点溶液中: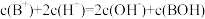 |
| C.水的电离程度:a>b |
| D.滴定至pH=7时,加入的V(HCl)为20mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用下列装置和试剂进行实验,设计合理且能达到实验目的的是


| A.图I:制备无水AlCl3固体 |
| B.图Ⅱ:检验NaCl中是否含有KCl |
| C.图Ⅲ:制取并收集NH3 |
| D.图Ⅳ:验证Ksp(Ag2SO4)>Ksp(Ag2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列化学用语对现象变化的解释不准确的是
A.“NO2球”浸泡在热水中,颜色加深: △H<0 △H<0 |
| B.用石墨电极电解CuSO4溶液,阴极附近溶液蓝色变浅:Cu2++2e-=Cu |
C.向FeSO4溶液中加入Br2水,溶液变为黄色: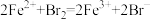 |
D.向Mg(OH)2悬浊液中滴加FeCl3溶液出现红褐色沉淀:3Mg(OH)2(s)+2Fe3+ 2Fe (OH)3(s)+3Mg2+ 2Fe (OH)3(s)+3Mg2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A.分馏石油气和裂解气可用溴水进行鉴别 |
| B.异丁烷的二氯取代物有3种(不考虑立体异构) |
| C.主链含四个碳的烷烃中,碳原子个数是最多的是2,3﹣四甲基丁烷 |
| D.乙醇和甘油都含羟基,葡萄糖和蔗糖都是糖类,但它们之间不是同系物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组变化中,前者是物理变化,后者是化学变化的是
| A.碘的升华、石油的分馏 |
| B.用NH₄Cl溶液(显酸性) 除铁锈、食盐水导电 |
| C.蛋白质溶液中加饱和(NH₄)₂SO₄溶液、蓝色的胆矾常温下变白 |
| D.煤的干馏、石油的裂化 |
您最近一年使用:0次

 溶液
溶液 固体是否变质
固体是否变质 反应,记录出现浑浊的时间
反应,记录出现浑浊的时间 的存在
的存在 为
为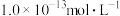 ,下列有关该溶液的叙述正确的是(
,下列有关该溶液的叙述正确的是(
 不可能为
不可能为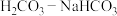 缓冲体系起到稳定血液pH的作用
缓冲体系起到稳定血液pH的作用

