氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______(选填编号)。
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关系”可用下图表示。
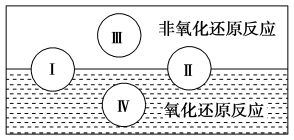
试写出有水参加且符合反应类型IV的一个化学方程式:_______ 。
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2。
①配平下列化学方程式并单线桥标明电子转移的方向和数目: _______ NaIO3+_______NaHSO3→_______
___
②该反应中,若生成1个还原产物则转移电子数目为___ 个。
(4)已知: 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
____ I-(填“>”或“<”)。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_______(选填编号)。
| A.高炉炼铁 | B.食物腐败变质 | C.高温煅烧石灰石 | D.燃放烟花爆竹 |

试写出有水参加且符合反应类型IV的一个化学方程式:
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2。
①配平下列化学方程式并单线桥标明电子转移的方向和数目: _______ NaIO3+_______NaHSO3→_______

②该反应中,若生成1个还原产物则转移电子数目为
(4)已知:
 、I2、I-、
、I2、I-、 和一些未知物组成的一个氧化还原反应,其中
和一些未知物组成的一个氧化还原反应,其中 是氧化产物,该反应中还原性
是氧化产物,该反应中还原性
更新时间:2022-11-08 08:30:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I、地球上的金属矿物资源是有限的,应合理开发利用。
铜在自然界存在于多种矿石中,如:
(1)若 中Cu为+1价、Fe为+3价,高温焙烧时发生的反应是
中Cu为+1价、Fe为+3价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有___________ 。
(2)工业上以辉铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为: ,该反应中氧化剂是
,该反应中氧化剂是___________ ;
(3)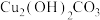 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
II. 是一种常用的氧化剂,工业上用途广泛
是一种常用的氧化剂,工业上用途广泛
(4)工业上可以用浓氨水检验输送氯气的管道是否泄漏,原理为
①该反应中氧化剂与还原剂的分子个数比为___________
②请用单线桥标出该反应中电子转移的方向和数目___________
(5) 与浓盐酸在一定温度下反应会生成氯气和黄绿色的易爆物质
与浓盐酸在一定温度下反应会生成氯气和黄绿色的易爆物质 ,化学方程式:
,化学方程式:
① 。
。___________
②浓盐酸在反应中显示出来的性质是___________ (填写编号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③若产生7.1g ,则生成
,则生成 的质量为
的质量为___________ g。
铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 |  |  | 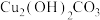 |
 中Cu为+1价、Fe为+3价,高温焙烧时发生的反应是
中Cu为+1价、Fe为+3价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有(2)工业上以辉铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:
 ,该反应中氧化剂是
,该反应中氧化剂是(3)
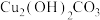 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为II.
 是一种常用的氧化剂,工业上用途广泛
是一种常用的氧化剂,工业上用途广泛(4)工业上可以用浓氨水检验输送氯气的管道是否泄漏,原理为

①该反应中氧化剂与还原剂的分子个数比为
②请用单线桥标出该反应中电子转移的方向和数目
(5)
 与浓盐酸在一定温度下反应会生成氯气和黄绿色的易爆物质
与浓盐酸在一定温度下反应会生成氯气和黄绿色的易爆物质 ,化学方程式:
,化学方程式:①
 。
。②浓盐酸在反应中显示出来的性质是
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③若产生7.1g
 ,则生成
,则生成 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为抗击新冠肺炎经常对环境进行消毒,常用药物如:高锰酸钾、漂白粉、氯气等。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________ (填化学符号,下同);过一会儿,溶液颜色逐渐褪去,起作用的微粒是___________ 。
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为___________ (填化学式)。向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式___________ 。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为: (浓)
(浓)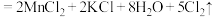 ,回答下列问题:
,回答下列问题:
①用双线桥标出电子转移的方向和数目___________
 (浓)
(浓)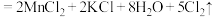
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:
___________ 
___________  (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。
③反应中氯化氢表现出的性质是___________ 。(填写字母)
a.还原性 b.酸性 c.氧化性
④若生成标准状况下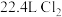 ,则转移电子总数是
,则转移电子总数是___________ 。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:
 (浓)
(浓)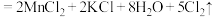 ,回答下列问题:
,回答下列问题:①用双线桥标出电子转移的方向和数目
 (浓)
(浓)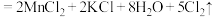
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:


 (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。③反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
④若生成标准状况下
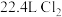 ,则转移电子总数是
,则转移电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1828年,德国化学家维勒在制备无机盐氰酸铵(NH4OCN)时得到尿素[CO(NH2)2]。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
(1)将上述元素按原子半径由小到大的顺序排列_______ 。(用元素符号表示)
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式_______ ,其中N元素的化合价为_______ 。
(3)N2H4性质与NH3相似,也可与硫酸反应生成N2H6SO4,则N2H6SO4中存在的作用力为_______ ,N2H6SO4与强碱溶液反应的离子方程式为_______ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2)。
①写出反应的化学方程式,并标出电子转移方向与数目_______ 。
②被氧化的元素是_______ ,还原产物是_______ ,若反应中有3NA个电子发生转移,参与反应的氨的质量为_______ g。
(1)将上述元素按原子半径由小到大的顺序排列
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式
(3)N2H4性质与NH3相似,也可与硫酸反应生成N2H6SO4,则N2H6SO4中存在的作用力为
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2)。
①写出反应的化学方程式,并标出电子转移方向与数目
②被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】能将KI氧化为I2的若干种氧化剂有H2O2、Cl2、KIO3、HNO3,KClO3、KMnO4等。
(1)上述试剂最适合贴上的一个标签是___ (填序号)。
(2)配平方程式:KClO3+KI+H2SO4=K2SO4+KCl+I2+H2O,___ 。已知过量KClO3会引起副反应:KClO3+I2→KIO3+Cl2,据此判断:KClO3和KIO3相比,氧化性较强的是___ 。
(3)写出KI溶液与Cl2反应的离子方程式___ 。
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-=I +2H2O
+2H2O___ 。
(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
请判断,等物质的量的四种氧化剂分别与足量KI作用,得到I2最多的是___ 。
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入___ ;②加入___ 。
(1)上述试剂最适合贴上的一个标签是
A. | B. | C. | D. |
(3)写出KI溶液与Cl2反应的离子方程式
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-=I
 +2H2O
+2H2O(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
| 氧化剂 | KMnO4 | KIO3 | H2O2 | HNO3 |
| 还原产物 | Mn2+ | I2 | H2O | NO |
请判断,等物质的量的四种氧化剂分别与足量KI作用,得到I2最多的是
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入
您最近一年使用:0次
【推荐2】根据①~④四个反应,回答下列问题:
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为___ (填序号)。
A.置换反应 B.复分解反应 C.化合反应 D.氧化还原反应
(2)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为____ 。
(3)亚硝酸钠(NaNO2)有毒,一次摄入量超过3g可导致死亡。
Ⅰ.实验室中,亚硝酸钠也被用于处理过量的叠氮化钠,有关反应方程式如下:
NaNO2+H2SO4=HNO2+NaHSO4 a
2NaN3+2HNO2=3N2↑+2NO↑+2NaOH b
①上述两个反应中属于非氧化还原反应的是___ (选填字母“a”或“b")。
②其中的氧化还原反应的氧化剂是___ (写化学式),该反应的还原产物与氧化产物的质量之比为___ 。
Ⅱ.亚硝酸钠外观与食盐相似,均有咸味。某学校实验探究小组欲对亚硝酸钠与氯化钠进行鉴别,下列是他们的鉴别方法:
将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再加淀粉。如果溶液显蓝色则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可以用下列化学方程式表示:2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O
写出X的化学式并用双线桥法标出电子转移的方向和数目___ ,___ 。
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为
A.置换反应 B.复分解反应 C.化合反应 D.氧化还原反应
(2)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为
(3)亚硝酸钠(NaNO2)有毒,一次摄入量超过3g可导致死亡。
Ⅰ.实验室中,亚硝酸钠也被用于处理过量的叠氮化钠,有关反应方程式如下:
NaNO2+H2SO4=HNO2+NaHSO4 a
2NaN3+2HNO2=3N2↑+2NO↑+2NaOH b
①上述两个反应中属于非氧化还原反应的是
②其中的氧化还原反应的氧化剂是
Ⅱ.亚硝酸钠外观与食盐相似,均有咸味。某学校实验探究小组欲对亚硝酸钠与氯化钠进行鉴别,下列是他们的鉴别方法:
将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再加淀粉。如果溶液显蓝色则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可以用下列化学方程式表示:2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O
写出X的化学式并用双线桥法标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】比较下列各组反应,回答问题:
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则在Cu、Fe、Ag中,___________ 还原性最强;在Cu2+、Fe2+、Ag+中,_________ 氧化性最强。
(2)已知氯气与氯化亚铁溶液反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl−;氯化铁溶液与碘化钾溶液反应的离子方程式是2Fe3++2I−=2Fe2++I2。则Fe3+、Cl2、I2的氧化性由强到弱的顺序是________ ;若将氯气通入物质的量浓度相同的氯化亚铁、碘化钾的混合溶液中,则先被氧化的离子是____________ 。
(3)铁丝可在氯气中燃烧:2Fe+3Cl2 2FeCl3,也可在硫蒸气中燃烧:Fe+S
2FeCl3,也可在硫蒸气中燃烧:Fe+S FeS。由此可推知,氯气的氧化性比硫的氧化性
FeS。由此可推知,氯气的氧化性比硫的氧化性__________ 。
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则在Cu、Fe、Ag中,
(2)已知氯气与氯化亚铁溶液反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl−;氯化铁溶液与碘化钾溶液反应的离子方程式是2Fe3++2I−=2Fe2++I2。则Fe3+、Cl2、I2的氧化性由强到弱的顺序是
(3)铁丝可在氯气中燃烧:2Fe+3Cl2
 2FeCl3,也可在硫蒸气中燃烧:Fe+S
2FeCl3,也可在硫蒸气中燃烧:Fe+S FeS。由此可推知,氯气的氧化性比硫的氧化性
FeS。由此可推知,氯气的氧化性比硫的氧化性
您最近一年使用:0次
【推荐1】根据反应2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl,回答下列问题:
(1)该反应中氧化剂是___ ,盐酸的作用是___ 。
(2)该反应中参加氧化还原 的氧化剂与还原剂的物质的量之比为___ 。
(3)用单线桥法标出电子转移的方向与数目___ 。
(1)该反应中氧化剂是
(2)该反应中参加
(3)用单线桥法标出电子转移的方向与数目
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】化合物KaFeb(C2O4)c·dH2O(其中铁为正三价)是重要的光化学试剂。通过下述实验确定该晶体的组成。
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知:_____ KMnO4+___ H2C2O4+____ H2SO4=____ MnSO4+____ K2SO4+____ CO2+____ H2O
(1) 配平上述反应方程式
(2) 草酸为二元弱酸,其一级电离的方程式为______________________ 。
(3)滴定终点观察到的现象为_____________________________________ 。
(4)通过计算确定样品的组成(写出计算过程)。______________________
步骤a:称取该样品4.91g溶于水中配成250mL溶液,取出25mL溶液,向其中加入过量的NaOH溶液,将沉淀过滤,洗涤,高温灼烧至质量不再改变,称量其固体的质量为0.08g。
步骤b:另取出25mL溶液,加入适量稀H2SO4溶液,用0.050 mol·L-1KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液24.00mL。
已知:
(1) 配平上述反应方程式
(2) 草酸为二元弱酸,其一级电离的方程式为
(3)滴定终点观察到的现象为
(4)通过计算确定样品的组成(写出计算过程)。
您最近一年使用:0次
【推荐3】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的“价—类”二维图:

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
(2)将X的溶液与Y混合反应,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)Z的浓溶液与铜单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为___________ 。
(4) 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是___________ (填字母)。
a. b.
b. c.
c.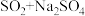 d.
d.
(5)已知 能被
能被 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与 的
的 溶液恰好反应时,X元素在还原产物中的化合价为
溶液恰好反应时,X元素在还原产物中的化合价为___________ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X的溶液与Y混合反应,该反应中氧化剂与还原剂的物质的量之比为
(3)Z的浓溶液与铜单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
(4)
 是重要的化工原料。从氧化还原反应的角度分析,下列制备
是重要的化工原料。从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是a.
 b.
b. c.
c.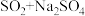 d.
d.
(5)已知
 能被
能被 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与 的
的 溶液恰好反应时,X元素在还原产物中的化合价为
溶液恰好反应时,X元素在还原产物中的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】青铜是人类历史上一项伟大的发明,它是红铜和锡、铅的合金,也是金属冶铸史上最早的合金。铜及其合金在日常生活中应用广泛。回答下列问题:
(1)西汉刘安在《淮南万毕术》中介绍了我国在西汉时期发明的湿法冶金技术,即“曾青得铁则化为铜”,其含义是铜的可溶性化合物的水溶液与铁反应生成铜。例如:将适量的铁粉加入硫酸铜溶液中,发生反应CuSO4+Fe=Cu+FeSO4。
①该反应发生时,溶液的颜色变化为_______ 。
②用双线桥法标出该反应中电子转移的方向和数目:_______ 。
③每生成6.4 g Cu,消耗的CuSO4的质量为_______ g。
(2)工业冶炼铜的原理主要是:
i.2Cu2S+3O2 2Cu2O+2SO2
2Cu2O+2SO2
ii.2Cu2O+Cu2S 6Cu+SO2↑
6Cu+SO2↑
①Cu2S中Cu元素的化合价为_______ 价。
②反应i中,生成的SO2属于_______ (填“氧化”、“还原”或“氧化和还原”)产物,将其通入足量的NaOH溶液中,发生反应的化学方程式为2NaOH+SO2=Na2SO3+H2O,该反应的离子方程式为_______ 。
③将Cu2O固体加入稀HNO3中,发生反应_______Cu2O+_______ HNO3=_______Cu(NO3)2+_______ NO↑+_______H2O,配平该化学方程式_________ 。
(1)西汉刘安在《淮南万毕术》中介绍了我国在西汉时期发明的湿法冶金技术,即“曾青得铁则化为铜”,其含义是铜的可溶性化合物的水溶液与铁反应生成铜。例如:将适量的铁粉加入硫酸铜溶液中,发生反应CuSO4+Fe=Cu+FeSO4。
①该反应发生时,溶液的颜色变化为
②用双线桥法标出该反应中电子转移的方向和数目:
③每生成6.4 g Cu,消耗的CuSO4的质量为
(2)工业冶炼铜的原理主要是:
i.2Cu2S+3O2
 2Cu2O+2SO2
2Cu2O+2SO2ii.2Cu2O+Cu2S
 6Cu+SO2↑
6Cu+SO2↑①Cu2S中Cu元素的化合价为
②反应i中,生成的SO2属于
③将Cu2O固体加入稀HNO3中,发生反应_______Cu2O+_______ HNO3=_______Cu(NO3)2+_______ NO↑+_______H2O,配平该化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铅(Pb)及其化合物广泛用于冶金、蓄电池、印刷、颜料、油漆等领域,常见铅的化合物主要以+2价和+4价的形态存在。经查阅资料:
已知:①Pb与酸反应都得到+2价的化合物。
②PbCl4不稳定,易分解为PbCl2和Cl2。
回答下列问题:
(1)Pb是较活泼金属,但在实验室或化工厂常用Pb作为某些酸(如稀硫酸)的耐酸反应器的衬里和贮存、输送的管道设备。请解释其原因___________ 。
(2)PbSO4可用于制造蓄电池、白色颜料等。写出用钠盐制备PbSO4的化学方程式___________ 。
(3)PbO2在强酸性条件下能与Mn2+反应生成Pb2+和 ,反应的离子方程式为
,反应的离子方程式为 ___________ ,该反应说明PbO2具有 ___________ (填“氧化性”或“还原性”)。
(4)经查阅,PbO2是两性氧化物,设计实验并验证
| 物质 | PbO | PbO2 | PbCl2 | PbCl+4 |
| 在水中的溶解性(常温) | 难溶于水的黄色固体 | 难溶于水的棕黑色固体 | 微溶于水的白色固体 | 易溶于水的黄色油状液体 |
| 物质 | PbSO4 | Pb(NO3)2 | Na2PbO2 | Na2PbO3 |
| 在水中的溶解性(常温) | 难溶于水的白色固体 | 易溶于水形成无色溶液 | 易溶于水形成无色溶液 | 易溶于水形成无色溶液 |
②PbCl4不稳定,易分解为PbCl2和Cl2。
回答下列问题:
(1)Pb是较活泼金属,但在实验室或化工厂常用Pb作为某些酸(如稀硫酸)的耐酸反应器的衬里和贮存、输送的管道设备。请解释其原因
(2)PbSO4可用于制造蓄电池、白色颜料等。写出用钠盐制备PbSO4的化学方程式
(3)PbO2在强酸性条件下能与Mn2+反应生成Pb2+和
 ,反应的离子方程式为
,反应的离子方程式为 (4)经查阅,PbO2是两性氧化物,设计实验并验证
| 实验步骤 | 实验现象 | 反应的化学方程式 |
| ①向盛有PbO2固体的试管中滴加NaOH溶液 | 棕黑色固体逐渐溶解 | |
| ②向盛有PbO2固体的试管中滴加稀盐酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。工业上有多种方法来制备氮化硅,下面是几种常见的方法:
(1)方法一——直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N21300~1400 ℃,Si3N4。
(2)方法二——可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 ℃的加热基板上生成氮化硅膜,其化学方程式为________________________________________________________ 。
(3)方法三——化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和氯化氢,与方法一相比,用此法制得的氮化硅纯度较高,其原因是_______________________ 。
(4)方法四——Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体:________ (填化学式);然后使Si(NH2)4受热分解,分解后的另一种产物的化学式为________ 。
工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(5)写出焦炭与原料B中的主要成分反应的化学方程式:________________________________________________________ 。
(1)方法一——直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N21300~1400 ℃,Si3N4。
(2)方法二——可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 ℃的加热基板上生成氮化硅膜,其化学方程式为
(3)方法三——化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和氯化氢,与方法一相比,用此法制得的氮化硅纯度较高,其原因是
(4)方法四——Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体:
工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(5)写出焦炭与原料B中的主要成分反应的化学方程式:
您最近一年使用:0次



