完成下列问题
(1)四卤化硅( )的沸点和二卤化铅(
)的沸点和二卤化铅( )的熔点如图所示
)的熔点如图所示

① 的沸点依
的沸点依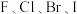 次序升高的原因是
次序升高的原因是_______ 。
②结合 的沸点和
的沸点和 的熔点变化规律,可推断:依
的熔点变化规律,可推断:依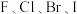 次序,
次序, 晶体中离子键百分数
晶体中离子键百分数_______ (填“增大”、“不变”或“减小”)。
(2)铍及其化合物的应用正日益被重视
①铍与相邻主族的铝元素性质相似。下列有关和铝的叙述正确的有_______ 。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液 均小于7
均小于7
②氯化铍在气态时存在 单分子——a和二聚分子
单分子——a和二聚分子 ——b,固态时则具有如下图所示的链状结构——c
——b,固态时则具有如下图所示的链状结构——c

a属于_______ (填“极性”或“非极性”)分子,二聚分子 中
中 原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为
原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为_______ 。
③ 立方晶胞如下图所示。
立方晶胞如下图所示。

阿伏加德罗常数的数值为 ,若
,若 晶体的密度为
晶体的密度为 ,则
,则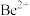 和
和 之间最近的距离为
之间最近的距离为_______  。
。
(1)四卤化硅(
 )的沸点和二卤化铅(
)的沸点和二卤化铅( )的熔点如图所示
)的熔点如图所示
①
 的沸点依
的沸点依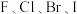 次序升高的原因是
次序升高的原因是②结合
 的沸点和
的沸点和 的熔点变化规律,可推断:依
的熔点变化规律,可推断:依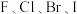 次序,
次序, 晶体中离子键百分数
晶体中离子键百分数(2)铍及其化合物的应用正日益被重视
①铍与相邻主族的铝元素性质相似。下列有关和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液
 均小于7
均小于7②氯化铍在气态时存在
 单分子——a和二聚分子
单分子——a和二聚分子 ——b,固态时则具有如下图所示的链状结构——c
——b,固态时则具有如下图所示的链状结构——c
a属于
 中
中 原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为
原子的杂化方式相同,且所有原子都在同一平面上,b的结构式为③
 立方晶胞如下图所示。
立方晶胞如下图所示。
阿伏加德罗常数的数值为
 ,若
,若 晶体的密度为
晶体的密度为 ,则
,则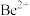 和
和 之间最近的距离为
之间最近的距离为 。
。
22-23高三上·辽宁沈阳·期中 查看更多[2]
更新时间:2022-11-12 08:46:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲: 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
乙: 无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
丙: 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.
请根据上述信息回答下列问题.
(1)B元素在元素周期表中的位置为_____ ,请写出BC2分子的电子式:______ .
(2)A、E、F在同一周期,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:________________________________ .
②F、C两种元素组成的化合物Y可作为耐高温结构的材料,X与Y两种化合物在溶液中发生反应的离子方程式:_________________________________________________ .
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液.滴加过程中的现象为:①试管中溶液变成深棕黄色,②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀.请回答“片刻后反应变得剧烈”的原因
a_____________________ b_________________ .
(4)物质戊的元素组成和乙相同,戊分子具有18电子结构.与乙互为同系物,则戊的氯取代有机物的共________ 种。
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:
 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.乙:
 无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。丙:
 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.请根据上述信息回答下列问题.
(1)B元素在元素周期表中的位置为
(2)A、E、F在同一周期,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:
②F、C两种元素组成的化合物Y可作为耐高温结构的材料,X与Y两种化合物在溶液中发生反应的离子方程式:
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液.滴加过程中的现象为:①试管中溶液变成深棕黄色,②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀.请回答“片刻后反应变得剧烈”的原因
a
(4)物质戊的元素组成和乙相同,戊分子具有18电子结构.与乙互为同系物,则戊的氯取代有机物的共
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】元素周期表和元素周期律是我们高中化学中的重要理论知识,试回答下列问题:
(1)X元素原子的核电荷数为8,其原子核内的质子数为_____ ,该元素原子的二价阴离子中,核外电子数为_____ ,离子结构示意图为______ ,中子数为9的核素表示为______ 。
(2)向 溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl_____ S(填“>”或“<”),反应的离子方程式为___________ 。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
①铷在元素周期表中的位置是___________ 。
②下列关于铷的说法不正确的是___________ (填序号)。
a.与水反应比钠更剧烈 b.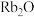 在空气中易吸收水和二氧化碳
在空气中易吸收水和二氧化碳
c.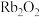 与水能剧烈反应并释放出
与水能剧烈反应并释放出 d.单质具有很强的氧化性
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(4)关于元素周期表、周期律,下列说法正确的是___________(填序号)。
(1)X元素原子的核电荷数为8,其原子核内的质子数为
(2)向
 溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl
溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
①铷在元素周期表中的位置是
②下列关于铷的说法不正确的是
a.与水反应比钠更剧烈 b.
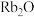 在空气中易吸收水和二氧化碳
在空气中易吸收水和二氧化碳c.
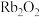 与水能剧烈反应并释放出
与水能剧烈反应并释放出 d.单质具有很强的氧化性
d.单质具有很强的氧化性e.RbOH的碱性比同浓度的NaOH弱
(4)关于元素周期表、周期律,下列说法正确的是___________(填序号)。
| A.在金属和非金属分界处可以找到半导体材料 |
| B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素 |
| C.通常农药所含有的元素位于元素周期表左下方区域 |
| D.稀有气体原子都满足8电子稳定结构 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】下图是元素周期表的一部分,回答下列问题:

(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是_______ 元素(填元素符号)。
② 的酸性强弱:
的酸性强弱:
_______ (填“>”“<”或“=”) 。
。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是
②
 的酸性强弱:
的酸性强弱:
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用。
(1)下列说法正确的是__________ (填序号)。
(2)CH4和CO2在Ni催化作用下反应可获得化工原料CO和H2。
①Ni基态原子核外电子排布式为__________ 。
②与CO互为等电子体的阴离子的电子式为__________ ,Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有σ键的数目为__________ 。
(3)CH4和CO2在含有钛氧化物的某种催化剂作用下,可直接转化为CH3COOH。
①CH3COOH中C原子轨道杂化类型为__________ ;
②钛氧化物晶胞结构如图所示,写出其化学式:__________ 。

(1)下列说法正确的是
| A.CH4与CO2分子均为含有极性共价键的非极性分子 | B.第一电离能:O>N>C |
| C.沸点高低:CH4>SnH4>GeH4>SiH4 | D.CH 离子的空间构型为平面正三角形 离子的空间构型为平面正三角形 |
①Ni基态原子核外电子排布式为
②与CO互为等电子体的阴离子的电子式为
(3)CH4和CO2在含有钛氧化物的某种催化剂作用下,可直接转化为CH3COOH。
①CH3COOH中C原子轨道杂化类型为
②钛氧化物晶胞结构如图所示,写出其化学式:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】PtCl2(NH3)2是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子,甲、乙的水解产物化学式均为Pt(OH)2(NH3)2,但只有甲的水解产物能与草酸(HOOC-COOH)反应生成Pt(C2O4)(NH3)2,根据信息,完成下题:
(1)根据相似相溶的规律,可推断_____ (填“甲”或“乙”)在水中的溶解度较大。
(2)Pt(OH)2(NH3)2中H-N-H的键角大于NH3分子中的H-N-H键角,请结合所学知识解释原因_____ 。
(3)查阅资料可知,甲、乙均为平面结构,画出乙的水解产物的空间结构_____ 。
(1)根据相似相溶的规律,可推断
(2)Pt(OH)2(NH3)2中H-N-H的键角大于NH3分子中的H-N-H键角,请结合所学知识解释原因
(3)查阅资料可知,甲、乙均为平面结构,画出乙的水解产物的空间结构
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D四种元素中,A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D是形成化合物种类最多的元素。
(1)A、D形成的某化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键与π键数目之比为___________ ;写出由甲制高聚物的反应方程式___________ 。
(2)A、C形成的某化合物乙中含非极性共价键,乙分子属于___________ (填“极性分子”或“非极性分子”);其电子式为___________ ,中心原子采取的杂化方式为___________ 。
(3)B的基态原子轨道表示式为___________ 。与 相比,
相比, 易液化的主要原因是
易液化的主要原因是___________ 。
(4)笑气(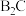 )是一种麻醉剂,有关理论认为
)是一种麻醉剂,有关理论认为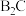 与
与 分子具有相似的结构。故
分子具有相似的结构。故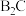 的空间结构是
的空间结构是___________ 。
(1)A、D形成的某化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键与π键数目之比为
(2)A、C形成的某化合物乙中含非极性共价键,乙分子属于
(3)B的基态原子轨道表示式为
 相比,
相比, 易液化的主要原因是
易液化的主要原因是(4)笑气(
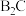 )是一种麻醉剂,有关理论认为
)是一种麻醉剂,有关理论认为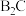 与
与 分子具有相似的结构。故
分子具有相似的结构。故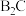 的空间结构是
的空间结构是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】铁( )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)铁系元素能与 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点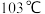 ,则
,则 中含有的化学键类型包括________(填字母)。
中含有的化学键类型包括________(填字母)。
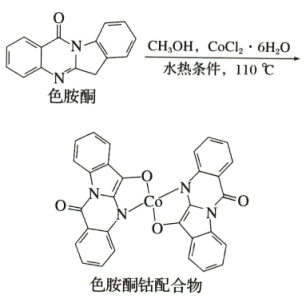
(2)以甲醇为溶剂, 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对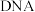 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序为
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序为________ ,色胺酮分子中N原子的杂化类型为________ 。X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 是通过
是通过________ 作用与色胺酮钴配合物相结合。
(3)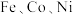 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点,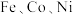 明显高于
明显高于 ,其原因是
,其原因是________________________ 。
(4) 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如图所示:
的晶胞结构如图所示:
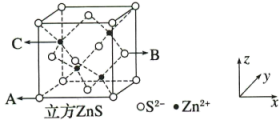
①已知A、B点的原子坐标分别为 和
和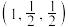 ,则C点的原子坐标为
,则C点的原子坐标为________ ;
②立方 的晶胞参数
的晶胞参数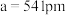 ,则其晶体密度为
,则其晶体密度为________  (列出计算表达式,设
(列出计算表达式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。(1)铁系元素能与
 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点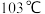 ,则
,则 中含有的化学键类型包括________(填字母)。
中含有的化学键类型包括________(填字母)。| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对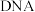 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序为
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序为 分子,
分子, 是通过
是通过
(3)
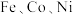 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点,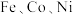 明显高于
明显高于 ,其原因是
,其原因是(4)
 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如图所示:
的晶胞结构如图所示:
①已知A、B点的原子坐标分别为
 和
和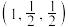 ,则C点的原子坐标为
,则C点的原子坐标为②立方
 的晶胞参数
的晶胞参数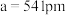 ,则其晶体密度为
,则其晶体密度为 (列出计算表达式,设
(列出计算表达式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为___________ ; 键角
键角___________ 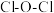 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。
(3)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体,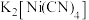 是红黄色单斜晶体。
是红黄色单斜晶体。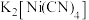 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: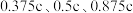 。晶胞中氢键的长度为
。晶胞中氢键的长度为___________  (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(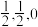 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为___________ ,该缺陷晶型的化学式可表示为___________ 。设阿伏加德罗常数的值为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为___________  (列出表达式)。
(列出表达式)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.  B.
B.
C. D.
D.
 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为 键角
键角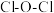 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。(3)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体,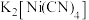 是红黄色单斜晶体。
是红黄色单斜晶体。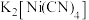 的熔点高于
的熔点高于 的原因是
的原因是(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数
 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: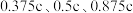 。晶胞中氢键的长度为
。晶胞中氢键的长度为 (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。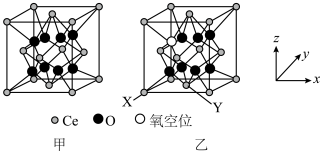
 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(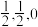 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜及其化合物用途广泛。 溶液与乙二胺
溶液与乙二胺 可形成配离子
可形成配离子 (
(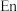 是乙二胺的简写):
是乙二胺的简写):

(1) 的价电子轨道表示式为:
的价电子轨道表示式为:_______ ;
(2)乙二胺和三甲胺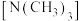 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______ 。
(3)配离子 的配位数为
的配位数为_______ ,该微粒含有的微粒间的作用力类型有_______ (填字母);
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(4) 为平面正方形结构,其中的两个
为平面正方形结构,其中的两个 被
被 取代后有两种不同的结构,其中
取代后有两种不同的结构,其中 是非极性分子的结构式为
是非极性分子的结构式为_______ 。
(5)铜镍合金的立方晶胞结构如图所示,其中原子A的坐标参数为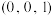 。
。

①原子B的坐标参数为_______
②)若该晶体密度为 ,则铜镍原子间最短距离为
,则铜镍原子间最短距离为_______ cm。
 溶液与乙二胺
溶液与乙二胺 可形成配离子
可形成配离子 (
(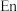 是乙二胺的简写):
是乙二胺的简写):
(1)
 的价电子轨道表示式为:
的价电子轨道表示式为:(2)乙二胺和三甲胺
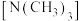 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是(3)配离子
 的配位数为
的配位数为A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(4)
 为平面正方形结构,其中的两个
为平面正方形结构,其中的两个 被
被 取代后有两种不同的结构,其中
取代后有两种不同的结构,其中 是非极性分子的结构式为
是非极性分子的结构式为(5)铜镍合金的立方晶胞结构如图所示,其中原子A的坐标参数为
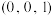 。
。
①原子B的坐标参数为
②)若该晶体密度为
 ,则铜镍原子间最短距离为
,则铜镍原子间最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】物质结构决定物质性质,试用物质结构知识解释下列实验事实
(1)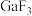 熔点比
熔点比 熔点高很多:
熔点高很多:_______ 。
(2)接近沸点的水蒸气的相对分子质量测定值大于18:_______ 。
(3)向 的
的 溶液中加入浓
溶液中加入浓 溶液,振荡后静置,
溶液,振荡后静置, 层紫色变浅:
层紫色变浅:_______ 。
(4) 分子中
分子中 键角大于
键角大于 分子中
分子中 :
:_______ 。
(5)Mn的第三电离能大于Fe的第三电离能:_______ 。
(1)
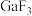 熔点比
熔点比 熔点高很多:
熔点高很多: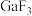 |  | 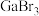 | |
熔点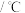 |  | 77.75 | 122.3 |
(3)向
 的
的 溶液中加入浓
溶液中加入浓 溶液,振荡后静置,
溶液,振荡后静置, 层紫色变浅:
层紫色变浅:(4)
 分子中
分子中 键角大于
键角大于 分子中
分子中 :
:(5)Mn的第三电离能大于Fe的第三电离能:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钛的化合物在化工、医药、材料等领域具有广泛应用。回答下列问题:
(1)Ti元素处于周期表的___________ 区,基态Ti原子4s轨道上的一个电子激发到4p轨道上形成激发态,写出该激发态价层电子排布式___________ 。
(2)钛卤化物的熔点和沸点如下表所示:
① 、
、 、
、 熔沸点依次升高的原因是
熔沸点依次升高的原因是___________ ;
② 熔点反常的原因是
熔点反常的原因是___________ 。
(3)Ti可形成配合物 ,urea表示尿素,其结构如下图所示:
,urea表示尿素,其结构如下图所示:

①配合物中Ti的化合价为___________ 。
②尿素中C原子的杂化轨道类型为___________ ,除H外,其余元素的第一电离能的大小关系为___________ 。
③ 的空间结构为
的空间结构为___________ 。
(4)如图为具有较高催化活性材料金红石的晶胞结构(已知4个氧原子在图形的面上,2个氧原子在图形的内部),若晶胞边长为apm,则金红石晶体的密度为___________ g·cm-3(列出计算式)。

[已知晶胞密度 (m为晶胞的质量,v为晶胞的体积)]。
(m为晶胞的质量,v为晶胞的体积)]。
(1)Ti元素处于周期表的
(2)钛卤化物的熔点和沸点如下表所示:
①
 、
、 、
、 熔沸点依次升高的原因是
熔沸点依次升高的原因是②
 熔点反常的原因是
熔点反常的原因是 |  |  |  | |
| 熔点/℃ | 377 | -24 | 38 | 150 |
| 沸点/℃ | - | 136 | 230 | 377 |
 ,urea表示尿素,其结构如下图所示:
,urea表示尿素,其结构如下图所示:
①配合物中Ti的化合价为
②尿素中C原子的杂化轨道类型为
③
 的空间结构为
的空间结构为(4)如图为具有较高催化活性材料金红石的晶胞结构(已知4个氧原子在图形的面上,2个氧原子在图形的内部),若晶胞边长为apm,则金红石晶体的密度为

[已知晶胞密度
 (m为晶胞的质量,v为晶胞的体积)]。
(m为晶胞的质量,v为晶胞的体积)]。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】锌在工业中有重要作用,也是人体必需的微量元素,回答下列问题:
(1)Zn2+原子核外电子排布式为_______________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)______ I1(Cu)填“大于”或“小于”)。原因是_______________________________ 。
(3)ZnF2具有较高的熔点(872℃),其化学键类型是______ ,ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是_____________________________________ 。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为______ ,C原子的杂化形式为___________________ 。

(5)金属Zn晶体中这种堆积方式称为_______________ 。该晶胞中含有的微粒个数为______ 。
(1)Zn2+原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(3)ZnF2具有较高的熔点(872℃),其化学键类型是
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为

(5)金属Zn晶体中这种堆积方式称为
您最近一年使用:0次



