甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)下图是在不同温度下CO的转化率随时间变化的曲线。
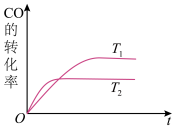
①T1_______ T2(填“>”、“<”或“=”)。该反应的ΔH_______ 0(填“>”、“<”或“=”)。
②若容器容积不变,下列措施能增加CO平衡转化率的是_______ (填字母)。
a.降低温度 b.使用合适的催化剂
c.将CH3OH(g)从体系中分离 d.充入He,使体系总压强增大
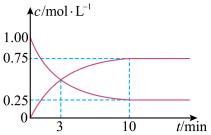
(2)下图是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率υ(CO)=_______ ;H2的平衡转化率为_______ 。
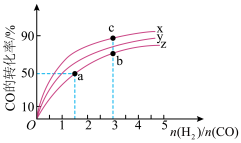
(3)一定温度下恒容容器中,分别研究在PX,PY,PZ三种压强下合成甲醇的规律。如图是上述三种压强下H2和CO的起始组成比[ ]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是_______ ,此时该反应的化学平衡常数KX,KY,KZ的大小关系为_______ 。
 CH3OH(g)。
CH3OH(g)。(1)下图是在不同温度下CO的转化率随时间变化的曲线。

①T1
②若容器容积不变,下列措施能增加CO平衡转化率的是
a.降低温度 b.使用合适的催化剂
c.将CH3OH(g)从体系中分离 d.充入He,使体系总压强增大
(2)下图是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率υ(CO)=

(3)一定温度下恒容容器中,分别研究在PX,PY,PZ三种压强下合成甲醇的规律。如图是上述三种压强下H2和CO的起始组成比[
 ]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
更新时间:2022-11-11 11:29:00
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)  Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
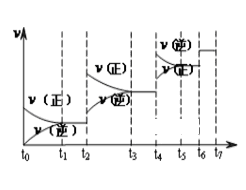
(1)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与 时间t的关系如图。图中t4时引起平衡移动的条件可能是______________________ ;图中表示平衡混合物中CO的含量最高的一段时间是____________ 。
(2)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是__________________ (提示:272 = 729)。
 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)(1)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与 时间t的关系如图。图中t4时引起平衡移动的条件可能是
(2)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
a.CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1
b.CO2(g)+H2(g) CO(g)+H2O(g)ΔH2
CO(g)+H2O(g)ΔH2
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比。
请回答(不考虑温度对ΔH的影响):
(1)反应a的平衡常数表达式K=___ ;
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有___ 。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___ 。
(4)在图中分别画出反应I在有Cat.1和有Cat.2两种情况下“反应过程-能量”示意图(图中的2条曲线要标注Cat.1和Cat.2)___ 。

a.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1b.CO2(g)+H2(g)
 CO(g)+H2O(g)ΔH2
CO(g)+H2O(g)ΔH2某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
| T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比。
请回答(不考虑温度对ΔH的影响):
(1)反应a的平衡常数表达式K=
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是
(4)在图中分别画出反应I在有Cat.1和有Cat.2两种情况下“反应过程-能量”示意图(图中的2条曲线要标注Cat.1和Cat.2)

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)化学反应 2NO(g)+2CO(g)=N2(g)+2CO2(g)在 298 K、100 kPa 下:ΔH=-113.0 kJ/mol,ΔS=-0.1kJ/(mol·K),反应在常温下________ (填“能”或“不能”)自发进行。
(2)在密闭容器中,控制不同温度进行 2SO3(g) 2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
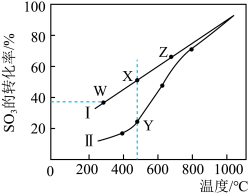
①比较图中X 点与 Y 点、X 点与 Z 点的平衡常数大小:K(X)______ K(Y),K(X)_______ K(Z)(填“>”“<”或“=”)。
②Y 点的反应速率:υ正____ υ逆(填“>”“<”或“=”)。
③随温度升高,曲线Ⅱ逼近曲线Ⅰ的原因是_______ 。
④下列措施在其他条件不变时,能提高 SO3转化率的是____ 。
A.使用合适的催化剂 B.升高温度 C.增大压强 D.降低温度 E.减小压强 F.SO3的起始浓度增加至 2c mol/L
(2)在密闭容器中,控制不同温度进行 2SO3(g)
 2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
2SO2(g)+O2(g)实验。已知 SO3起始浓度均为c mol/L,测定 SO3的转化率。图中曲线Ⅰ为 SO3的平衡转化率与温度的关系,曲线Ⅱ表示不同温度下,反应经过相同时间尚未达到化学平衡时 SO3的转化率。
①比较图中X 点与 Y 点、X 点与 Z 点的平衡常数大小:K(X)
②Y 点的反应速率:υ正
③随温度升高,曲线Ⅱ逼近曲线Ⅰ的原因是
④下列措施在其他条件不变时,能提高 SO3转化率的是
A.使用合适的催化剂 B.升高温度 C.增大压强 D.降低温度 E.减小压强 F.SO3的起始浓度增加至 2c mol/L
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,在2L 的密闭容器中,A、B、C 三种气体物质的量随时间变化的曲线如图I, 能量变化如图 II 所示:

(1)从反应开始到到5s,用C 表示的反应速度为_____ , A 的转化率为_______ ,该化学反应的平衡常数为____________ 。
(2)分析图 II , 该反应的反应热ΔH =______ ,逆反应的活化能是___ 。
(3)将2. 00molA(g)、2. 00molB(g)的混合气体分别置于a、b、c 三个起始体积相同的密闭容器中,使反应在不同条件下进行,反应过程中 C 的浓度随时间的变化如图 III所示。

①反应从开始到达到平衡.反应速率由大到小的顺序为________ (用a、b、c 表示)。
② 与容器a中的反应相比,容器b中的反应改变的实验条件可能是______ ,容器c 中的反应改变的实验条件可能是___________ 。

(1)从反应开始到到5s,用C 表示的反应速度为
(2)分析图 II , 该反应的反应热ΔH =
(3)将2. 00molA(g)、2. 00molB(g)的混合气体分别置于a、b、c 三个起始体积相同的密闭容器中,使反应在不同条件下进行,反应过程中 C 的浓度随时间的变化如图 III所示。

①反应从开始到达到平衡.反应速率由大到小的顺序为
② 与容器a中的反应相比,容器b中的反应改变的实验条件可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)对于下列反应:2SO2 +O2 2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为
2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为________ 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_______ 。

(2)下图左表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是_____ ;b-c过程中改变的条件可能是________ ;若增大压强时,反应速度变化情况画在c~d处。_______
(3)酶是蛋白质,具有蛋白质的特性,酶能催化很多化学反应,下图表示酶参加的反应中,温度与反应速率的关系。解释曲线变化原因__________________ 。

 2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为
2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用O2浓度变化来表示的反应速率为
(2)下图左表示在密闭容器中反应:2SO2+O2
 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是(3)酶是蛋白质,具有蛋白质的特性,酶能催化很多化学反应,下图表示酶参加的反应中,温度与反应速率的关系。解释曲线变化原因

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
⑴根据下图,计算从反应开始到平衡时,平均反应速率v(NH3)=______________________________

⑵该反应450℃的平衡常数________ 500℃时的平衡常数(填“>”、“<”或“=”)。
⑶下列描述中能说明上述反应已达平衡的是___________ 。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡_______________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
⑸第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线___________ 。
 2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:⑴根据下图,计算从反应开始到平衡时,平均反应速率v(NH3)=

⑵该反应450℃的平衡常数
⑶下列描述中能说明上述反应已达平衡的是
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡
⑸第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线
您最近一年使用:0次



