冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石(Na3AlF6)的化学方程式为2Al(OH)3+12HF+3A =2Na3AlFs+3CO2+9H2O。
(1)熔融晶体A时痛要破坏的作用力是_______ ,冰晶石中的配位体是______ 。
(2)上述反应的生成物中属于非极性分子的中心原子的杂化轨道类型为________________ ,该分子的空间构型为___________ 。
(3)上述反应的反应物中有两种元素在元素周期表中的位置相邻,用化学方程式表示二者的电负性大小:____________ ;写出含有其中电负性较小元素的原子,且形成的分子的空间构型呈“V”形的物质的化学式(单质和化合物各写一种)_______________ 、________________ 。
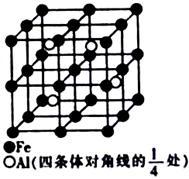
(4)某种Al—Fe合金的晶胞如图所示,该合金的化学式为_________ 。若晶胞的边长为a nm,则合金的密度为______ g• cm-3。
(1)熔融晶体A时痛要破坏的作用力是
(2)上述反应的生成物中属于非极性分子的中心原子的杂化轨道类型为
(3)上述反应的反应物中有两种元素在元素周期表中的位置相邻,用化学方程式表示二者的电负性大小:
(4)某种Al—Fe合金的晶胞如图所示,该合金的化学式为

2013·河北邯郸·二模 查看更多[1]
(已下线)2013届河北省邯郸市高三第二次模拟考试理综化学试卷
更新时间:2016-12-09 04:44:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】水是生命之源,它与我们的生活密切相关。在化学实验中,水也是一种常用的试剂。
(1)水分子与H+形成水合氢离子( H3O +)的立体构型为_______ 。
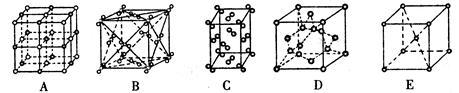
(2)冰是立方面心结构。下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞示意图(未按顺序排序)。上述五种晶体中与冰的晶体类型相同的是_______ ;(填写编号)。
(3)在冰的晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),

已知冰的升华热(即1mol水由冰转化为水蒸气所需能量)是51KJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”(破坏lmol氢键所需的能量即为氢键的“键能”)是_______ kJ/mol。
(1)水分子与H+形成水合氢离子( H3O +)的立体构型为
(2)冰是立方面心结构。下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞示意图(未按顺序排序)。上述五种晶体中与冰的晶体类型相同的是

(3)在冰的晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),

已知冰的升华热(即1mol水由冰转化为水蒸气所需能量)是51KJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”(破坏lmol氢键所需的能量即为氢键的“键能”)是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表某一元素。
(1)A的的最高价氧化物对应水化物的电子式为__________ 。
(2)R是由表中已标出的A~F 中某三种元素组成的化合物,是常见家用消毒剂的主要成分,其化学名称为_____________ ;Na2FeO4是工业常用的消毒剂,利用R 制备Na2FeO4的原理如下,请补齐缺少的物质,并配平反应方程式的系数:___ Fe(OH)3 + ___R(________) + ___ NaOH = ____ Na2FeO4 + ___ NaCl + ____H2O
(3)气态氢化物沸点:D_____ E;元素形成的简单离子的半径:A _____ D(填“>”,“<”或“=”)
(4)E 的某种氧化物通入F 单质的水溶液中,并不能增大F 单质水溶液的漂白性,请结合方程式说明______________________________________________________________ 。
(5)由表中未标出的某种金属元素的单质G ,可以发生如图所示的转化:

①写出 G 转化为 K 的化学方程式________________________________________ 。
②写出 L 转化为 M 的离子方程式________________________________________ 。
| B | C | D | |||||
| A | E | F | |||||
(1)A的的最高价氧化物对应水化物的电子式为
(2)R是由表中已标出的A~F 中某三种元素组成的化合物,是常见家用消毒剂的主要成分,其化学名称为
(3)气态氢化物沸点:D
(4)E 的某种氧化物通入F 单质的水溶液中,并不能增大F 单质水溶液的漂白性,请结合方程式说明
(5)由表中未标出的某种金属元素的单质G ,可以发生如图所示的转化:

①写出 G 转化为 K 的化学方程式
②写出 L 转化为 M 的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是___________。
(2)硼酸( )溶液呈酸性,试写出其电离方程式:
)溶液呈酸性,试写出其电离方程式:___________ 。
(3)科学家对 结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
结构的认识经历了较为漫长的过程,最初,科学家提出了种观点: 与浓
与浓 反应生成
反应生成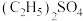 和水;
和水;
b.将制得的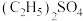 与
与 反应,只生成A和
反应,只生成A和 ;
;
c.将生成的A与 反应(已知该反应中
反应(已知该反应中 作还原剂)。
作还原剂)。
①如果 的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
的结构如甲所示,实验c中化学反应方程式为(A写结构简式)___________ 。
②为了进一步确定 的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:___________ 。
(1)下列粒子中可能存在配位键的是___________。
A. | B. | C. | D. |
(2)硼酸(
 )溶液呈酸性,试写出其电离方程式:
)溶液呈酸性,试写出其电离方程式:(3)科学家对
 结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:甲: 、乙:
、乙: ,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究
,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究 的结构,设计并完成了下列实验:
的结构,设计并完成了下列实验:
 与浓
与浓 反应生成
反应生成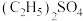 和水;
和水;b.将制得的
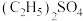 与
与 反应,只生成A和
反应,只生成A和 ;
;c.将生成的A与
 反应(已知该反应中
反应(已知该反应中 作还原剂)。
作还原剂)。①如果
 的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
的结构如甲所示,实验c中化学反应方程式为(A写结构简式)②为了进一步确定
 的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,________ (填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有________ 种。
(3)H2S和H2Se的参数对比见下表。
①H2Se分子中含有的共价键类型为_____________ (填“σ”或“π”)。
②H2S的键角大于H2Se的原因可能为______________________________ 。
③H2Se的酸性比H2S________ (填“强”或“弱”)。
(4)已知钼(Mo)位于第五周期ⅥB族,钼、铬、锰的部分电离能如下表所示:
A是____________ (填元素符号),B的价电子排布式为____________ 。

(1)天冬酰胺所含元素中,
(2)天冬酰胺中碳原子的杂化轨道类型有
(3)H2S和H2Se的参数对比见下表。
| 化学式 | 键长/nm | 键角 | 沸点/℃ |
| H2S | 1.34 | 92.3° | -60.75 |
| H2Se | 1.47 | 91.0° | -41.50 |
①H2Se分子中含有的共价键类型为
②H2S的键角大于H2Se的原因可能为
③H2Se的酸性比H2S
(4)已知钼(Mo)位于第五周期ⅥB族,钼、铬、锰的部分电离能如下表所示:
| 编号 | I5/kJ·mol-1 | I6/kJ·mol-1 | I7/kJ·mol-1 | I8/kJ·mol-1 |
A | 6990 | 9220 | 11500 | 18770 |
B | 6702 | 8745 | 15455 | 17820 |
C | 5257 | 6641 | 12125 | 13860 |
A是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据元素周期表中完整周期元素的性质,填写下列空白。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其基态原子的简化电子排布式为_______ ,有_______ 个未成对电子,有_______ 个能级,能量最高的能级符号为_______ 。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ ,原子中所有电子占有_______ 个轨道,核外共有_______ 个不同运动状态的电子。
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显_______ 性(填“酸”、“碱”或“中”),用离子方程式解释其原因_______ 。
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为_______ 。电解一段时间后,阴极区pH_______ (填“增大”、“减小”或“不变”)
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W的第一电离能比氧原子的________ (填“大”或“小”),W的气态氢化物稳定性比H2O(g)_______ (填“强”或“弱”),W的单质分子中含_________ 个∏键;
(2)Z位于元素周期表第__ 周期第___ 族,Z的基态原子核外电子排布式是________ ;
(3)X、Y的最高价氧化物对应水化物相互反应的离子方程式是
_______________________________________________________________ 。
(1)W的第一电离能比氧原子的
(2)Z位于元素周期表第
(3)X、Y的最高价氧化物对应水化物相互反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)有机化合物 是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有
是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有______ 、_______ 、_____ (写名称),它属于________ (填“脂环”或“芳香族”)化合物。
(2)1 mol CH2=CH—CH2OH含________ mol σ键,烯丙醇分子中碳原子的杂化类型为________ 。
(3)乙炔与氢氰酸(HCN)反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中σ键和π键的个数之比为___________ ,分子中处于同一直线上的原子数目最多为_______ 。
(1)有机化合物
 是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有
是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有(2)1 mol CH2=CH—CH2OH含
(3)乙炔与氢氰酸(HCN)反应可得丙烯腈(H2C=CH—C≡N)。丙烯腈分子中σ键和π键的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】材料科学的应用领域十分广泛,如做磁性元器件的纳米晶软磁合金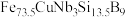 ;合成全氮材料中间体的五氮阴离子盐
;合成全氮材料中间体的五氮阴离子盐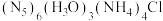 。回答下列问题:
。回答下列问题:
(1) 元素在元素周期表中的位置是
元素在元素周期表中的位置是_______ ,基态 原子的未成对电子数是
原子的未成对电子数是_______ 。
(2)基态 原子的核外价电子排布式为
原子的核外价电子排布式为_______ , 位于元素周期表的
位于元素周期表的_______ 区,基态N原子的价电子排布图为_______ 。
(3) 原子的核外电子有
原子的核外电子有_______ 种不同的运动状态,次外层电子云有_______ 种不同的伸展方向。
(4) 呈色,配位数是
呈色,配位数是_______ , 中
中 键的数目为
键的数目为_______ 。
(5)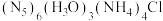 中两种阳离子的中心原子杂化方式都是
中两种阳离子的中心原子杂化方式都是_______ ; 的电子式为
的电子式为_______ 。
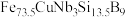 ;合成全氮材料中间体的五氮阴离子盐
;合成全氮材料中间体的五氮阴离子盐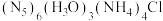 。回答下列问题:
。回答下列问题:(1)
 元素在元素周期表中的位置是
元素在元素周期表中的位置是 原子的未成对电子数是
原子的未成对电子数是(2)基态
 原子的核外价电子排布式为
原子的核外价电子排布式为 位于元素周期表的
位于元素周期表的(3)
 原子的核外电子有
原子的核外电子有(4)
 呈色,配位数是
呈色,配位数是 中
中 键的数目为
键的数目为(5)
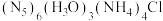 中两种阳离子的中心原子杂化方式都是
中两种阳离子的中心原子杂化方式都是 的电子式为
的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】配合物X{[Cu(phen)(Thr)(H2O)]ClO4}能够通过插入或部分插入的模式与DNA作用,它可由Cu(ClO4)2、HThr(结构简式如图l所示)、phen等为原料制备。
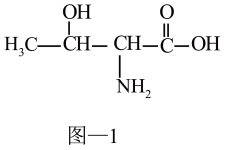
(1)Cu2+基态电子排布式为___ 。
(2)ClO4-的空间构型为__ (用文字描述),与ClO4-互为等电子体的一种分子的化学式为___ 。
(3)HThr分子中,碳原子的杂化类型为___ ;1molHThr中含有σ键的数目为___ 。
(4)配合物X中配离子的结构如图2所示,则配位原子为___ (填元素符号)。


(1)Cu2+基态电子排布式为
(2)ClO4-的空间构型为
(3)HThr分子中,碳原子的杂化类型为
(4)配合物X中配离子的结构如图2所示,则配位原子为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】中国古代四大发明之一——黑火药,它在爆炸时发生的化学反应为2KNO3+3C+S=A+N2↑+3CO2↑(已配平)
(1)①除S外,上列元素的电负性从大到小依次为__________ 。
②在生成物中,A的晶体类型为_______ ,含极性共价键的分子的中心原子轨道杂化类型为_____ 。
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为_____ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______ ,Q2+的未成对电子数是_______ 。
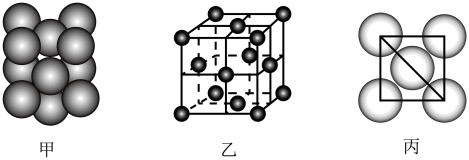
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________ 。
(1)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的晶体类型为
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d第一电离能大小关系为___________________ ,e的外围电子排布图为_____________________ 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_________ ;分子中既含有极性共价键,又含有非极性共价键的化合物是_____________ (填化学式,写两种)。
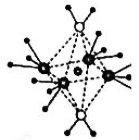
(3)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如下图所示)。该化合物中阴离子为__________ ,阳离子中存在的化学键类型有________________ ;
(1)b、c、d第一电离能大小关系为
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为
(3)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如下图所示)。该化合物中阴离子为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据如表所示:
(1)Mn元素原子的价电子排布式为___________ 。比较两元素的I2、I3可知:气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是___________
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是___________ 。
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为___________ 。

| 元素 | Mn | Fe | |
| 电离能/(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(1)Mn元素原子的价电子排布式为
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次



