Ⅰ.已知在25℃时,次氯酸、碳酸和亚硫酸的电离平衡常数分别为:
HClO

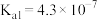
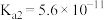

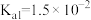
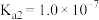
(1)相同浓度的 、
、 、
、 、
、 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为_______ 。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)室温下, 通入NaOH溶液中,在所得溶液中,
通入NaOH溶液中,在所得溶液中,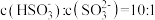 ,则溶液的pH=
,则溶液的pH=_______ 。
II.水在25℃和95℃时电离平衡曲线如图。
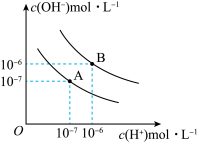
(4)在曲线A所对应的温度下,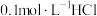 溶液由水电离出来的
溶液由水电离出来的
_______  。
。
(5)在曲线A所对应的温度下, 的下列溶液:①HCl②
的下列溶液:①HCl② ③
③ ④NaOH ⑤
④NaOH ⑤ ,pH由大到小的顺序是
,pH由大到小的顺序是_______ (填序号顺序)。
(6)在曲线A所对应的温度下, 的醋酸与
的醋酸与 的NaOH等体积混合,所得溶液的pH
的NaOH等体积混合,所得溶液的pH_______ 7(填“>”“<”或“=”)。
(7)在曲线B所对应的温度下,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的6,则NaOH溶液与
溶液混合,若所得混合溶液的6,则NaOH溶液与 溶液的体积比为
溶液的体积比为_______ 。
HClO


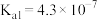
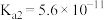

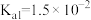
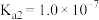
(1)相同浓度的
 、
、 、
、 、
、 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为(2)写出
 的电离方程式
的电离方程式(3)室温下,
 通入NaOH溶液中,在所得溶液中,
通入NaOH溶液中,在所得溶液中,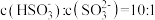 ,则溶液的pH=
,则溶液的pH=II.水在25℃和95℃时电离平衡曲线如图。

(4)在曲线A所对应的温度下,
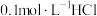 溶液由水电离出来的
溶液由水电离出来的
 。
。(5)在曲线A所对应的温度下,
 的下列溶液:①HCl②
的下列溶液:①HCl② ③
③ ④NaOH ⑤
④NaOH ⑤ ,pH由大到小的顺序是
,pH由大到小的顺序是(6)在曲线A所对应的温度下,
 的醋酸与
的醋酸与 的NaOH等体积混合,所得溶液的pH
的NaOH等体积混合,所得溶液的pH(7)在曲线B所对应的温度下,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的6,则NaOH溶液与
溶液混合,若所得混合溶液的6,则NaOH溶液与 溶液的体积比为
溶液的体积比为
更新时间:2022-11-27 15:36:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知水的电离平衡曲线如图所示。 是
是_______ 。
(2)造成C点到A点水的离子积变化的原因是_______ 。
(3)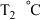 ,溶液
,溶液 的溶液可能是_______。
的溶液可能是_______。
(4)①向水中滴加 溶液可实现
溶液可实现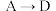 点的变化,则D点对应溶液的
点的变化,则D点对应溶液的 为
为_______ 。
② 时,若某盐酸中
时,若某盐酸中 ,则由水电离产生的c(H+)=
,则由水电离产生的c(H+)=_______________ mol/L。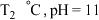 的
的 溶液浓度为
溶液浓度为_______ mol/L。
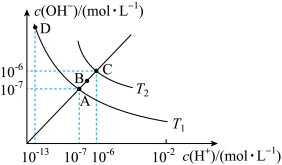
 是
是(2)造成C点到A点水的离子积变化的原因是
(3)
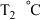 ,溶液
,溶液 的溶液可能是_______。
的溶液可能是_______。A. 溶液 溶液 | B.氨水 | C.氯化钠溶液 | D.稀硝酸 |
(4)①向水中滴加
 溶液可实现
溶液可实现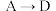 点的变化,则D点对应溶液的
点的变化,则D点对应溶液的 为
为②
 时,若某盐酸中
时,若某盐酸中 ,则由水电离产生的c(H+)=
,则由水电离产生的c(H+)=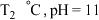 的
的 溶液浓度为
溶液浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水是一种极其微弱的电解质。
(1)已知t℃时纯水的 ,计算该温度下水的离子积
,计算该温度下水的离子积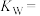
_______ ,该温度下 的硫酸溶液中水电离出的
的硫酸溶液中水电离出的
_______  。
。
(2)对水进行下列操作,能抑制水的电离的是_______。
(3)已知水的电离平衡曲线如图所示:回答下列问题:
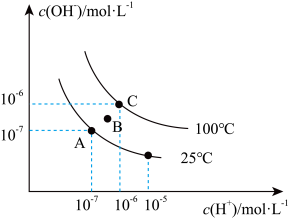
A、B、C、D四点 的关系是
的关系是_______ ( 、
、 …表示)。
…表示)。
(4)室温下,实验测得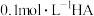 溶液的
溶液的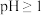 ,下列说法正确的是
,下列说法正确的是_______ 。
a. 可能呈酸性
可能呈酸性
b. 溶液中
溶液中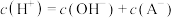
c.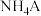 可能呈中性
可能呈中性
(1)已知t℃时纯水的
 ,计算该温度下水的离子积
,计算该温度下水的离子积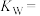
 的硫酸溶液中水电离出的
的硫酸溶液中水电离出的
 。
。(2)对水进行下列操作,能抑制水的电离的是_______。
A.加入一小块 | B.加入适量 溶液 溶液 |
| C.升温至60℃ | D.通入适量 气体 气体 |
(3)已知水的电离平衡曲线如图所示:回答下列问题:

A、B、C、D四点
 的关系是
的关系是 、
、 …表示)。
…表示)。(4)室温下,实验测得
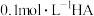 溶液的
溶液的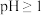 ,下列说法正确的是
,下列说法正确的是a.
 可能呈酸性
可能呈酸性b.
 溶液中
溶液中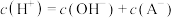
c.
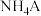 可能呈中性
可能呈中性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡。请回答下列问题:
(1)常温下,物质的量浓度均为0.1mol·L-1的六种溶液
①Na2CO3、②NaCl、③NaOH、④(NH4)2SO4、⑤CH3COONa、⑥NH4NO3 , pH从大到小排列顺序为__________ (填序号)。
(2)已知T℃时,Kw=1×10-12,在该温度时,将pH=9的NaOH溶液bL与pH=2的H2SO4溶液aL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3, 则a:b=__________ 。
(3)现有HA、HB两种酸。室温下用0.1mol· L-1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如下图。

①由图可知;酸性HA______ HB,b 点对应的溶液中c(HB)_____ c(B-)(填“>”“<”或“=”)。
②室温下HB的电离平衡常数Ka的数量级为________ 。
(1)常温下,物质的量浓度均为0.1mol·L-1的六种溶液
①Na2CO3、②NaCl、③NaOH、④(NH4)2SO4、⑤CH3COONa、⑥NH4NO3 , pH从大到小排列顺序为
(2)已知T℃时,Kw=1×10-12,在该温度时,将pH=9的NaOH溶液bL与pH=2的H2SO4溶液aL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3, 则a:b=
(3)现有HA、HB两种酸。室温下用0.1mol· L-1NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如下图。

①由图可知;酸性HA
②室温下HB的电离平衡常数Ka的数量级为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知 时,三种酸的平衡常数分别为:
时,三种酸的平衡常数分别为: 的
的 ;
; 的
的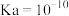 ;
; 的
的 ;
;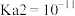 回答下列问题:
回答下列问题:
(1)将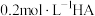 溶液与
溶液与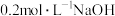 溶液等体积混合,测得混合溶液中
溶液等体积混合,测得混合溶液中 ,混合溶液中
,混合溶液中
_______  ;
;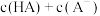
_____  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(2)将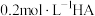 溶液与
溶液与 氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的
氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的 较大的是
较大的是________ (填(1)或(2))。
(3) 相同的
相同的 两溶液稀释后
两溶液稀释后 仍相同,加水量:
仍相同,加水量:
________  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(4) 溶液与
溶液与 溶液混合,当溶液中
溶液混合,当溶液中 时,溶液的
时,溶液的
___________ 。
(5)同浓度的四种溶液:① ②
② ③
③ 溶液,
溶液, 由大到小的顺序是
由大到小的顺序是___________ 。
(6)写出 的
的 表达式
表达式___________ 。
 时,三种酸的平衡常数分别为:
时,三种酸的平衡常数分别为: 的
的 ;
; 的
的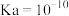 ;
; 的
的 ;
;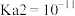 回答下列问题:
回答下列问题:(1)将
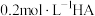 溶液与
溶液与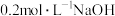 溶液等体积混合,测得混合溶液中
溶液等体积混合,测得混合溶液中 ,混合溶液中
,混合溶液中
 ;
;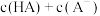
 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(2)将
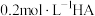 溶液与
溶液与 氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的
氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的 较大的是
较大的是(3)
 相同的
相同的 两溶液稀释后
两溶液稀释后 仍相同,加水量:
仍相同,加水量:
 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(4)
 溶液与
溶液与 溶液混合,当溶液中
溶液混合,当溶液中 时,溶液的
时,溶液的
(5)同浓度的四种溶液:①
 ②
② ③
③ 溶液,
溶液, 由大到小的顺序是
由大到小的顺序是(6)写出
 的
的 表达式
表达式
您最近一年使用:0次
【推荐3】回答下列问题:
(1)某元素基态的正三价离子的3d轨道有3个电子,该元素的元素符号是_______ ,其基态原子的电子排布式为_______ 。
(2)室温下,在0.5mol·L-1的纯碱溶液中加入少量水,由水电离出的c(H+)_______ (填“变大”、“变小”和“不变”。
(3)已知:H2CO3:K1=4.3×10-7,K2=5.6×10-11;HClO:K=4.0×10-8。室温下,向NaClO溶液中通入CO2,该反应的离子方程式为_______ 。
(4)甲烷燃料电池用于电解的装置如图所示,回答以下问题:

①B电极作_______ (填“正极”或“负极”);A电极发生的反应式为_______ 。
②若乙装置用于铁上镀铜,则X的化学式为_______ 。
③若乙装置用于金属铁的防护,应将金属铁置于_______ (填“M”或“N”)极。
(1)某元素基态的正三价离子的3d轨道有3个电子,该元素的元素符号是
(2)室温下,在0.5mol·L-1的纯碱溶液中加入少量水,由水电离出的c(H+)
(3)已知:H2CO3:K1=4.3×10-7,K2=5.6×10-11;HClO:K=4.0×10-8。室温下,向NaClO溶液中通入CO2,该反应的离子方程式为
(4)甲烷燃料电池用于电解的装置如图所示,回答以下问题:

①B电极作
②若乙装置用于铁上镀铜,则X的化学式为
③若乙装置用于金属铁的防护,应将金属铁置于
您最近一年使用:0次

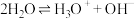 相似,液氨中也存在着微弱的电离:
相似,液氨中也存在着微弱的电离:  ,据此回答下列问题:
,据此回答下列问题: 、
、 等微粒
等微粒 ”的反应:
”的反应:

