请根据元素周期律、元素周期表的知识解决下列问题。
(1)写出以下元素的元素符号。其单质氧化性最强的元素:______ ,短周期中其单质还原性最强的元素:________ 。
(2)从原子结构的角度说明Cl的得电子能力比S强的原因:___________ 。
(3)已知33As、35Br位于同一周期,请完成下列排序。
①As3-、Br-的还原性:_______ >_______ 。
②H3AsO4、H2SO4、H3PO4的酸性:_______ >_______ >________ 。
(1)写出以下元素的元素符号。其单质氧化性最强的元素:
(2)从原子结构的角度说明Cl的得电子能力比S强的原因:
(3)已知33As、35Br位于同一周期,请完成下列排序。
①As3-、Br-的还原性:
②H3AsO4、H2SO4、H3PO4的酸性:
更新时间:2022-11-26 16:22:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】为验证卤素单质Cl2、Br2、I2氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
已知:稀溴水的颜色是黄色,浓溴水的颜色为红棕色。
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体对应的化学方程式是___________ 。
(2)B中溶液发生反应的离子方程式是___________ 。
(3)浸有NaOH溶液的棉花的作用是___________ ,反应的离子方程式为:___________ 。
(4)过程Ⅲ实验的目的是___________ 。
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________ ,现象是___________ 。
(6)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________ (填化学式)。
已知:稀溴水的颜色是黄色,浓溴水的颜色为红棕色。
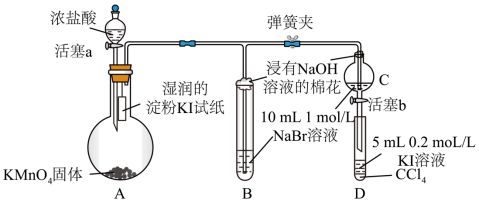
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体对应的化学方程式是
(2)B中溶液发生反应的离子方程式是
(3)浸有NaOH溶液的棉花的作用是
(4)过程Ⅲ实验的目的是
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作是
(6)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】K2Cr2O7是实验室常用试剂。回答下列问题:
(1)实验室配制一定浓度的K2Cr2O7溶液(橙红色)并标定的实验步骤如下:
步骤I.称取约5 g K2Cr2O7于烧杯中,加入少量蒸馏水溶解,配制成1 L溶液;
步骤II.移取30.00 mL已配制的K2Cr2O7溶液于碘量瓶中,加入2 g过量KI,再加20 mL20%的硫酸,摇匀( 还原为亮绿色的Cr3+),在暗处放置10 min,加水稀释,用c mol·L-1的Na2S2O3标准溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),接近终点时,加入几滴淀粉溶液,继续滴定至终点,消耗V mL Na2S2O3溶液。
还原为亮绿色的Cr3+),在暗处放置10 min,加水稀释,用c mol·L-1的Na2S2O3标准溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),接近终点时,加入几滴淀粉溶液,继续滴定至终点,消耗V mL Na2S2O3溶液。
①步骤I需要的玻璃仪器除烧杯、量筒、玻璃棒外,还需要___________ 、胶头滴管。
②K2Cr2O7溶液的物质的量浓度为___________ (用含c、V的代数式表示)。
(2)为验证Cu与Cr3+的氧化还原能力,利用下列电池装置进行实验。

①电池装置中,盐桥用于连接两电极电解质溶液,盐桥中的阴、阳离子应满足下列条件:
i.不与溶液中的物质发生化学反应;
ii.离子的电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择___________ 作为电解质。
25℃无限稀溶液中离子的电迁移率
②电流表显示电子由铜电极流向铂电极可知,盐桥中的阴离子进入___________ 电极溶液中。
③一段时间后铜电极溶液中Cu2+变为1.03 mol·L-1,铂电极溶液中Cr3+的浓度为___________ mol·L-1(假设两边溶液体积相等且不变化);铂电极的电极反应式为___________ 。
④由实验结果可确定还原性:Cu___________ (填“大于”或“小于”)Cr3+。
(1)实验室配制一定浓度的K2Cr2O7溶液(橙红色)并标定的实验步骤如下:
步骤I.称取约5 g K2Cr2O7于烧杯中,加入少量蒸馏水溶解,配制成1 L溶液;
步骤II.移取30.00 mL已配制的K2Cr2O7溶液于碘量瓶中,加入2 g过量KI,再加20 mL20%的硫酸,摇匀(
 还原为亮绿色的Cr3+),在暗处放置10 min,加水稀释,用c mol·L-1的Na2S2O3标准溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),接近终点时,加入几滴淀粉溶液,继续滴定至终点,消耗V mL Na2S2O3溶液。
还原为亮绿色的Cr3+),在暗处放置10 min,加水稀释,用c mol·L-1的Na2S2O3标准溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),接近终点时,加入几滴淀粉溶液,继续滴定至终点,消耗V mL Na2S2O3溶液。①步骤I需要的玻璃仪器除烧杯、量筒、玻璃棒外,还需要
②K2Cr2O7溶液的物质的量浓度为
(2)为验证Cu与Cr3+的氧化还原能力,利用下列电池装置进行实验。

①电池装置中,盐桥用于连接两电极电解质溶液,盐桥中的阴、阳离子应满足下列条件:
i.不与溶液中的物质发生化学反应;
ii.离子的电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
25℃无限稀溶液中离子的电迁移率
| 阳离子 | u∞/m2·s-1·V-1 | 阴离子 | u∞/m2·s-1·V-1 |
| H+ | 36.30×10-8 | OH- | 20.52×10-8 |
| K+ | 7.62×10-8 |  | 8.27×10-8 |
| Ba2+ | 6.59×10-8 | Cl- | 7.91×10-8 |
| Na+ | 5.19×10-8 |  | 7.40×10-8 |
| Li+ | 4.01×10-8 |  | 4.61×10-8 |
③一段时间后铜电极溶液中Cu2+变为1.03 mol·L-1,铂电极溶液中Cr3+的浓度为
④由实验结果可确定还原性:Cu
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室中利用如图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
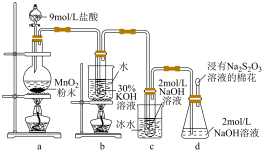
(1)盛放9mol/L盐酸的仪器名称是_______ 。
(2)b中发生化学反应的离子方程式是_______ 。
(3)d中浸有 溶液的棉花的作用是
溶液的棉花的作用是_______ 。
(4)下列相关说法不正确的是_______(填标号)。
(5)当b中试管内溶液由黄色变为无色时,反应到达终点。实际操作时,发现溶液由黄色变为紫红色甚至产生棕色沉淀影响产品纯度。针对该现象,可能混入的物质是_______ 。
(6)取少量 和NaClO溶液分别置于1号和2号试管中,滴加
和NaClO溶液分别置于1号和2号试管中,滴加 溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下
溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下 的氧化能力小于NaClO
的氧化能力小于NaClO_______ 。(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、 溶液)
溶液)
(7) 中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
_______  (填“>”或“<”)。
(填“>”或“<”)。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
(1)盛放9mol/L盐酸的仪器名称是
(2)b中发生化学反应的离子方程式是
(3)d中浸有
 溶液的棉花的作用是
溶液的棉花的作用是(4)下列相关说法不正确的是_______(填标号)。
| A.使用选择9mol/L盐酸替换浓盐酸,有利于减少HCl挥发 |
| B.控制液体滴加速率以维持氯气气流稳定,有利于减少反应过程倒吸的可能 |
C.反应结束后,b中液体经冷却结晶、过滤、冷水洗涤、干燥,可得 晶体 晶体 |
| D.增大装置c中NaOH溶液的浓度,有利于提高NaClO产率 |
(5)当b中试管内溶液由黄色变为无色时,反应到达终点。实际操作时,发现溶液由黄色变为紫红色甚至产生棕色沉淀影响产品纯度。针对该现象,可能混入的物质是
(6)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加
和NaClO溶液分别置于1号和2号试管中,滴加 溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下
溶液。两支试管均无明显现象,但试管2试管壁发烫。在上述实验基础上,设计实验进一步验证该条件下 的氧化能力小于NaClO
的氧化能力小于NaClO 溶液)
溶液)(7)
 中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
中氧原子的p轨道上的孤对电子进入氯原子的d轨道形成d-pπ键。d-pπ键长:
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图列出了①~⑩十种元素在周期表中的位置,请按题目要求回答下列问题:

请回答下列问题:
(1)请写出元素⑦在周期表中的位置___________ 。元素⑤的一种核素可以用来考古断代,该核素的符号为___________ 。
(2)写出②的最高价氧化物对应水化物的电子式___________ ,其中含有的化学键类型为___________ 。
(3)用电子式表示①、⑥形成最简单化合物的过程___________ 。
(4)⑨⑩的简单氢化物中还原性更强的是___________ (填化学式)。
(5)元素②和③相比,金属性较强的是___________ (填元素符号),下列能证明这一事实的有___________ (填序号)。
A.在化合物中②的化合价比③的低 B.②的单质能与冷水剧烈反应而③的单质不能
C.②的最高价氧化物对应水化物的碱性比③强 D.②单质的熔点比③单质的低
(6)元素④和⑧的最高价氧化物对应的水化物反应的离子方程式___________ 。

请回答下列问题:
(1)请写出元素⑦在周期表中的位置
(2)写出②的最高价氧化物对应水化物的电子式
(3)用电子式表示①、⑥形成最简单化合物的过程
(4)⑨⑩的简单氢化物中还原性更强的是
(5)元素②和③相比,金属性较强的是
A.在化合物中②的化合价比③的低 B.②的单质能与冷水剧烈反应而③的单质不能
C.②的最高价氧化物对应水化物的碱性比③强 D.②单质的熔点比③单质的低
(6)元素④和⑧的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】表是周期表中的一部分,根据A-I在周期表中的位,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是_______ ,氧化性最强的单质是_______ ,还原性最强的单质是_______ 。
(2)最高价氧化物的水化物碱性最强的是_______ ,酸性最强的是_______ ,呈两性的是_______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的是_______ 。
(4)在B、C、D、E、F、G、H中,原子半径最大的是_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
 | A | |||||||
 | D | E | G | I | ||||
 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的是
(4)在B、C、D、E、F、G、H中,原子半径最大的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素周期表是学习化学的基础,元素周期表的一部分如图。

请回答下列问题:
(1)比较①②形成最简单气态氢化物的稳定性_______ >_______ (填化学式)。
(2)③、⑤、⑥三种元素对应的简单离子半径由大到小的顺序为_______ (用元素的离子符号表示)。
(3)写出①的最高价氧化物的电子式:_______ 。
(4)④⑤的最高价氧化物对应的水化物反应的化学方程式为_______ 。
(5)下列各项能说明非金属性⑥<⑦的是_______(填字母标号)。

请回答下列问题:
(1)比较①②形成最简单气态氢化物的稳定性
(2)③、⑤、⑥三种元素对应的简单离子半径由大到小的顺序为
(3)写出①的最高价氧化物的电子式:
(4)④⑤的最高价氧化物对应的水化物反应的化学方程式为
(5)下列各项能说明非金属性⑥<⑦的是_______(填字母标号)。
| A.含氧酸的酸性;⑥<⑦ |
| B.⑦的单质能与⑥的最简单气态氢化物反应,置换出⑥的单质 |
| C.单质与Fe发生化合反应,生成物中Fe的化合价:⑥<⑦ |
| D.单质的熔、沸点:⑥>⑦ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
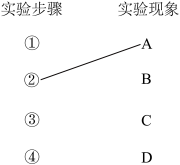
【推荐1】某小组研究第3周期元素性质的递变规律,设计了如下实验,并记录了实验现象:
(1)补齐实验步骤与实验现象之间的连线___________ 。
(2)由上述实验可知Na、Mg、Al三种元素原子失电子能力(金属性)依次_______ (填“增强”或“减弱”)。从原子结构的角度解释原因____________ 。
(3)比较第3周期中硫与氯两种元素原子得电子能力(非金属性)的相对强弱。
①甲同学设计的下列方法可行的是_______ 。
A.比较气态氢化物的稳定性 B.比较盐酸与硫酸的酸性 C.比较单质与酸反应置换出氢气的难易程度
②乙同学设计将氯气通入硫化钠溶液中,观察是否有淡黄色沉淀生成。这一实验的设计思路是通过比较________ ,推知元素原子得电子能力的相对强弱。
(4)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是_____ 。
A.失电子能力:Rb>Na B.碱性:NaOH>RbOH C.Rb比Na更容易与氧气发生反应 D.Rb不易与水反应放出H2
| 实验步骤 | 实验现象 |
| ①将一小块钠放入滴有酚酞的冷水中 | A.有气体产生,溶液变成浅红色 |
| ②将用砂纸打磨过的镁条放入沸水中,再向其中滴加少量酚酞溶液 | B.浮在水面上,熔成小球,做不定向运动,随后消失,溶液变为红色 |
| ③将镁条放入稀盐酸中 | C.反应较快,产生无色气体 |
| ④将铝条放入稀盐酸中 | D.反应剧烈,迅速产生大量无色气体 |

(2)由上述实验可知Na、Mg、Al三种元素原子失电子能力(金属性)依次
(3)比较第3周期中硫与氯两种元素原子得电子能力(非金属性)的相对强弱。
①甲同学设计的下列方法可行的是
A.比较气态氢化物的稳定性 B.比较盐酸与硫酸的酸性 C.比较单质与酸反应置换出氢气的难易程度
②乙同学设计将氯气通入硫化钠溶液中,观察是否有淡黄色沉淀生成。这一实验的设计思路是通过比较
(4)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是
A.失电子能力:Rb>Na B.碱性:NaOH>RbOH C.Rb比Na更容易与氧气发生反应 D.Rb不易与水反应放出H2
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国科学家受中医启发,发现As2O3(俗称砒霜)对白血病有疗效。氮、磷、砷(As)是VA族、第二至第四周期的元素,这些元素的化合物在研究和生产中有许多重要用途。

完成下列填空:
(1)As原子最外层电子的轨道表示式为_____________ ;砷蒸气的分子式:As4,其分子结构与白磷(P4)相似,也是正四面体,则As4中砷砷键的键角是__________ 。
(2)P的非金属性比As强,从原子结构的角度解释其原因_______ ;如图是元素周期表的一部分,请推测砷的单质或其化合物可能具有的性质_______________ (写出两条即可)
(3)NH4NO3可做化肥,但易爆,300℃发生爆炸:2NH4NO3→2N2↑+O2↑+4H2O。每生成2molN2,反应中转移的电子为_____ mol,氧化产物与还原产物的质量之比为_____ 。
(4)发电厂常用氨气吸收烟气中的CO2。常温下,当CO2不断通入pH=11的氨水中时会产生微量的新离子:NH2COO-。
(i)写出NH2COO-的电子式___________ 。
(ii)计算原氨水中c(NH4+)=_______ mol/L。

完成下列填空:
(1)As原子最外层电子的轨道表示式为
(2)P的非金属性比As强,从原子结构的角度解释其原因
(3)NH4NO3可做化肥,但易爆,300℃发生爆炸:2NH4NO3→2N2↑+O2↑+4H2O。每生成2molN2,反应中转移的电子为
(4)发电厂常用氨气吸收烟气中的CO2。常温下,当CO2不断通入pH=11的氨水中时会产生微量的新离子:NH2COO-。
(i)写出NH2COO-的电子式
(ii)计算原氨水中c(NH4+)=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表列出了A~H8种元素在周期表中的位置:
(1)8种元素中化学性质最不活泼的是______ (填元素符号);最高价氧化物对应的水化物的酸性最强的是______ (填化学式)。
(2)元素D、E、F的简单离子的半径从大到小的顺序为______ (填离子符号)。
(3)元素D的最低价的氢化物与G的单质发生反应的化学方程式为____________ 。
(4)写出元素A、C形成的化学式为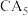 的电子式:
的电子式:______ 。
(5)镓(Ga)和同族的铝具有相似的化学性质,请写出镓与沸水反应的化学方程式:__________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | B | C | D | |||||
3 | E | F | G | H |
(2)元素D、E、F的简单离子的半径从大到小的顺序为
(3)元素D的最低价的氢化物与G的单质发生反应的化学方程式为
(4)写出元素A、C形成的化学式为
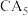 的电子式:
的电子式:(5)镓(Ga)和同族的铝具有相似的化学性质,请写出镓与沸水反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】I.元素X、Y、Z、T部分元素性质如表:
(1)元素Y与元素Z相比,金属性较强的是____ (填元素符号),下列表述中能证明这一事实的是____ (填字母)。
A.Y元素的单质的熔点比Z元素的单质的低
B.Y元素的最高正化合价比Z元素的低
C.Y元素的单质与水反应比Z元素的单质与水反应剧烈
D.Y元素的最高价氧化物对应的水化物的碱性比Z元素的强
(2)能用于比较T和X得电子能力强弱的是____ (填字母)。
(3)X氢化物曾用于刻蚀玻璃,相应的方程式为____ 。
II.利用如图装置来验证同主族元素非金属性的变化规律:

(4)仪器A的名称为____ ,D的作用是___ 。
(5)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置B中所装药品为___ ,装置C中的实验现象为有淡黄色沉淀生成,则反应的离子方程式为____ 。
(6)要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,应在B、D之间增加一个盛有足量___ 的洗气装置。
| 元素 | 元素性质与原子(或分子)结构 |
| X | 单质与H2暗处能剧烈化合并发生爆炸 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小的 |
| T | 常温下单质由双原子分子构成,1个分子有34个电子 |
A.Y元素的单质的熔点比Z元素的单质的低
B.Y元素的最高正化合价比Z元素的低
C.Y元素的单质与水反应比Z元素的单质与水反应剧烈
D.Y元素的最高价氧化物对应的水化物的碱性比Z元素的强
(2)能用于比较T和X得电子能力强弱的是
| A.X原子的电子层数比T的少 |
| B.X的单质的颜色比T的浅 |
| C.X的气态氢化物比T的气态氢化物稳定 |
| D.X的单质能将T从NaX的溶液中置换出来 |
II.利用如图装置来验证同主族元素非金属性的变化规律:

(4)仪器A的名称为
(5)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置B中所装药品为
(6)要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,应在B、D之间增加一个盛有足量
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请回答下列问题:
(1)属于卤族元素的有_______ (填元素符号,下同);属于碱金属元素的有_______ 。
(2)②③原子结构的相同点是_______ 。
(3)画出元素④的原子结构示意图:_______ ;元素④与⑤同属于_______ 族;预测它们单质的化学性质的相似性是_______ 。
(4)元素⑥与⑦的原子最外层电子数都为_______ ;单质的氧化性:⑥_______ (填“>”或“<”)⑦,其依据是_______ 。
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:_______ (任写一种)。
| 周期 | IA | 0 | ||||||
| 一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 二 | ⑥ | |||||||
| 三 | ② | ④ | ⑦ | ⑧ | ||||
| 四 | ③ | ⑤ | ⑨ |
(1)属于卤族元素的有
(2)②③原子结构的相同点是
(3)画出元素④的原子结构示意图:
(4)元素⑥与⑦的原子最外层电子数都为
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,其中每个数字序号代表短周期的一种元素。

请回答下列问题:
(1)元素⑥在元素周期表中的位置为第___________ 周期第___________ 族。
(2)表中金属性最强的元素是___________ (填元素符号)。
(3)②③⑤三种元素按原子半径由大到小的顺序排列为___________ (用元素符号表示)。
(4)元素③的最高价氧化物对应的水化物的化学式为___________ 。
(5)元素④和元素⑤各自的最高价氧化物对应的水化物反应的离子方程式是___________ 。

请回答下列问题:
(1)元素⑥在元素周期表中的位置为第
(2)表中金属性最强的元素是
(3)②③⑤三种元素按原子半径由大到小的顺序排列为
(4)元素③的最高价氧化物对应的水化物的化学式为
(5)元素④和元素⑤各自的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次



