利用丙烷制备丙烯的机理如图所示,下列说法不正确的是
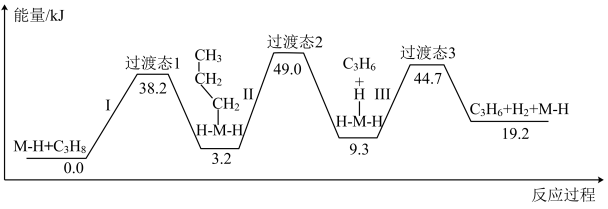

| A.反应的快慢主要取决于步骤Ⅱ | B.升高温度有利于提高丙烷转化率 |
| C.反应过程中碳的成键总数不变 | D. 为该反应的催化剂 为该反应的催化剂 |
更新时间:2022-12-06 11:31:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于热化学反应的描述正确的是
| A.已知稀溶液中,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ•mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1mol液态水时放出57.3kJ的热量 |
| B.H2(g)的燃烧热为285.8kJ•mol-1,则反应2H2O(l)=2H2(g)+O2(g)的△H=+571.6kJ•mol-1 |
| C.放热反应比吸热反应容易发生 |
| D.1mol丙烷燃烧生成水和二氧化碳所放出的热量是丙烷的燃烧热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】科学家用计算机模拟了乙炔在钯表面催化加氢的反应机理,单个乙炔分子在催化剂表面的反应历程如图所示,吸附在钯表面的物种用*标注。下列叙述错误的是


| A.乙炔加氢是放热反应 |
B.该历程中最小能垒的化学方程式为 +H*= +H*=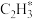 |
| C.该反应的热化学方程式为C2H2(g)+H2(g)=C2H4(g) △H=-1.02NAeV·mol-1 |
| D.整个反应的速率由I→II步骤决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】工业制硫酸的接触室中发生反应: 。该反应在500℃和催化剂存在下进行,下列有关说法正确的是
。该反应在500℃和催化剂存在下进行,下列有关说法正确的是
 。该反应在500℃和催化剂存在下进行,下列有关说法正确的是
。该反应在500℃和催化剂存在下进行,下列有关说法正确的是| A.如果使氧气过量,并给足够时间让反应充分进行,SO2可以全部转化为SO3 |
| B.该反应的平衡常数(K)随体系压强的增加而增大 |
| C.该反应选择在500℃和催化剂存在下进行,因此该反应是吸热反应 |
| D.反应达到化学平衡后,只改变温度,化学平衡一定会被破坏 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.加入合适的催化剂能降低反应活化能,从而改变反应的焓变 |
B.在恒容密闭容器中发生N2(g)+3H2(g) 2NH3(g)△H<0,达到平衡后升高温度可提高N2转化率 2NH3(g)△H<0,达到平衡后升高温度可提高N2转化率 |
C.某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s)△H>0,当容器中气体压强不变时,该反应达到平衡状态 Z(g)+W(s)△H>0,当容器中气体压强不变时,该反应达到平衡状态 |
D.对于可逆反应A(g) B(g)+C(g),增大压强,正反应速率和逆反应速率都增大,并且正反应速率增大的程度大于逆反应速率增大的程度 B(g)+C(g),增大压强,正反应速率和逆反应速率都增大,并且正反应速率增大的程度大于逆反应速率增大的程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在强碱中氢氧化铁可被一些氧化剂氧化为高铁酸根离子(FeO ),FeO
),FeO 在酸性条件下氧化性极强且不稳定, Fe3O4 中铁元素有2、3价;H2O2可在催化剂Fe2O3或Fe3O4作用下产生OH,OH能将烟气中的NO、SO2氧化。OH产生机理如下:
在酸性条件下氧化性极强且不稳定, Fe3O4 中铁元素有2、3价;H2O2可在催化剂Fe2O3或Fe3O4作用下产生OH,OH能将烟气中的NO、SO2氧化。OH产生机理如下:
反应Ⅰ: Fe3 H2O2 = Fe2 + OOH H (慢反应)
反应Ⅱ:Fe2 H2O2 = Fe3 OH OH- (快反应)
对于H2O2 脱除SO2反应:SO2 g H2O2 l =H2SO4 l ,下列有关说法不正确 的是
 ),FeO
),FeO 在酸性条件下氧化性极强且不稳定, Fe3O4 中铁元素有2、3价;H2O2可在催化剂Fe2O3或Fe3O4作用下产生OH,OH能将烟气中的NO、SO2氧化。OH产生机理如下:
在酸性条件下氧化性极强且不稳定, Fe3O4 中铁元素有2、3价;H2O2可在催化剂Fe2O3或Fe3O4作用下产生OH,OH能将烟气中的NO、SO2氧化。OH产生机理如下: 反应Ⅰ: Fe3 H2O2 = Fe2 + OOH H (慢反应)
反应Ⅱ:Fe2 H2O2 = Fe3 OH OH- (快反应)
对于H2O2 脱除SO2反应:SO2 g H2O2 l =H2SO4 l ,下列有关说法
| A.该反应能自发进行,则该反应的ΔH 0 |
| B.加入催化剂 Fe2O3,可提高SO2 的脱除效率 |
| C.向固定容积的反应体系中充入氦气,反应速率加快 |
| D.与Fe2O3作催化剂相比,相同条件下Fe3O4作催化剂时SO2 脱除效率可能更高 |
您最近一年使用:0次

 的反应
的反应

