硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:

回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______ 。
(2)为了提高锌的浸取效果,可采取的措施有_______ 。
(3)加入物质X调节溶液pH=5,最适宜使用的X是_______ (填标号)。
A.NH3·H2O B.Ca(OH)2 C.NaOH
滤渣①的主要成分是Fe(OH)3、_______ 、_______ 。
(4)向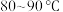 的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为
的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为_______ 。
(5)滤液②中加入锌粉的目的是_______ 。
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是_______ 。

回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为
(2)为了提高锌的浸取效果,可采取的措施有
(3)加入物质X调节溶液pH=5,最适宜使用的X是
A.NH3·H2O B.Ca(OH)2 C.NaOH
滤渣①的主要成分是Fe(OH)3、
(4)向
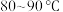 的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为
的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为(5)滤液②中加入锌粉的目的是
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是
更新时间:2022-10-02 17:20:05
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】从钒铬锰矿渣(主要成分为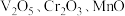 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
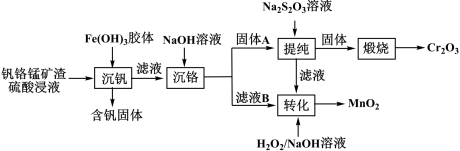
已知: 较大时,二价锰
较大时,二价锰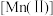 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:
(1) 元素在周期表中的位置是
元素在周期表中的位置是___________ 。
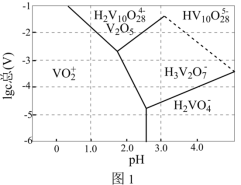
(2)常温下,各种形态五价钒粒子总浓度的对数 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中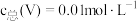 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为___________ (填化学式)。
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为_____ (填标号);
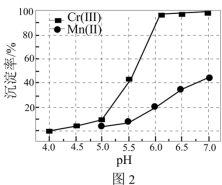
a.4.0 b.5.0 c.6.0
在该条件下滤液B中
______  [
[ 近似为
近似为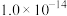 ,
, 的
的 近似为
近似为 ]。
]。
(4)“转化”过程中生成 的离子方程式为
的离子方程式为_________ 。
(5)“提纯”过程中 的作用为
的作用为________ 。
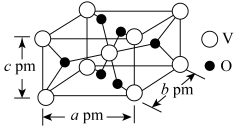
(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为_______ g•cm-3 (列出计算式即可)。
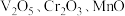 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
已知:
 较大时,二价锰
较大时,二价锰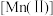 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:(1)
 元素在周期表中的位置是
元素在周期表中的位置是(2)常温下,各种形态五价钒粒子总浓度的对数
 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中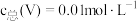 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为

a.4.0 b.5.0 c.6.0
在该条件下滤液B中

 [
[ 近似为
近似为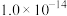 ,
, 的
的 近似为
近似为 ]。
]。(4)“转化”过程中生成
 的离子方程式为
的离子方程式为(5)“提纯”过程中
 的作用为
的作用为(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】某研究小组欲从含少量 、
、 、
、 、
、 的
的 溶液中制纯净的无水
溶液中制纯净的无水 固体,设计的流程如下:
固体,设计的流程如下:

常温下,几种金属离子沉淀完全(离子浓度小于 )时的
)时的 如表所示:
如表所示:
回答下列问题:
(1)实验室用 配制
配制 溶液的方法是
溶液的方法是___________
(2)加入 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ ;“过滤2”得到的沉淀是___________ (填化学式)。
(3)常温时,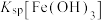 、
、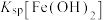 、
、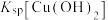 、
、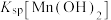 中数值最大的为
中数值最大的为___________ ;第一次“调pH”的最小值为___________ ,第二次“调pH”的最小值为___________ 。已知常温下, 的
的 ,
, 的氨水的pH=
的氨水的pH=___________ (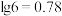 )。
)。
(4)“一系列操作”包括___________ 、洗涤、干燥;由 制无水
制无水 的操作是
的操作是___________ 。
 、
、 、
、 、
、 的
的 溶液中制纯净的无水
溶液中制纯净的无水 固体,设计的流程如下:
固体,设计的流程如下:
常温下,几种金属离子沉淀完全(离子浓度小于
 )时的
)时的 如表所示:
如表所示:| 金属离子 |  |  |  |  |
沉淀完全时的 | 2.8 | 8.3 | 10.1 | 6.7 |
(1)实验室用
 配制
配制 溶液的方法是
溶液的方法是(2)加入
 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)常温时,
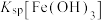 、
、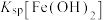 、
、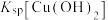 、
、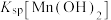 中数值最大的为
中数值最大的为 的
的 ,
, 的氨水的pH=
的氨水的pH=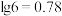 )。
)。(4)“一系列操作”包括
 制无水
制无水 的操作是
的操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料:铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、 、FeO、
、FeO、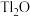 等)中提炼,具体工艺流程如图。
等)中提炼,具体工艺流程如图。

已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂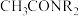 的二乙苯溶液,萃取过程的反应原理为
的二乙苯溶液,萃取过程的反应原理为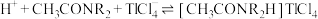 。
。
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供 ,另一作用为
,另一作用为_______ 。
(2)在实验室中,“萃取”过程使用的玻璃仪器有_______ ,用平衡移动解释“反萃取”过程的原理和目的_______ 。
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为_______ ,为提高经济效益充分利用原料,该反应的滤液可加入_______ 步骤循环使用最合适。
(4)Tl对人体毒性很大,难溶盐 可通过离子交换治疗
可通过离子交换治疗 中毒,将其转化为沉淀同时生成
中毒,将其转化为沉淀同时生成 溶液,写出治疗
溶液,写出治疗 中毒的离子方程式:
中毒的离子方程式:_______ 。
 、FeO、
、FeO、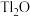 等)中提炼,具体工艺流程如图。
等)中提炼,具体工艺流程如图。
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂
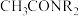 的二乙苯溶液,萃取过程的反应原理为
的二乙苯溶液,萃取过程的反应原理为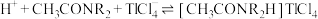 。
。回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供
 ,另一作用为
,另一作用为(2)在实验室中,“萃取”过程使用的玻璃仪器有
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为
(4)Tl对人体毒性很大,难溶盐
 可通过离子交换治疗
可通过离子交换治疗 中毒,将其转化为沉淀同时生成
中毒,将其转化为沉淀同时生成 溶液,写出治疗
溶液,写出治疗 中毒的离子方程式:
中毒的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钴在现代有着广泛应用,如草酸钴可作指示剂与催化剂,氯化钴是一种饲料营养强化剂。利用水钴矿(主要成分为: Co2O3, 含少量Fe2O3、Al2O3、 MnO2、MgO、CaO、SiO2等)可以制取草酸钴晶体和氯化钴晶体,依据如图制备流程回答下列问题:

已知:①氧化性: Co3+>ClO 。
。
②沉淀I、沉淀II中都只含有两种沉淀。
③以氢氧化物形式沉淀时溶液的pH见表:
(1)通过增大接触面积的形式可以加快水钴矿“浸出”速率,可采取的措施是将水钴矿粉碎和_______ , 浸出过程中加入Na2SO3的作用是_______ 。
(2)加入NaClO3的作用是为了氧化Fe2+,反应的离子方程式是_______ ,后续加入Na2CO3调pH,其值不能超过_______ 。
(3)NaF溶液可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0 ×10-5mol/L,则c(Mg2+)=_______ mol/L。[已知Ksp (CaF2)=a ×10-10, Ksp (MgF2)=b ×10-11]
(4)加入萃取剂的目的是_______ 。
(5)操作I包括:向水层加入浓盐酸调整pH为2~3,_______ ,过滤、 洗涤、减压烘干等过程。
(6)为测定获得草酸钴晶体(CoC2O4·2H2O)的纯度,现称取mg样品,将其用适当试剂转化为草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用c mol/L高锰酸钾溶液滴定,达到滴定终点时,共用去高锰酸钾溶液V mL,该产品的纯度为_______ ;某兴趣小组测得产品中CoC2O4·2H2O的含量为100.6%。若滴定时实验操作无误,造成该结果可能的原因是_______ 。

已知:①氧化性: Co3+>ClO
 。
。②沉淀I、沉淀II中都只含有两种沉淀。
③以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 | Co(OH)2 |
| 开始沉淀 | 2.7 | 4.0 | 7.6 | 7.7 | 9.6 | 7.5 |
| 完全沉淀 | 3.7 | 5.2 | 9.6 | 9.8 | 11.1 | 9.2 |
(2)加入NaClO3的作用是为了氧化Fe2+,反应的离子方程式是
(3)NaF溶液可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0 ×10-5mol/L,则c(Mg2+)=
(4)加入萃取剂的目的是
(5)操作I包括:向水层加入浓盐酸调整pH为2~3,
(6)为测定获得草酸钴晶体(CoC2O4·2H2O)的纯度,现称取mg样品,将其用适当试剂转化为草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用c mol/L高锰酸钾溶液滴定,达到滴定终点时,共用去高锰酸钾溶液V mL,该产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
I.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II.向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III.向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV.……
(1)步骤I中Al与NaOH溶液的反应化学方程式为___________ ;另一种与NaOH溶液反应的氧化物是___________ ;该氧化物属于___________ (填“碱性”,“酸性”或“两性氧化物”)。
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在___________ (填离子符号);用离子方程式解释其可能的原因___________ ;取该硫酸亚铁滤液滴加NaOH溶液的现象是___________ 。
(3)步骤II所得硫酸亚铁滤液经进一步处理可制得Na2FeO4,流程如下:

该流程有关反应中属于氧化剂的有___________ 。
(4)步骤III获得CuSO4溶液的离子方程式为___________ 。
I.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II.向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III.向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV.……
(1)步骤I中Al与NaOH溶液的反应化学方程式为
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在
(3)步骤II所得硫酸亚铁滤液经进一步处理可制得Na2FeO4,流程如下:

该流程有关反应中属于氧化剂的有
(4)步骤III获得CuSO4溶液的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
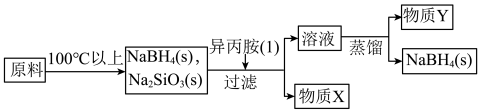
【推荐3】硼氢化钠(NaBH4)在有机合成中被称为“万能还原剂”,它的特点是性能稳定,还原时有选择性。采用NaBO2、SiO2、Na、H2为原料制备NaBH4的流程如图所示。
已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33 ℃)。
(1)NaBH4中含有的化学键类型为____________________ 。
(2)制取NaBH4的化学方程式为_________________________________________________ ;
在该反应加料之前,需要将反应容器加热至100 ℃以上并通入氩气,通入氩气的目的是__ 。
(3)在强碱性条件下,常用NaBH4处理含Au3+的废液生成单质Au,已知,反应后硼元素以BO2−形式存在,反应前后硼元素化合价不变,且无气体生成,则发生反应的离子方程式为_______ 。
(4)物质X的化学式为__________ ;以上流程中可以循环使用的物质是_________ 。
已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33 ℃)。

(1)NaBH4中含有的化学键类型为
(2)制取NaBH4的化学方程式为
在该反应加料之前,需要将反应容器加热至100 ℃以上并通入氩气,通入氩气的目的是
(3)在强碱性条件下,常用NaBH4处理含Au3+的废液生成单质Au,已知,反应后硼元素以BO2−形式存在,反应前后硼元素化合价不变,且无气体生成,则发生反应的离子方程式为
(4)物质X的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
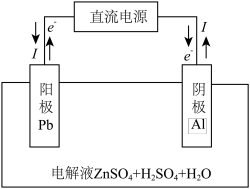
【推荐1】以菱锌矿(主要含有ZnCO3,另含有少量CaO、Fe2O3、FeO、CoO、CuO、SiO2等)为原料电解制Zn的流程如图:
(1)“酸浸”时为提高锌的浸出率,可采取的措施有___________ (写出一种即可)。
(2)“调pH过滤”中,物质X最适宜选择___________ (填标号)。
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为___________ 。若反应结束时,溶液pH为5,则残留的c(Fe3+)=___________ mol·L-l。
(4)H2O2是常见绿色氧化剂,原因是___________ 。
(5)“脱钙镁过滤”后,溶液中 =
=___________ 。
(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为___________ 。
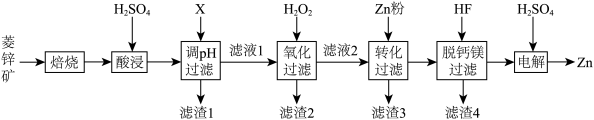
| 物质 | Fe(OH)3 | Zn(OH)2 | MgF2 | CaF2 |
| Ksp | 2.7×10-39 | 1.3×10-17 | 5.2×10-11 | 3.9×10-9 |
(1)“酸浸”时为提高锌的浸出率,可采取的措施有
(2)“调pH过滤”中,物质X最适宜选择
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为
(4)H2O2是常见绿色氧化剂,原因是
(5)“脱钙镁过滤”后,溶液中
 =
=(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
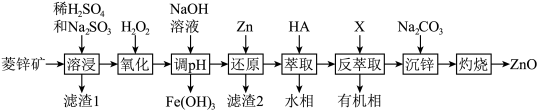
【推荐2】ZnO是一种难溶于水的白色固体,在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上由菱锌矿(主要成分为ZnCO3、ZnO,还含有少量Ni2O3、FeO、MgCO3、PbO2等杂质)制备ZnO的工艺流程如图所示:
②“溶浸”后的溶液所含金属离子主要有:Zn2+、Fe2+、Ni2+、Mg2+;
③氧化性顺序:Ni2+>Zn2+。
回答下列问题:
(1)基态Zn原子核外电子排布式为___________ 。
(2)滤渣1的化学式是___________ ,“溶浸”过程中Ni2O3发生反应的离子方程式是___________ 。
(3)已知“氧化”后溶液中c(Zn2+)=1.2mol·L-1,“调pH”的pH范围是___________ (保留两位有效数字)。(已知:溶液中离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。)“还原”时加入锌粉的目的是___________ 。
(4)有机萃取剂HA与ZnSO4反应的化学方程式为2HA+ZnSO4 ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是
ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是___________ 。
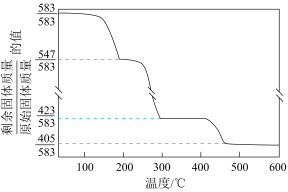
(5)在“沉锌”与“灼烧”之间进行的操作是___________ ,“沉锌”得到碱式碳酸锌[化学式为2ZnCO3·3Zn(OH)2·2H2O],碱式碳酸锌升温过程中固体的质量变化如图所示。350℃时,剩余固体中已不含碳元素,则剩余固体的成分是___________ (填化学式)。
②“溶浸”后的溶液所含金属离子主要有:Zn2+、Fe2+、Ni2+、Mg2+;
③氧化性顺序:Ni2+>Zn2+。
回答下列问题:
(1)基态Zn原子核外电子排布式为
(2)滤渣1的化学式是
(3)已知“氧化”后溶液中c(Zn2+)=1.2mol·L-1,“调pH”的pH范围是
(4)有机萃取剂HA与ZnSO4反应的化学方程式为2HA+ZnSO4
 ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是
ZnA2+H2SO4,则“反萃取”时加入试剂X的化学式是(5)在“沉锌”与“灼烧”之间进行的操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】活性氧化锌是一种多功能性的新型无机材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
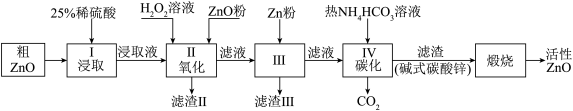
已知各相关氢氧化物沉淀pH范围如下表所示:
完成下列填空:
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要_____ (选填编号)
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤II中加入H2O2溶液的作用是_________________________ (用离子方程式表示);
(3)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是_______________________ 。
(4)步骤III中加入Zn粉的作用是:①__________________ ;②进一步调节溶液pH。
(5)碱式碳酸锌[Zn2(OH)2 CO3]煅烧的化学方程式为________________________________ 。
(6)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
① 取1.000g活性氧化锌,用15.00mL 1.000mol·L-1 硫酸溶液完全溶解,滴入几滴甲基橙。② 用浓度为0.5000mol·L-1 的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL。判断滴定终点的方法是________ ;所得活性氧化锌的纯度为________ (相对原子质量 O-16 Zn-65 )。

已知各相关氢氧化物沉淀pH范围如下表所示:
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
完成下列填空:
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤II中加入H2O2溶液的作用是
(3)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是
(4)步骤III中加入Zn粉的作用是:①
(5)碱式碳酸锌[Zn2(OH)2 CO3]煅烧的化学方程式为
(6)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
① 取1.000g活性氧化锌,用15.00mL 1.000mol·L-1 硫酸溶液完全溶解,滴入几滴甲基橙。② 用浓度为0.5000mol·L-1 的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL。判断滴定终点的方法是
您最近一年使用:0次



