德国化学家凯库勒认为:苯分子是由 6 个碳原子以单双键相互交替结合而成的环状结构。 为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案。
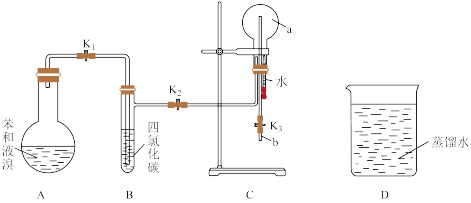
①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在 A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待 C 中烧瓶收集满气体后,将导管 b 的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象回答下列问题。
(1)仪器 a 的名称是_______ ,A中所发生的有机反应的化学方程式为_______ 。
(2)能证明凯库勒观点错误的实验现象是_______ 。
(3)装置 B 的作用是_______ 。
(4)反应完毕后,将装置 A 内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯:①蒸馏;②水洗;③用干燥剂干燥;④用 10%NaOH 溶液洗;⑤水洗 ,正确的操作顺序是_______ ,得到纯净的溴苯为_______ 色有特殊气味的液体。
(5)上题中加入 10%NaOH 溶液的目的是_______ 。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在 A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待 C 中烧瓶收集满气体后,将导管 b 的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象回答下列问题。
(1)仪器 a 的名称是
(2)能证明凯库勒观点错误的实验现象是
(3)装置 B 的作用是
(4)反应完毕后,将装置 A 内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯:①蒸馏;②水洗;③用干燥剂干燥;④用 10%NaOH 溶液洗;⑤水洗 ,正确的操作顺序是
(5)上题中加入 10%NaOH 溶液的目的是
更新时间:2022-10-23 16:28:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硝基苯是重要的有机中间体。实验室制取少量硝基苯的装置如下图所示。根据题意完成下列填空:
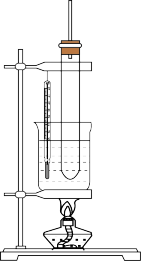
(1)写出制取硝基苯的化学方程式______ 。
(2)该实验先在大试管中配制混合酸,配制混合酸的注意事项是:____ 并及时冷却;混合酸冷却后才能加入苯的可能原因是:_______ 。
(3)大试管上方的长玻璃导管的作用是:______ 。
(4)用胶头滴管吸取少许反应液,滴到水中,当观察到油珠下沉时,表示硝基苯已生成。这样操作利用了硝基苯的哪些性质:______ 。
(5)将除去混酸后的粗硝基苯先用冷水洗涤,再用10%碳酸钠溶液洗至不显酸性,最后用水洗至中性。洗涤和分离粗硝基苯的仪器是______ (填仪器名称)。
(6)经上述洗涤的硝基苯中仍含少量的间二硝基苯、苯杂质,依据下面物质性质表,回答以下问题:继续提纯硝基苯的最佳方法是_____ ,选择该提纯方法的理由____ 。硝基苯有毒,如果少量的液体溅在皮肤上,应用______ 擦洗。
a.苯 b.酒精 c.硫酸 d.水

(1)写出制取硝基苯的化学方程式
(2)该实验先在大试管中配制混合酸,配制混合酸的注意事项是:
(3)大试管上方的长玻璃导管的作用是:
(4)用胶头滴管吸取少许反应液,滴到水中,当观察到油珠下沉时,表示硝基苯已生成。这样操作利用了硝基苯的哪些性质:
(5)将除去混酸后的粗硝基苯先用冷水洗涤,再用10%碳酸钠溶液洗至不显酸性,最后用水洗至中性。洗涤和分离粗硝基苯的仪器是
(6)经上述洗涤的硝基苯中仍含少量的间二硝基苯、苯杂质,依据下面物质性质表,回答以下问题:继续提纯硝基苯的最佳方法是
a.苯 b.酒精 c.硫酸 d.水
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g/ml) | 溶解性 |
| 苯 | 5.5 | 80 | 0.8765 | 难溶于水,易溶于有机溶剂 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水,易溶于乙醇、苯等有机溶剂 |
| 间二硝基苯 | 89 | 301 | 1.57 | 难溶于水,易溶于乙醇、苯等有机溶剂 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某实验小组制备溴苯并分离提纯溴苯,其制备溴苯的实验装置如图所示,回答下列问题:
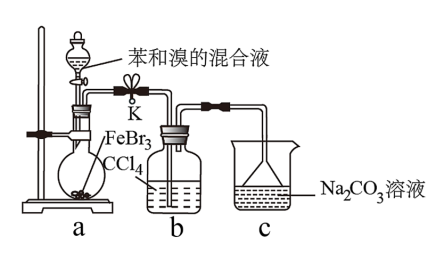
Ⅰ.制备溴苯:
(1)盛放苯和溴的仪器名称为_______
(2)在该反应中催化剂是_______ ;实验中装置b吸收挥发出的_______ 和苯,液体颜色逐渐变为_______ 。
(3)装置c中倒扣的漏斗作用是_______ 。
(4)写出圆底烧瓶中苯发生反应的化学方程式_______ 。
Ⅱ.分离提纯溴苯:
(5)反应后的混合液加入NaOH溶液振荡、静置、_______ (填写实验操作方法),在有机层中加干燥剂,最后蒸馏分离出沸点较低的苯,得到溴苯。

Ⅰ.制备溴苯:
(1)盛放苯和溴的仪器名称为
(2)在该反应中催化剂是
(3)装置c中倒扣的漏斗作用是
(4)写出圆底烧瓶中苯发生反应的化学方程式
Ⅱ.分离提纯溴苯:
(5)反应后的混合液加入NaOH溶液振荡、静置、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室制备硝基苯的实验装置如图所示,主要步骤如下:
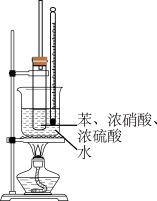
Ⅰ.配制一定比例的浓硫酸与浓硝酸的混合酸,加入试管中;
Ⅱ.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
Ⅲ.在50~60℃下发生反应,直至反应结束;
Ⅳ.将粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤并用无水CaCl2进行干燥;
Ⅴ.对用无水CaCl2干燥后的粗硝基苯进行“某种操作”,得到纯净的硝基苯。
回答下列问题:
(1)步骤I中配制混合酸时的加入次序是_______ 中,并不断搅拌。
A.“浓硫酸加入浓硝酸” B.“浓硝酸加入到浓硫酸”
(2)试管中发生反应的化学方程式为_______ ,该反应中浓硫酸的作用是_______ 。
(3)经步骤Ⅴ后得到纯净的硝基苯:
①但在实验过程中得到的硝基苯却为黄色液体,可能的原因是_______ 。
②硝基苯有毒,与人体皮肤接触或蒸气被人体吸收,都能引起中毒。洗去人体皮肤上的硝基苯的常用安全试剂是_______ (填化学名称)。
③“某种操作”指的是_______ 。
(4)若起始时加入的苯的质量为9.75g,混合酸足量,经过上述步骤后,最后得到纯净的硝基苯的质量为12.3 g,则产率为_______ 。

Ⅰ.配制一定比例的浓硫酸与浓硝酸的混合酸,加入试管中;
Ⅱ.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
Ⅲ.在50~60℃下发生反应,直至反应结束;
Ⅳ.将粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤并用无水CaCl2进行干燥;
Ⅴ.对用无水CaCl2干燥后的粗硝基苯进行“某种操作”,得到纯净的硝基苯。
回答下列问题:
(1)步骤I中配制混合酸时的加入次序是
A.“浓硫酸加入浓硝酸” B.“浓硝酸加入到浓硫酸”
(2)试管中发生反应的化学方程式为
(3)经步骤Ⅴ后得到纯净的硝基苯:
①但在实验过程中得到的硝基苯却为黄色液体,可能的原因是
②硝基苯有毒,与人体皮肤接触或蒸气被人体吸收,都能引起中毒。洗去人体皮肤上的硝基苯的常用安全试剂是
③“某种操作”指的是
(4)若起始时加入的苯的质量为9.75g,混合酸足量,经过上述步骤后,最后得到纯净的硝基苯的质量为12.3 g,则产率为
您最近一年使用:0次
【推荐1】以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取精银、Mn及MnO2的一种流程示意图如下。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是_______ 。
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有_______ 。
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整:_______ 。
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:_______ 。
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:
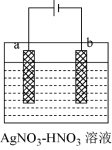
①_______ 极为“粗银电极”(填“a”或“b”)。
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为_______ ;当电路中通过0.025NA电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为_______ mL(保留三位有效数字)。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以
 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整:
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:

①
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】实验室模拟“镁法工业烟气脱硫”并制备MgSO4∙H2O,其实验过程可表示如下:

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成 。
。
①“吸收”过程中,发生的主要反应的化学方程式为___________ ;
②64gSO2在标准状况下的体积约为___________ L;
③NaOH溶液也可以用于捕集SO2,配制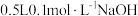 溶液,需NaOH
溶液,需NaOH___________ g;
(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为___________ L;
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,___________ (填写操作步骤),洗涤,干燥,制得MgSO4∙H2O晶体;
(4)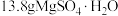 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为___________ mol。

(1)在搅拌下向氧化镁浆料[主要成分为Mg(OH)2]中匀速缓慢通入SO2气体,生成
 。
。①“吸收”过程中,发生的主要反应的化学方程式为
②64gSO2在标准状况下的体积约为
③NaOH溶液也可以用于捕集SO2,配制
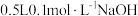 溶液,需NaOH
溶液,需NaOH(2)在催化剂作用下MgSO3被O2氧化为MgSO4。“氧化”过程若转移1mole⁻,则消耗标准状况下O2的体积约为
(3)制取MgSO4∙H2O晶体。将氧化后溶液蒸发浓缩、降温至室温结晶,
(4)
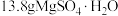 中所含Mg2+的物质的量为
中所含Mg2+的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某实验小组欲从苯甲酸、环己烷和苯酚的混合物中分离出苯甲酸、环己烷和苯酚,设计分离流程如图所示,所加试剂均过量,请回答下列问题:
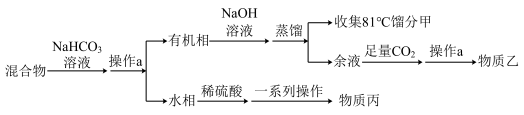
已知:①苯甲酸的沸点为249.2℃,100℃会迅速升华;
②环己烷的沸点为80.7℃,苯酚的沸点为181.9℃,二者易形成恒沸混合液。
(1)“操作a”为___________ ,分液漏斗使用前必须进行的操作为___________ 。
(2)甲中含有少量水,可以加入物质___________ (填标号)充分反应,然后蒸馏;获得物质乙的过程中,通入足量CO₂生成苯酚的化学方程式为___________ ,苯酚的俗名为 ___________ 。
A. NaCl B. CaO C.浓盐酸
(3)“一系列操作”为蒸发浓缩、冷却结晶、___________ 、___________ 、干燥,物质丙的分子式为 ___________ 。

已知:①苯甲酸的沸点为249.2℃,100℃会迅速升华;
②环己烷的沸点为80.7℃,苯酚的沸点为181.9℃,二者易形成恒沸混合液。
(1)“操作a”为
(2)甲中含有少量水,可以加入物质
A. NaCl B. CaO C.浓盐酸
(3)“一系列操作”为蒸发浓缩、冷却结晶、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
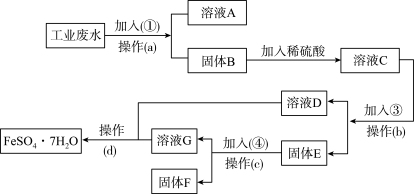
【推荐1】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。
(1)加入的试剂①为______ (填化学式),加入试剂①的目的是______ 。
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为______ 。洗涤固体B的操作是________ 。
(3)固体E的成分为_____ ,加入的试剂④为_____ ,发生的化学方程式为_________ 。
(4)从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为______ 、______ 、______ 、洗涤、干燥。
(1)加入的试剂①为
(2)操作a的名称为过滤、洗涤,所需要的玻璃仪器为
(3)固体E的成分为
(4)从溶液D和溶液G中得到FeSO4•7H2O晶体的操作为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备难溶于水的碱式碳酸铜的流程如图:
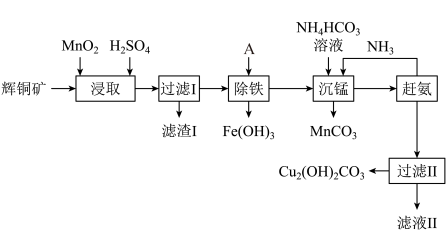
(1)下列措施是为了加快浸取速率,其中无法达到目的的是_______(填字母)。
(2)滤渣Ⅰ中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______ 。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是_______ 。
(4)“除铁”的方法是通过调节溶液pH,使 转化为Fe(OH)3。则加入的试剂A可以是
转化为Fe(OH)3。则加入的试剂A可以是_______ (填化学式):“赶氨”时,最适宜的操作方法是_______ 。
(5)“沉锰”(除 )过程中有关反应的离子方程式为
)过程中有关反应的离子方程式为_______ 。

(1)下列措施是为了加快浸取速率,其中无法达到目的的是_______(填字母)。
| A.延长浸取时间 | B.将辉铜矿粉碎 | C.充分搅拌 | D.适当增加硫酸浓度 |
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是
(4)“除铁”的方法是通过调节溶液pH,使
 转化为Fe(OH)3。则加入的试剂A可以是
转化为Fe(OH)3。则加入的试剂A可以是(5)“沉锰”(除
 )过程中有关反应的离子方程式为
)过程中有关反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知有以下物质相互转化
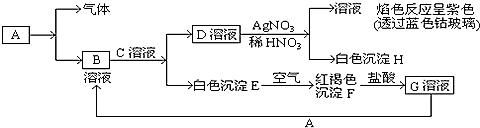
试回答:
(1)写出B的化学式___ 。C的化学式___ 。D的化学式___ 。
(2)写出由E转变成F的化学方程式___ 。
(3)把KSCN加到G溶液中的现象是___ ;向G溶液加入A的有关离子反应方程式___ 。
(4)焰色反应是___ (填物理或化学)变化,经过焰色反应试验后的铂丝可选择下面___ (填字母)试剂清洗。
A.硫酸 B.盐酸 C.硝酸
(5)选择合适的方法除杂:
①Fe2O3[Fe(OH)2]______ 。
②FeCl3溶液(FeCl2)______ 。
③FeCl2溶液(FeCl3)______ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)把KSCN加到G溶液中的现象是
(4)焰色反应是
A.硫酸 B.盐酸 C.硝酸
(5)选择合适的方法除杂:
①Fe2O3[Fe(OH)2]
②FeCl3溶液(FeCl2)
③FeCl2溶液(FeCl3)
您最近一年使用:0次



