已知:A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,H是白色沉淀,W溶液中加入KSCN溶液出现红色。各物质之间的转化关系如下图所示,请回答下列问题:
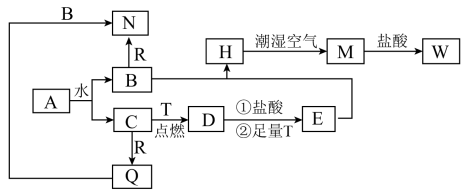
(1)写出化学式:D_______ ,W_______ 。
(2)H在潮湿空气中变成M的化学方程式_______ 。
(3)写出Q+B→N的离子方程式_______ ;在B与R反应中,当有1molN物质生成时,参与反应的氧化剂有_______ mol。
(4)D→E过程中①的离子反应方程式_______ 。
(5)将一定量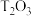 和
和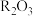 混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
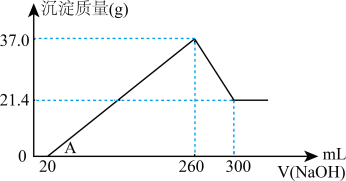
①混合物中含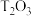 的质量为
的质量为_______ g;
②所用硫酸溶液物质的量浓度为_______  。
。

(1)写出化学式:D
(2)H在潮湿空气中变成M的化学方程式
(3)写出Q+B→N的离子方程式
(4)D→E过程中①的离子反应方程式
(5)将一定量
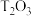 和
和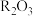 混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
①混合物中含
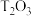 的质量为
的质量为②所用硫酸溶液物质的量浓度为
 。
。
更新时间:2022-12-16 17:48:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:A、F为金属单质,D、E为气体单质,E是黄绿色气体,其余均为化合物,其中B为黑色粉末,C的焰色试验呈黄色,金属单质F既可以与C溶液反应,也可以与G溶液反应,且均产生D气体。各物质间的转化关系如图所示(部分生成物已略去)。
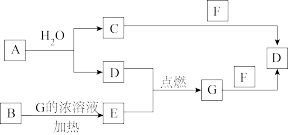
回答下列问题:
(1)单质A应保存在_______ 中。
(2)F的化学式是_______ 。
(3)每生成标准状况下33.6LE气体,被氧化的G的物质的量为_______ 。
(4)描述D在E中燃烧的实验现象_______ 。
(5)写出C溶液与F反应的化学方程式_______ 。

回答下列问题:
(1)单质A应保存在
(2)F的化学式是
(3)每生成标准状况下33.6LE气体,被氧化的G的物质的量为
(4)描述D在E中燃烧的实验现象
(5)写出C溶液与F反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
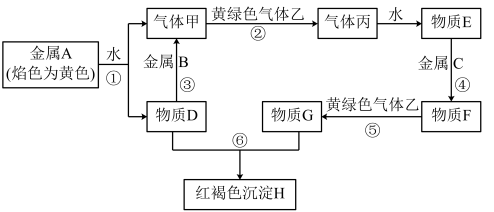
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:甲:______ 、乙:_____ 、F:_____ 、H________ ;
(2)金属B既能与强酸又能与强碱反应,该金属B是:_________ (填化学式),金属C的最高价阳离子遇KSCN溶液呈血红色,该金属C是:_______ (填化学式);
(3)反应③的化学方程式____________ ;
(4)反应⑤的离子方程式____________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:甲:
(2)金属B既能与强酸又能与强碱反应,该金属B是:
(3)反应③的化学方程式
(4)反应⑤的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
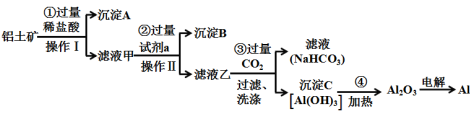
(1)用电解饱和食盐水制备试剂a的化学方程式为___________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________ ;
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是___________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为___________ 。
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是___________ ;
a.MgO b.V2O5 c.Fe3O4 d.MnO2
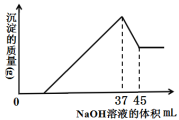
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为___________ 。

(1)用电解饱和食盐水制备试剂a的化学方程式为
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为

您最近一年使用:0次
【推荐1】铝氢化钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分Al2O3,含少量SiO2、Fe2O3等杂质)为原料制备NaAlH4的一种流程如图:

已知:碱浸中SiO2转化成难溶的Na2Al2SixO8
(1)Na2Al2SixO8用氧化物的形式表示为___ (x用具体的数值表示)。
(2)过滤1得滤液的主要成分为NaOH和NaAlO2,写出反应1中NaHCO3与NaAlO2反应的离子方程式:___ 。
(3)电解2生成NaHCO3和NaOH用于循环使用,写出电解2阴极的电极反应式:___ 。
(4)反应3的化学方程式为___ 。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为___ 。
(6)滤渣主要成分有Na2Al2SixO8和Fe2O3,可以采用如图流程进行分离:

①滤渣溶于盐酸所得的固体物质可能为___ (填化学式)。
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因___ 。
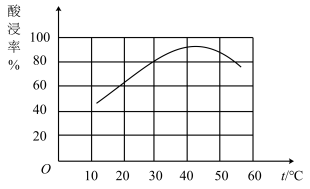
③已知常温下,Ksp[Fe(OH)3]=8.0×10-38,Al3+开始沉淀的pH为4,(溶液中离子的浓度小于1×10-5mol/L为沉淀完全),从滤液中先分离出Fe3+,应调节pH范围为___ (lg2≈0.3)。

已知:碱浸中SiO2转化成难溶的Na2Al2SixO8
(1)Na2Al2SixO8用氧化物的形式表示为
(2)过滤1得滤液的主要成分为NaOH和NaAlO2,写出反应1中NaHCO3与NaAlO2反应的离子方程式:
(3)电解2生成NaHCO3和NaOH用于循环使用,写出电解2阴极的电极反应式:
(4)反应3的化学方程式为
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为
(6)滤渣主要成分有Na2Al2SixO8和Fe2O3,可以采用如图流程进行分离:

①滤渣溶于盐酸所得的固体物质可能为
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因

③已知常温下,Ksp[Fe(OH)3]=8.0×10-38,Al3+开始沉淀的pH为4,(溶液中离子的浓度小于1×10-5mol/L为沉淀完全),从滤液中先分离出Fe3+,应调节pH范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用赤铁矿(主要含Fe2O3、FeO,还含有少量的Al2O3、CuO等杂质 制备绿矾(FeSO4∙7H2O)的流程如下:
制备绿矾(FeSO4∙7H2O)的流程如下:
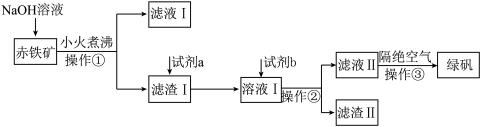
(1)NaOH溶液加入赤铁矿中发生反应的离子方程式为___________ 。
(2)滤液I通过一系列操作可得到Al2O3,该过程涉及化学反应的流程可表示为___________ 。(示例:滤液I B……)。
B……)。
(3)试剂a为___________ (填化学式),试剂 为
为___________ (填化学式),“溶液I”中氧化性最强的阳离子为___________ (填化学式)。
(4)操作③需要隔绝空气的主要原因是___________ 。
(5)8.34gFeSO4∙7H2O(M=278g∙mol-1)样品受热分解过程中样品质量随温度变化的曲线如图所示:
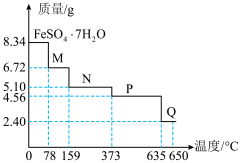
请回答下列问题
①温度为78℃时,固体物质M的化学式为___________ 。
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见含硫氧化物生成,则Q的化学式为___________ 。
 制备绿矾(FeSO4∙7H2O)的流程如下:
制备绿矾(FeSO4∙7H2O)的流程如下:
(1)NaOH溶液加入赤铁矿中发生反应的离子方程式为
(2)滤液I通过一系列操作可得到Al2O3,该过程涉及化学反应的流程可表示为
 B……)。
B……)。(3)试剂a为
 为
为(4)操作③需要隔绝空气的主要原因是
(5)8.34gFeSO4∙7H2O(M=278g∙mol-1)样品受热分解过程中样品质量随温度变化的曲线如图所示:

请回答下列问题
①温度为78℃时,固体物质M的化学式为
②取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种常见含硫氧化物生成,则Q的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品)。
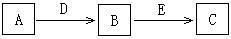
(1)若D为氧气,E为NaOH,C为NaAlO2,则单质A的名称为_____________ ;B转化为C的化学方程式:_________________ ;
(2)若A为气态单质,B为漂白粉的有效成分,C具有漂白性,则C的化学式为_____________ ;A转化为B的化学方程式:__________________ ;
(3)若A、B、C均为钠盐的水溶液,D、E均为卤素单质,写出B转化为C的离子方程式:_______________ 。
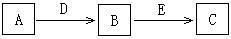
(1)若D为氧气,E为NaOH,C为NaAlO2,则单质A的名称为
(2)若A为气态单质,B为漂白粉的有效成分,C具有漂白性,则C的化学式为
(3)若A、B、C均为钠盐的水溶液,D、E均为卤素单质,写出B转化为C的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
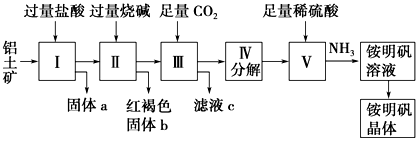
【推荐1】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示;
请回答下列问题:
(1)固体a的化学式为_______________ ,Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________ 。
(2)由Ⅴ制取铵明矾溶液的化学方程式为____________ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)______________ 、冷却结晶、过滤洗涤。
(3)以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数98%的硫酸(密度1.84 g/cm3)_________________ L(保留4位有效数字)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为____________________ 。

请回答下列问题:
(1)固体a的化学式为
(2)由Ⅴ制取铵明矾溶液的化学方程式为
(3)以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数98%的硫酸(密度1.84 g/cm3)
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
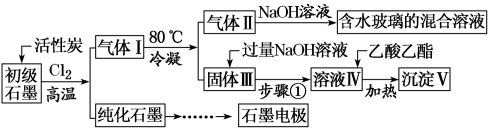
【推荐2】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用工艺如下:
(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是_______ 。
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。气体I中的氯化物主要为_______ 。由气体II中某物质得到水玻璃的化学方程式为_______ 。
(3)步骤①为:搅拌、_______ 。
(4)由溶液IV生成沉淀V的总反应的离子方程式为_______ 。100 kg初级石墨最多可获得V的质量为_______ kg。

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。气体I中的氯化物主要为
(3)步骤①为:搅拌、
(4)由溶液IV生成沉淀V的总反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
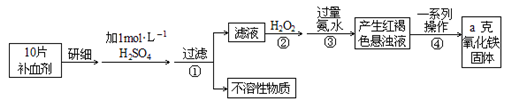
【推荐1】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法______________________ ,该过程的现象为:___________________
(2)步骤②加入过量H2O2的目的(用离子方程式表示):_______________ 。
(3)步骤③中反应的离子方程式:_______________________________________ 。
(4)实际上向滤液中直接滴加X溶液最终也会生成红褐色浊液,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________ 。
(5)步骤④中最终得到a克红棕色粉末,则一系列处理的操作步骤:_________ 、洗涤、_________ 、冷却、称量。
(6)若实验无损耗,则每片补血剂含铁元素的质量__________ g。
(7)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含______________ mgFeSO4·7H2O的片剂。

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法
(2)步骤②加入过量H2O2的目的(用离子方程式表示):
(3)步骤③中反应的离子方程式:
(4)实际上向滤液中直接滴加X溶液最终也会生成红褐色浊液,此过程中发生的氧化还原反应为(用化学方程式表达)
(5)步骤④中最终得到a克红棕色粉末,则一系列处理的操作步骤:
(6)若实验无损耗,则每片补血剂含铁元素的质量
(7)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】各物质间的转化关系如下图所示,请完成下列空白。
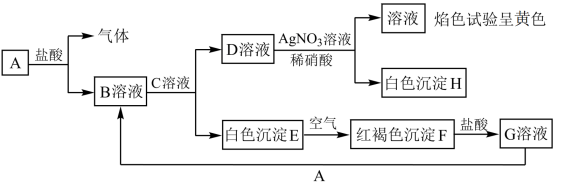
(1)写出D和H的化学式:D_______ ;H_______ 。
(2)B溶液中加入C,写出反应的离子方程式:_______ 。
(3)写出E转变成F的化学方程式:_______ 。
(4)向G溶液中加入A,写出反应的离子方程式:_______ 。

(1)写出D和H的化学式:D
(2)B溶液中加入C,写出反应的离子方程式:
(3)写出E转变成F的化学方程式:
(4)向G溶液中加入A,写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组同学欲探究某袋敞口放置一段时间的名为“硫酸亚铁家庭园艺精品肥料”的化肥的主要成分及相关性质。首先对该化肥的成分进行了如下假设:
a.只含有FeSO4
b.含有FeSO4和Fe2(SO4)3
c.只含有Fe2(SO4)3
将化肥固体粉末溶于水中得到溶液(记为X),进行如下实验:
(1)对实验ⅰ的预期现象是产生白色沉淀、变为灰绿色、最后出现红褐色沉淀,预期产生该现象的依据是(用化学方程式或离子方程式表达)___________ 、___________ 。
(2)由实验ⅱ得出的结论是,化肥中肯定有___________ (填化学式)。
为进一步验证假设,小组同学进行了以下实验:
(3)实验ⅳ中氯水参加反应的离子方程式是___________ 。
(4)通过以上实验,可得到的结论是假设___________ 成立。
a.只含有FeSO4
b.含有FeSO4和Fe2(SO4)3
c.只含有Fe2(SO4)3
a.只含有FeSO4
b.含有FeSO4和Fe2(SO4)3
c.只含有Fe2(SO4)3
将化肥固体粉末溶于水中得到溶液(记为X),进行如下实验:
| 序号 | 操作 | 现象 |
| ⅰ | 取2mL溶液X,加入1mL1mol·L-1NaOH溶液 | 产生红褐色沉淀 |
| ⅱ | 取2mL溶液X,加入1滴KSCN溶液 | 溶液显红色 |
(2)由实验ⅱ得出的结论是,化肥中肯定有
为进一步验证假设,小组同学进行了以下实验:
| 序号 | 操作 | 现象 |
| ⅲ | 取2mL溶液X,加入1滴KSCN溶液,再加入1mL水 | 溶液显红色 |
| ⅳ | 取2mL溶液X,加入1滴KSCN溶液,再加入1mL氯水 | 溶液显红色,颜色比ⅲ深 |
(4)通过以上实验,可得到的结论是假设
a.只含有FeSO4
b.含有FeSO4和Fe2(SO4)3
c.只含有Fe2(SO4)3
您最近一年使用:0次



