在体积为1L密闭容器中充入1 mol CO和1 mol H2O(g),在一定条件下发生反应CO(g)+H2O(g)  CO2(g)+H2(g),达到平衡时,CO的转化率为50%,在另一相同的密闭容器中充入1 mol CO和4mol H2O(g)时,在上述条件发下反应,达平衡时下列说法正确的是
CO2(g)+H2(g),达到平衡时,CO的转化率为50%,在另一相同的密闭容器中充入1 mol CO和4mol H2O(g)时,在上述条件发下反应,达平衡时下列说法正确的是
 CO2(g)+H2(g),达到平衡时,CO的转化率为50%,在另一相同的密闭容器中充入1 mol CO和4mol H2O(g)时,在上述条件发下反应,达平衡时下列说法正确的是
CO2(g)+H2(g),达到平衡时,CO的转化率为50%,在另一相同的密闭容器中充入1 mol CO和4mol H2O(g)时,在上述条件发下反应,达平衡时下列说法正确的是| A.CO的转化率为不变 | B.CO的转化率为80% |
| C.H2O的转化率增大 | D.H2的浓度为1mol/L |
更新时间:2022-12-17 20:38:42
|
【知识点】 化学平衡常数的有关计算解读
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知反应: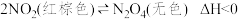 。将一定量的
。将一定量的 充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
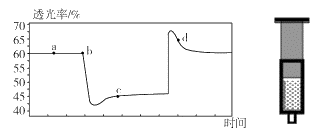
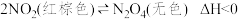 。将一定量的
。将一定量的 充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气体透光率随时间的变化的关系图(气体颜色越深,透光率越小)。下列说法正确的是
A.d点: |
| B.b点的操作是拉伸注射器 |
C.c点与a点相比,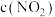 增大, 增大,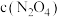 减小 减小 |
| D.若注射器绝热(不与外界进行热交换),则压缩达新平衡后平衡常数K值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在三种不同条件下,分别向容积为2 L的密闭容器中充入2 mol A和1 mol B,发生反应:2A(g)+B(g) 2D(g)。相关条件和数据见下表:
2D(g)。相关条件和数据见下表:
下列说法正确的是
 2D(g)。相关条件和数据见下表:
2D(g)。相关条件和数据见下表:| 实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 700 | 700 | 750 |
| 达平衡时间/min | 40 | 5 | 30 |
| 平衡时n(D)/mol | 1.6 | 1.6 | 1 |
| 化学平衡常数 | K1 | K2 | K3 |
| A.K1=80 |
| B.K1=K2<K3 |
| C.实验I和Ⅱ探究的可能是催化剂对化学反应的影响 |
| D.升高温度能加快反应速率的原理是降低了反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】温度为T℃,向体积不等的密闭容器中分别加入足量活性炭和1molNO2,发生反应:2C(S)+2NO2(g)=N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。已知:理想气体状态方程是pV=nRT。下列说法错误的是
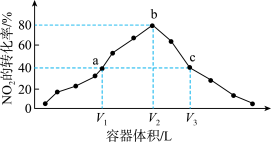
A.T℃时,a点时反应的平衡常数为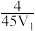 |
| B.根据理想气体方程可知,容器内压强:Pa:Pb=6:7 |
| C.T℃时,b点达到化学平衡状态,c点未达到化学平衡状态 |
| D.对c点容器加压,缩小容器体积,则此时v正>v逆 |
您最近一年使用:0次



