回答下列问题:
(1)甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
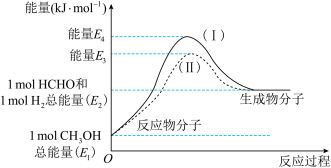
①甲醇催化脱氢转化为甲醛的反应是_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
②过程I与过程II的反应热是否相同?_______ ,原因是_______ 。
(2)在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:_______ 。
(3)CH4(g)+2O2(g)=CO2 (g) +2H2O(l) △H1
CH4(g)+2O2(g)=CO2 (g) +2H2O(g) △H2
则 △H1_______ △H2(填“>”、“﹤”或“=”)
(4)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知: ① N2(g)+2O2(g)=N2O4 (l) △H1= -195.0kJ/mol
② N2H4 (l)+ O2(g)= N2(g)+ 2H2O(g) △H2= -534.2kJ/mol
写出肼和N2O4反应的热化学方程式_______ 。
(1)甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。

①甲醇催化脱氢转化为甲醛的反应是
 填“吸热”或“放热”
填“吸热”或“放热”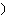 反应。
反应。②过程I与过程II的反应热是否相同?
(2)在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:
(3)CH4(g)+2O2(g)=CO2 (g) +2H2O(l) △H1
CH4(g)+2O2(g)=CO2 (g) +2H2O(g) △H2
则 △H1
(4)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知: ① N2(g)+2O2(g)=N2O4 (l) △H1= -195.0kJ/mol
② N2H4 (l)+ O2(g)= N2(g)+ 2H2O(g) △H2= -534.2kJ/mol
写出肼和N2O4反应的热化学方程式
更新时间:2022-12-09 17:57:37
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】反应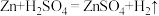 的能量变化趋势如图甲所示。
的能量变化趋势如图甲所示。___________ (填“吸热”或“放热”)反应。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为___________ (填“正”或“负”)极。铜片上产生的现象为___________ ,该极的电极反应式为___________ 。
(3)某学生为了探究锌与硫酸反应过程中的速率变化,将表面被氧化的锌粒投入稀硫酸中,测得生成氢气的速率 与反应时间t关系曲线如图乙所示。
与反应时间t关系曲线如图乙所示。___________ 。
②曲线b~c段,产生氢气的速率增加较快的主要原因是___________ 。
③曲线由c以后,产生氢气的速率逐渐下降的主要原因是___________ 。
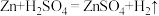 的能量变化趋势如图甲所示。
的能量变化趋势如图甲所示。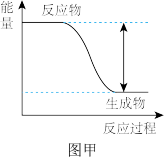
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
(3)某学生为了探究锌与硫酸反应过程中的速率变化,将表面被氧化的锌粒投入稀硫酸中,测得生成氢气的速率
 与反应时间t关系曲线如图乙所示。
与反应时间t关系曲线如图乙所示。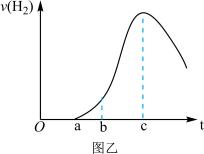
②曲线b~c段,产生氢气的速率增加较快的主要原因是
③曲线由c以后,产生氢气的速率逐渐下降的主要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol 与足量
与足量 充分燃烧生成液态水时放出572kJ热量。
充分燃烧生成液态水时放出572kJ热量。
①该反应的能量变化可用图中的_______ (填字母)表示。

②写出 燃烧生成液态水的热化学反应方程式:
燃烧生成液态水的热化学反应方程式:_______ 。
(4)表中是部分共价键的键能。
根据表中的数据写出工业合成氨的热化学反应方程式:_______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)已知:2mol
 与足量
与足量 充分燃烧生成液态水时放出572kJ热量。
充分燃烧生成液态水时放出572kJ热量。①该反应的能量变化可用图中的

②写出
 燃烧生成液态水的热化学反应方程式:
燃烧生成液态水的热化学反应方程式:(4)表中是部分共价键的键能。
| 共价键 |  |  |  |
键能( ) ) | 436 | 946 | 391 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】生产生活中的化学反应都伴随能量的变化,请用学到的有关知识回答下列问题:
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热盒饭”可利用下面___________ (填字母序号)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)CH3OH是优质液体燃料,在25℃、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:___________ 。
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用
(2)“即热盒饭”可利用下面
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)CH3OH是优质液体燃料,在25℃、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】东京奥运会火炬传递的火炬样式采用樱花形状。奥运会火炬常用的燃料为丙烷(C3H8)、丁烷(C4H10)等。已知:
(1)写出丙烷燃烧热的热化学方程式:___________ 。
(2)下列有关说法不正确的是___________ (填字母)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷多
C.正丁烷比异丁烷稳定
(3)现有3 mol由甲烷和乙烷组成的混合气体,完全燃烧放出的热量是3340 kJ,则该混合气体中甲烷和乙烷的物质的量之比是___________ 。
| 化合物 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | 正丁烷CH3CH2CH2CH3 | 异丁烷CH3CH(CH3)2 |
| 燃烧热kJ·mol-1 | 890 | 1560 | 2220 | 2878 | 2870 |
(2)下列有关说法不正确的是
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.异丁烷分子中的碳氢键比正丁烷多
C.正丁烷比异丁烷稳定
(3)现有3 mol由甲烷和乙烷组成的混合气体,完全燃烧放出的热量是3340 kJ,则该混合气体中甲烷和乙烷的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】我国含硫天然气资源丰富,甲烷与硫化氢重整制氢和天然气脱硫具有重要的现实意义。甲烷与硫化氢重整制氢反应为 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: 在
在_____ 下可自发进行。
A.高温 B.低温
在恒压条件下,起始时按 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数 的影响如图所示:
的影响如图所示: 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是_____ 。
(3)已知每1克 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_____ 。
 ,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为:
,其过程中反应ⅰ、ⅱ及其相对能量变化示意图为: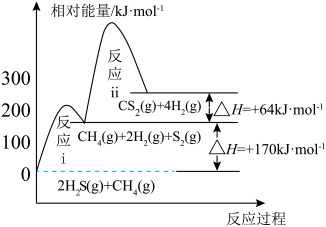
 在
在A.高温 B.低温
在恒压条件下,起始时按
 (同时通入一定量的
(同时通入一定量的 进行稀释,
进行稀释, 不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中
不参与反应)向某密闭容器中充入反应混合物,温度变化对平衡时反应混合物中 、
、 、
、 、
、 的物质的量分数
的物质的量分数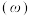 的影响如图所示:
的影响如图所示: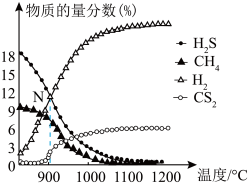
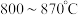 温度区间内,随温度升高,
温度区间内,随温度升高, 在平衡时反应混合物中含量迅速下降,而
在平衡时反应混合物中含量迅速下降,而 的含量几乎为0,根据图2分析其可能的原因是
的含量几乎为0,根据图2分析其可能的原因是(3)已知每1克
 燃烧放热
燃烧放热 ,则表示
,则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ΔH=﹣570
②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6
③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8
④C(s)+O2(g)=CO2(g)ΔH=﹣393.5
回答下列问题:
(1)上述反应中属于吸热反应的是___________ 。(填写序号)。
(2)H2的燃烧热为___________ 。
(3)燃烧10 g H2生成液态水,放出的热量为___________ 。
(4)CO的燃烧热的热化学方程式为:___________ 。
①2H2(g)+O2(g)=2H2O(l) ΔH=﹣570

②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6

③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8

④C(s)+O2(g)=CO2(g)ΔH=﹣393.5

回答下列问题:
(1)上述反应中属于吸热反应的是
(2)H2的燃烧热为
(3)燃烧10 g H2生成液态水,放出的热量为
(4)CO的燃烧热的热化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1 (反应I)
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1 (反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) ΔH2=-175.6kJ·mol-1 (反应II)
CaS(s)+4CO2(g) ΔH2=-175.6kJ·mol-1 (反应II)
请回答下列问题:
(1)反应I是放热反应还是吸热反应?________ ,能否通过反应I判断等物质的量的CO、CO2具有能量的高低?_______ 。
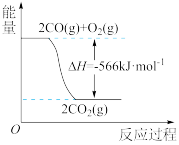
(2)已知CO转化成CO2的能量关系如图所示。写出该反应的热化学方程式_______ ,则CO的燃烧热ΔH为______ kJ·mol-1。
(3)依据反应I、II确定反应CaO(s)+3CO(g)+SO2(g)===CaS(s)+3CO2(g) ΔH=________ kJ·mol-1。
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1 (反应I)
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4kJ·mol-1 (反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) ΔH2=-175.6kJ·mol-1 (反应II)
CaS(s)+4CO2(g) ΔH2=-175.6kJ·mol-1 (反应II)请回答下列问题:
(1)反应I是放热反应还是吸热反应?
(2)已知CO转化成CO2的能量关系如图所示。写出该反应的热化学方程式

(3)依据反应I、II确定反应CaO(s)+3CO(g)+SO2(g)===CaS(s)+3CO2(g) ΔH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)对于下列反应:2SO2 + O2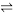 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为___________ ,用O2浓度变化来表示的反应速率为___________ 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为___________ 。
(2)已知:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1;
H2O(g)=H2O(1);△H2;
C2H5OH(g)=C2H5OH(1);△H3
若使23 g C2H5OH(1)完全燃烧生成H2O(1),则放出的热量为____
(1)对于下列反应:2SO2 + O2
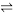 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为(2)已知:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1;
H2O(g)=H2O(1);△H2;
C2H5OH(g)=C2H5OH(1);△H3
若使23 g C2H5OH(1)完全燃烧生成H2O(1),则放出的热量为
您最近一年使用:0次

 H2(g)+
H2(g)+

