过氧化氢是一种常用的绿色试剂,某学习小组针对 性质进行如下实验。
性质进行如下实验。
I.验证 的还原性
的还原性
查阅资料: 溶液与氯水发生反应时表现还原性。
溶液与氯水发生反应时表现还原性。
(1)制取氯水
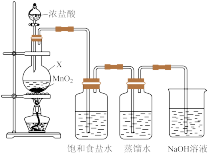
①仪器X的名称是_________ ,生成 的化学方程式为
的化学方程式为 _________ 。
②饱和食盐水的作用是_________ 。
(2)取5mL上述新制饱和氯水于试管中,向其中加入 溶液至过量,产生大量气泡
溶液至过量,产生大量气泡 该气体可使余烬复燃
该气体可使余烬复燃 ,还观察到溶液颜色发生的变化是
,还观察到溶液颜色发生的变化是 _________ 。
Ⅱ.探究 、
、 对
对 分解的影响
分解的影响
选用 溶液和
溶液和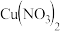 溶液,探究
溶液,探究 、
、 对
对 分解的影响。记录数据如下:
分解的影响。记录数据如下:
(3)实验结果显示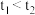 ,可得出的结论是:
,可得出的结论是:_________  填化学式
填化学式 更有利于
更有利于 分解。
分解。
(4)甲同学查阅资料得知: 能加速
能加速 分解,
分解, 对
对 分解无影响。为排除
分解无影响。为排除 干扰,该同学进行实验:向两份
干扰,该同学进行实验:向两份 溶液中分别加入amL浓度均为
溶液中分别加入amL浓度均为 _________  的
的 _________  填化学式
填化学式 溶液和
溶液和 _________  填化学式
填化学式 溶液。
溶液。 内,发现
内,发现 均几乎不分解。甲同学认为:在无
均几乎不分解。甲同学认为:在无 存在的情况下,
存在的情况下, 、
、 对
对 催化分解无影响。
催化分解无影响。
 性质进行如下实验。
性质进行如下实验。I.验证
 的还原性
的还原性查阅资料:
 溶液与氯水发生反应时表现还原性。
溶液与氯水发生反应时表现还原性。(1)制取氯水

①仪器X的名称是
 的化学方程式为
的化学方程式为 ②饱和食盐水的作用是
(2)取5mL上述新制饱和氯水于试管中,向其中加入
 溶液至过量,产生大量气泡
溶液至过量,产生大量气泡 该气体可使余烬复燃
该气体可使余烬复燃 ,还观察到溶液颜色发生的变化是
,还观察到溶液颜色发生的变化是 Ⅱ.探究
 、
、 对
对 分解的影响
分解的影响选用
 溶液和
溶液和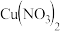 溶液,探究
溶液,探究 、
、 对
对 分解的影响。记录数据如下:
分解的影响。记录数据如下: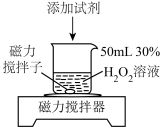 | 实验序号 | 添加试剂及用量 |  完全分解所需时间 完全分解所需时间 |
| 1 | 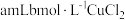 溶液 溶液 | 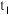 | |
| 2 | 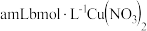 溶液 溶液 | 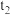 |
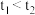 ,可得出的结论是:
,可得出的结论是: 填化学式
填化学式 更有利于
更有利于 分解。
分解。(4)甲同学查阅资料得知:
 能加速
能加速 分解,
分解, 对
对 分解无影响。为排除
分解无影响。为排除 干扰,该同学进行实验:向两份
干扰,该同学进行实验:向两份 溶液中分别加入amL浓度均为
溶液中分别加入amL浓度均为  的
的  填化学式
填化学式 溶液和
溶液和  填化学式
填化学式 溶液。
溶液。 内,发现
内,发现 均几乎不分解。甲同学认为:在无
均几乎不分解。甲同学认为:在无 存在的情况下,
存在的情况下, 、
、 对
对 催化分解无影响。
催化分解无影响。
更新时间:2022-12-13 20:11:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】如图所示是一个制取氯气并以氯气为原料进行特定反应的装置,多余的氯气可以贮存在b瓶中,其中各试剂瓶中所装试剂为:C(氯化亚铁溶液)、D(碘化钾淀粉溶液)、E(紫色石蕊试液)、G(含酚酞的氢氧化钠溶液)

(1)A是氯气的发生装置,反应的离子方程式为________________________ 。
(2)a仪器的名称为_________________ ,B中宜加入的液体是_________________ 。
(3)实验开始后C中反应的离子方程式是________________________________ ,D中的现象是___________________ ,E中的现象是____________________________ 。
(4)F装置中硬质玻璃管内盛有炭粉,若F中发生氧化还原反应,其产物为二氧化碳和氯化氢,则F中反应的化学方程式为___________________________________________ 。
(5)G中发生氧化还原反应的离子方程式为________________________________ 。
(6)F处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是____________________________ ;若发现装置B中该现象不明显,可能的原因是A或B装置漏气,查找原因时若用蘸有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程式_____________________________ 。

(1)A是氯气的发生装置,反应的离子方程式为
(2)a仪器的名称为
(3)实验开始后C中反应的离子方程式是
(4)F装置中硬质玻璃管内盛有炭粉,若F中发生氧化还原反应,其产物为二氧化碳和氯化氢,则F中反应的化学方程式为
(5)G中发生氧化还原反应的离子方程式为
(6)F处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】三氯氧磷( )是一种重要的化工原料,工业上可以直接氧化
)是一种重要的化工原料,工业上可以直接氧化 制备
制备 ,反应原理为:
,反应原理为: ,
,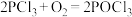 。
。
 、
、 的部分性质如下:
的部分性质如下:
某化学兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):

(1)仪器a的名称为_______ ,装置B中长颈漏斗的作用是_______ 。
(2)装置E用来制取 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(3)为使实验顺利进行,还需补充的装置为_______ 。
(4)反应时,需严格控制三个条件:
①先制取_______ ,缓慢地通入装置C中,直至装置C中的白磷消失后,再通入另一种气体。
②C装置用水浴加热控制温度为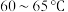 ,除加快反应速率外,另一目的是
,除加快反应速率外,另一目的是_______ 。
③反应物必须干燥,否则会在装置C中产生大量的白雾,其主要成分为_______ (写化学式)。
 )是一种重要的化工原料,工业上可以直接氧化
)是一种重要的化工原料,工业上可以直接氧化 制备
制备 ,反应原理为:
,反应原理为: ,
,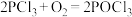 。
。 、
、 的部分性质如下:
的部分性质如下:| 物质 | 熔点/ | 沸点/ | 其他 |
 |  | 75.5 | 遇水生成 和 和 |
 | 2 | 105.3 | 遇水生成 和 和 |

(1)仪器a的名称为
(2)装置E用来制取
 ,反应的离子方程式为
,反应的离子方程式为(3)为使实验顺利进行,还需补充的装置为
(4)反应时,需严格控制三个条件:
①先制取
②C装置用水浴加热控制温度为
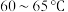 ,除加快反应速率外,另一目的是
,除加快反应速率外,另一目的是③反应物必须干燥,否则会在装置C中产生大量的白雾,其主要成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯气和亚氯酸钠(NaClO2)都是重要的漂白剂。
(1)实验室制备氯气时,可选用的发生装置为_____________ (填序号),反应的离子方程为_____________ 。
若要收集干燥、纯净的氯气,选择上述装置,其连接顺序为:发生装置→______ →i(按气流方向,用小写字母表示),F装置所盛溶液是___________ (填溶液名称);
(2)实验室制备无水NaClO2晶体的原理为2NaOH+2ClO2 + H2O2 2NaClO2+2H2O+O2,实验装置如图所示:
2NaClO2+2H2O+O2,实验装置如图所示:
已知:NaClO2和溶液在低于38℃时析出NaClCO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为 NaClO3和NaCl。
①装置B中制备ClO2气体的化学方程式为________________ ;
②装置C中的水浴温度应控制在__________________ (填温度范围);
③装置C中的反应达到预期目的后,下一步的实验操作是_______________ ,撤掉装置C的热源;
(3)工业上常用每克漂白剂转移的电子数表示其漂白效率,则氯气与亚氯酸钠的漂白效率之比为_______ (最终氯元素均以C1-形式存在,填最简整数比)。
(1)实验室制备氯气时,可选用的发生装置为

若要收集干燥、纯净的氯气,选择上述装置,其连接顺序为:发生装置→
(2)实验室制备无水NaClO2晶体的原理为2NaOH+2ClO2 + H2O2
 2NaClO2+2H2O+O2,实验装置如图所示:
2NaClO2+2H2O+O2,实验装置如图所示:
已知:NaClO2和溶液在低于38℃时析出NaClCO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为 NaClO3和NaCl。
①装置B中制备ClO2气体的化学方程式为
②装置C中的水浴温度应控制在
③装置C中的反应达到预期目的后,下一步的实验操作是
(3)工业上常用每克漂白剂转移的电子数表示其漂白效率,则氯气与亚氯酸钠的漂白效率之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某组同学为探究草酸浓度对该反应速率的影响,设计下列对照实验:
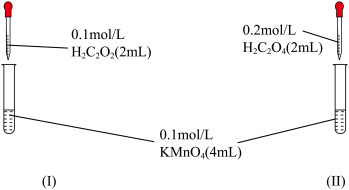
(1)写出上述反应的离子方程式____________ 。
(2)根据所学知识,你预期的实验现象是:_______ (填“l”或“Ⅱ”)中紫色先褪去
(3)实验时,他们发现反应速率的变化从开始后的一段时间内,变化趋势如图,已知反应过程中温度基本不变,分析:
①反应开始时,速度加块的原因为________ ;
②后期反应速度下降的原因为________ 。

(1)写出上述反应的离子方程式
(2)根据所学知识,你预期的实验现象是:
(3)实验时,他们发现反应速率的变化从开始后的一段时间内,变化趋势如图,已知反应过程中温度基本不变,分析:
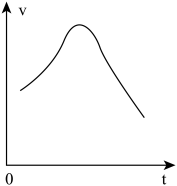
①反应开始时,速度加块的原因为
②后期反应速度下降的原因为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸的消费量常用来衡量一个国家工业发展水平。其中 的催化氧化是重要的一步,其反应为:
的催化氧化是重要的一步,其反应为: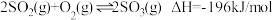 。回答下列问题:
。回答下列问题:
(1) 催化氧化反应在
催化氧化反应在_______ 温下自发(填“高”或“低”,下同),_______ 压有利于提高反应速率,_______ 压有利于提高平衡转化率。根据下表数据( 条件下测得)阐述实际工业生产选择
条件下测得)阐述实际工业生产选择 的理由:
的理由:_______ 。
(2)科研人员使用 为基础固硫材料,复合不同的催化剂
为基础固硫材料,复合不同的催化剂 催化
催化 向
向 的转化。同时研究了不同温度下使用三种催化剂对
的转化。同时研究了不同温度下使用三种催化剂对 固硫效率(用单位时间
固硫效率(用单位时间 转化率表示)的影响,结论如下图:
转化率表示)的影响,结论如下图:
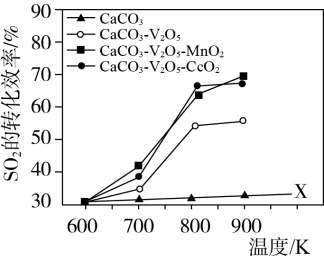
①仅使用 而不使用催化剂获得的X线的实验目的是
而不使用催化剂获得的X线的实验目的是_______ 。
②下列有关说法正确的是_______ 。
a.三种催化剂中 催化剂效率最低
催化剂效率最低
b.同温同压下,使用复合催化剂有利于提高 的平衡产率
的平衡产率
c.温度越高一定越有利于催化剂催化效率的提升
(3)某 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: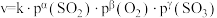 ,根据表中数据,
,根据表中数据,
_______ 。
 的催化氧化是重要的一步,其反应为:
的催化氧化是重要的一步,其反应为: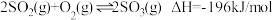 。回答下列问题:
。回答下列问题:(1)
 催化氧化反应在
催化氧化反应在 条件下测得)阐述实际工业生产选择
条件下测得)阐述实际工业生产选择 的理由:
的理由:| 压强 |  | 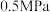 |  | 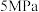 | 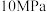 |
平衡时 的转化率 的转化率 | 97.5% | 98.9% | 99.2% | 99.6% | 99.7% |
(2)科研人员使用
 为基础固硫材料,复合不同的催化剂
为基础固硫材料,复合不同的催化剂 催化
催化 向
向 的转化。同时研究了不同温度下使用三种催化剂对
的转化。同时研究了不同温度下使用三种催化剂对 固硫效率(用单位时间
固硫效率(用单位时间 转化率表示)的影响,结论如下图:
转化率表示)的影响,结论如下图:
①仅使用
 而不使用催化剂获得的X线的实验目的是
而不使用催化剂获得的X线的实验目的是②下列有关说法正确的是
a.三种催化剂中
 催化剂效率最低
催化剂效率最低b.同温同压下,使用复合催化剂有利于提高
 的平衡产率
的平衡产率c.温度越高一定越有利于催化剂催化效率的提升
(3)某
 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: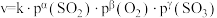 ,根据表中数据,
,根据表中数据,
| 实验 | 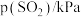 | 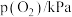 | 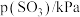 | 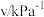 |
| 1 | m | n | p | q |
| 2 | 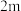 | n | p |  |
| 3 | m | n |  | 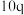 |
| 4 | m |  | p | 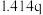 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ. 合成氨反应在化工生产中具有重要意义。
(1)合成氨反应为放热反应,如图图示表示的过程也为放热反应的是_____________________ (填字母)。 和
和 在催化剂表面合成氨的微观历程如图所示,用
在催化剂表面合成氨的微观历程如图所示,用 、
、 、
、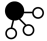 分别表示
分别表示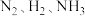 下列说法中正确的是 (填字母)。
下列说法中正确的是 (填字母)。
Ⅱ. 化学能在一定条件下能够转化为电能,构成原电池。
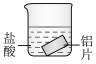
(3)为了探究化学反应中的能量变化,某同学设计了如图两个实验。
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示: 名称是
名称是_________________ (填“正极”或“负极”)。
②电解质溶液中 离子向
离子向_____________ 移动(填“电极 ”或“电极
”或“电极 ”)。
”)。
③电极 的电极反应式为
的电极反应式为_________________________________ 。
Ⅲ. 近年来,我国化工技术获得重大突破,利用合成气(主要成分为 和
和 )在催化剂的作用下合成甲醇
)在催化剂的作用下合成甲醇 是其中的一个研究项目,该研究发生的主要反应如下:
是其中的一个研究项目,该研究发生的主要反应如下:
Ⅰ. 与
与 反应合成甲醇:
反应合成甲醇:
Ⅱ. 与
与 反应合成甲醇:
反应合成甲醇: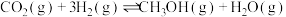
(5)在某一时刻采取下列措施,能使反应Ⅰ的正反应速率在该时刻减小的措施是 (填字母)。
(6)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是 。(填字母)
(1)合成氨反应为放热反应,如图图示表示的过程也为放热反应的是

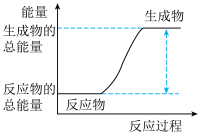



 和
和 在催化剂表面合成氨的微观历程如图所示,用
在催化剂表面合成氨的微观历程如图所示,用 、
、 、
、 分别表示
分别表示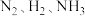 下列说法中正确的是 (填字母)。
下列说法中正确的是 (填字母)。
| A.反应过程存在非极性共价键的断裂和形成 |
B.催化剂仅起到吸附 和 和 的作用,对化学反应速率没有影响 的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.使用催化剂,合成氨反应放出的热量减少 |
Ⅱ. 化学能在一定条件下能够转化为电能,构成原电池。
(3)为了探究化学反应中的能量变化,某同学设计了如图两个实验。
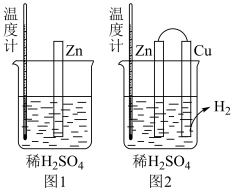
| A.图1和图2都只有锌棒表面产生气泡 | B.图2中产生气体的速度比1快 |
| C.图1中温度计的示数高于图2的示数 | D.图1和图2中温度计的示数相等,且均高于室温 |
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

 名称是
名称是②电解质溶液中
 离子向
离子向 ”或“电极
”或“电极 ”)。
”)。③电极
 的电极反应式为
的电极反应式为Ⅲ. 近年来,我国化工技术获得重大突破,利用合成气(主要成分为
 和
和 )在催化剂的作用下合成甲醇
)在催化剂的作用下合成甲醇 是其中的一个研究项目,该研究发生的主要反应如下:
是其中的一个研究项目,该研究发生的主要反应如下:Ⅰ.
 与
与 反应合成甲醇:
反应合成甲醇:
Ⅱ.
 与
与 反应合成甲醇:
反应合成甲醇: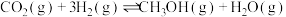
(5)在某一时刻采取下列措施,能使反应Ⅰ的正反应速率在该时刻减小的措施是 (填字母)。
A.恒温恒容下,再充入 | B.升高温度 |
C.恒温恒容下,向其中充入 | D.恒温恒压下,向其中充入 |
(6)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是 。(填字母)
A.单位时间内消耗 ,同时生成 ,同时生成 的 的 |
B. 的体积分数不再发生变化 的体积分数不再发生变化 |
C. |
| D.容器内气体的平均摩尔质量不再改变 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某学习小组设计如图装置,验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质不参与反应)。
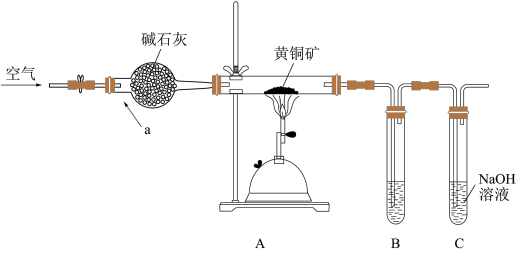
回答下列问题。
(1)仪器a的名称_________ ,碱石灰的作用______________________________________ 。
(2)为检验灼烧黄铜矿产生的气体,B中可选__________________
a.HNO3溶液 b.品红溶液 c.BaCl2溶液 d.溴水 e.KMnO4溶液
(3)C中NaOH的作用____________________________________________________
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀H2SO4反应生成Cu和CuSO4。
①请设计实验验证泡铜中含有Cu2O____________________________________________ 。
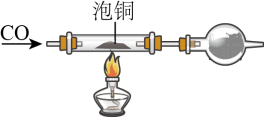
②用泡铜与CO反应来制取粗铜装置如下图,实验时依次进行的操作:
组装仪器→检查装置气密性→加装药品→____________ →____________ →…→尾气处理;CO还原Cu2O的化学方程式_______________________________________________
(5)为测定CuFeS2的纯度,称取a g黄铜矿样品充分灼烧,从灼烧产物中分离出泡铜,完全溶于稀硝酸,并配成200 mL的溶液,取20.00 mL该溶液用c mol· L-1的标准液EDTA(用H2Y2-表示)滴定至终点(标准液不与杂质反应),消耗EDTA V mL,则CuFeS2的纯度为____________ 。(滴定时的反应为:Cu2++H2Y2-===CuY2-+2H+)

回答下列问题。
(1)仪器a的名称
(2)为检验灼烧黄铜矿产生的气体,B中可选
a.HNO3溶液 b.品红溶液 c.BaCl2溶液 d.溴水 e.KMnO4溶液
(3)C中NaOH的作用
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀H2SO4反应生成Cu和CuSO4。
①请设计实验验证泡铜中含有Cu2O
②用泡铜与CO反应来制取粗铜装置如下图,实验时依次进行的操作:
组装仪器→检查装置气密性→加装药品→

(5)为测定CuFeS2的纯度,称取a g黄铜矿样品充分灼烧,从灼烧产物中分离出泡铜,完全溶于稀硝酸,并配成200 mL的溶液,取20.00 mL该溶液用c mol· L-1的标准液EDTA(用H2Y2-表示)滴定至终点(标准液不与杂质反应),消耗EDTA V mL,则CuFeS2的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】节日期间因燃放鞭炮会引起空气中 含量增大,造成大气污染。某实验小组同学欲探究
含量增大,造成大气污染。某实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的含量。
的含量。
(1)他们设计如下实验装置,请你参与探究,并回答下列问题:
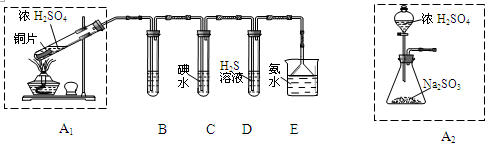
①装置A1中发生反应的化学方程式为______ ;
②装置B用于检验 的漂白性,其中所盛试剂为
的漂白性,其中所盛试剂为______ ,装置D用于检验 的
的______ 性;
③为验证二氧化硫的还原性,反应一段时间后取试管C中的溶液分成三份,进行如下实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 ,产生白色沉淀
,产生白色沉淀
上述方案合理的是______ (填“Ⅰ”、“Ⅱ”、“Ⅲ”);C中发生的离子方程式为:______ 。
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1你认为装置A2的优点是(写两点)______ 。
(2)他们拟用以下方法测定空气中 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
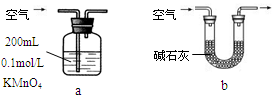
你认为哪个装置可行______ (填序号),另一装置不可行的理由为______ 。(如没有,则不填)
 含量增大,造成大气污染。某实验小组同学欲探究
含量增大,造成大气污染。某实验小组同学欲探究 的性质并测定空气中
的性质并测定空气中 的含量。
的含量。(1)他们设计如下实验装置,请你参与探究,并回答下列问题:

①装置A1中发生反应的化学方程式为
②装置B用于检验
 的漂白性,其中所盛试剂为
的漂白性,其中所盛试剂为 的
的③为验证二氧化硫的还原性,反应一段时间后取试管C中的溶液分成三份,进行如下实验:
方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 ,产生白色沉淀
,产生白色沉淀上述方案合理的是
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1你认为装置A2的优点是(写两点)
(2)他们拟用以下方法测定空气中
 含量(假设空气中无其他还原性气体)。
含量(假设空气中无其他还原性气体)。
你认为哪个装置可行
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易水解。
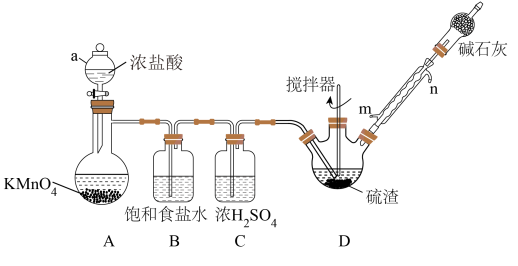
相关产物的熔沸点:
(1)仪器a的名称___________ ,A中发生反应的化学方程式___________ 。
(2)冷凝管的进水口为___________ (填“m”或“n”),碱石灰的作用为___________ 。
(3)如果缺少B装置,可能造成的影响为___________ 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,___________ (填操作名称,下同),得到粗产品,粗产品再___________ 可得到纯净的SnCl4。
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用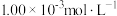 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②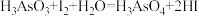
③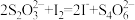
则产品中SnCl4的质量分数___________ (保留三位有效数字)。某同学认为粗产品中会溶有少量氯气,导致测量结果___________ (填“偏高”“偏低”或“无影响”)。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(2)冷凝管的进水口为
(3)如果缺少B装置,可能造成的影响为
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用
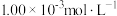 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:①

②
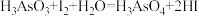
③
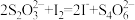
则产品中SnCl4的质量分数
您最近一年使用:0次



