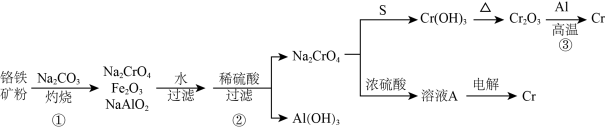
工业上以铭铁矿(主要成分为 ,含有少量
,含有少量 )为原料制备金属铬的流程如图。下列说法错误的是
)为原料制备金属铬的流程如图。下列说法错误的是
 ,含有少量
,含有少量 )为原料制备金属铬的流程如图。下列说法错误的是
)为原料制备金属铬的流程如图。下列说法错误的是
| A.反应①若在坩埚中进行,可以选择陶瓷坩埚 |
B.生成 的反应中氧化剂和还原剂的物质的量之比为2:1 的反应中氧化剂和还原剂的物质的量之比为2:1 |
C.加入浓硫酸发生反应的离子方程式: |
D.电解溶液 的阴极反应式: 的阴极反应式: |
更新时间:2022-12-24 21:52:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列化学用语书写正确的是
A.硫酸的电离方程式: |
B.氢氧化钡溶液与硫酸铜溶液反应的离子方程式: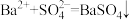 |
C.钠与水反应的离子方程式: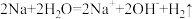 |
D.铁与盐酸反应的化学方程式: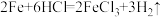 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学反应中,反应物用量或反应条件不同,可能对生成物产生影响。下列反应的生成物不受上述因素影响的
| A.KAl(SO4)2溶液和Ba(OH)2溶液 |
| B.铁粉和氯气反应 |
| C.NaOH溶液和Ca(HCO3)2溶液 |
| D.FeCl3溶液和锌反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
| B | 向5mL0.005mol/LFeCl3溶液中加入5mL0.010mol/LKSCN溶液,溶液呈红色,再滴加几滴KCl溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) N2O4(g),△H<0,平衡向生成NO2方向移动 N2O4(g),△H<0,平衡向生成NO2方向移动 |
| D | 在密闭容器中有反应:A(?)+xB(g) 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L | A为气体,x<2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列反应原理设计的应用,不正确的是
A.CO +H2O +H2O HCO HCO +OH-用热的纯碱溶液清洗油污效果更佳 +OH-用热的纯碱溶液清洗油污效果更佳 |
B.Al3++3H2O Al(OH)3(胶体)+3H+明矾净水 Al(OH)3(胶体)+3H+明矾净水 |
C.Cl2+H2O HCl+HClO新制氯水中加入碳酸钙,提高次氯酸浓度 HCl+HClO新制氯水中加入碳酸钙,提高次氯酸浓度 |
D.Fe3++3H2O Fe(OH)3+3H+配制Fe2(SO4)3溶液时,加入一定量Fe粉 Fe(OH)3+3H+配制Fe2(SO4)3溶液时,加入一定量Fe粉 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】含铬(+6)废水严重危害人体健康,工业上常用还原法进行处理。其部分工艺流程如下:

已知:①Cr(OH)3与Al(OH)3性质相似,是两性氢氧化物;
②Cr2O (橙色)+ H2O
(橙色)+ H2O  2CrO
2CrO (黄色) + 2H+。
(黄色) + 2H+。
下列说法错误的是

已知:①Cr(OH)3与Al(OH)3性质相似,是两性氢氧化物;
②Cr2O
 (橙色)+ H2O
(橙色)+ H2O  2CrO
2CrO (黄色) + 2H+。
(黄色) + 2H+。下列说法错误的是
| A.含铬(+6)废水随着酸性增强,颜色由黄色向橙色转变 |
B.若用NaHSO3做还原剂,则还原池中发生反应的离子方程式为:2CrO + 3HSO + 3HSO + 7H+ = 2Cr3++ 3SO + 7H+ = 2Cr3++ 3SO + 5H2O + 5H2O |
| C.常在沉淀池中加入絮凝剂,增大生成Cr(OH)3颗粒,使其更好地沉淀过滤回收 |
| D.调整pH时,若碱加入过量太多,导致pH过高,除铬效果不好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为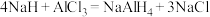 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是
 (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为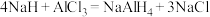 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是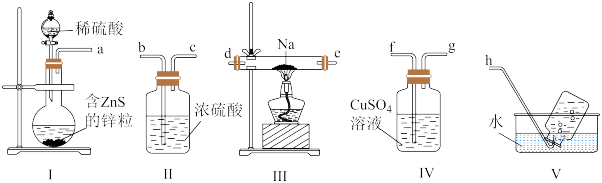
A.装置连接顺序为 |
| B.不能用浓硫酸、硝酸替代装置Ⅰ中的稀硫酸 |
| C.实验中观察到装置Ⅳ中产生黑色沉淀 |
D.实验室制备 的装置要保持干燥 的装置要保持干燥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某废催化剂主要成分有SiO2、ZnO、ZnS和CuS。某化学兴趣小组拟用该废催化剂为原料,制备硫酸锌和硫酸铜晶体。采用的实验方案如下,下列说法正确的是( )
已知:ZnS与稀硫酸发生反应且化合价不变,CuS既不溶于稀硫酸也不和稀硫酸反应。

已知:ZnS与稀硫酸发生反应且化合价不变,CuS既不溶于稀硫酸也不和稀硫酸反应。

| A.第一次浸出可以在烧杯中进行 |
| B.第二次浸出时发生反应为CuS+H2O2+H2SO4=CuSO4+S+2H2O |
| C.滤渣2中只有二氧化硅 |
| D.获得硫酸锌和硫酸铜晶体采用蒸发结晶的方式 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】黏土钒矿(主要成分为钒的+3、+4、+5价的化合物以及SiO2、Al2O3等)中钒的化合物溶于酸后多以VO+、VO2+、VO 形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。
形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。
已知:V2O5在碱性条件下以VO 形式存在。
形式存在。

以下说法正确的是( )
 形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。
形式存在,采用以下工艺流程可由黏土钒矿制备V2O5。已知:V2O5在碱性条件下以VO
 形式存在。
形式存在。
以下说法正确的是( )
A.“酸浸氧化”中欲使3molVO2+被氧化成VO ,至少需要1molKClO3 ,至少需要1molKClO3 |
B.滤液1中主要的阴离子有[Al(OH)4]-和VO |
| C.“煅烧”时需要的仪器主要有蒸发皿、玻璃棒、三脚架、酒精灯 |
D.“煅烧”时,NH4VO3受热分解:2NH4VO3 V2O5+2NH3↑+H2O V2O5+2NH3↑+H2O |
您最近一年使用:0次

 +2OH-=CaCO3 ↓+CO
+2OH-=CaCO3 ↓+CO +2H2O
+2H2O

