电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2_____ (填“>”“=”或“<”)2L,原因是_____ 。装置改进后,可用于制备NaOH溶液,若测定NaOH溶液的浓度,常用的方法为_____ 。


22-23高二上·全国·课时练习 查看更多[1]
(已下线)4.2.2 电解原理的应用-同步学习必备知识
更新时间:2022-12-27 18:08:10
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气是一种非常重要的化工原料,可用于制造盐酸、漂白剂、农药等,但氯气有毒,使用或接触到有关物质时应注意安全。请回答下列问题:
(1)新制氯水中,含有氯元素的微粒有___________ (填微粒符号,下同,不考虑水中杂质与氯气的反应),其中使新制氯水显淡黄绿色的微粒是___________ 。
(2) 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为___________ L。
(3)标准状况下,氯气的密度为___________ 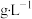 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是___________ (填序号)。
a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为___________ ;通常不用澄清石灰水吸收氯气的原因是___________ 。
(1)新制氯水中,含有氯元素的微粒有
(2)
 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为(3)标准状况下,氯气的密度为
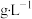 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】NaCN超标的电镀废水可用两段氧化法处理:
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为___________ (选填“酸性”、“碱性”或“中性”);原因是___________ 。
(2)写出第二次氧化时发生反应的离子方程式。___________
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成___________ 、___________ 和H2O。
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为
(2)写出第二次氧化时发生反应的离子方程式。
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B是两种常见的无机物,它们分别能与下图中周围4种物质在一定条件下反应:
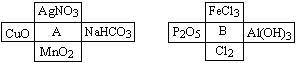
请回答下列问题:
(1)A溶液与B溶液反应的离子方程式_______________________ 。
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为________________
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:_________ ,____________
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:_______________

请回答下列问题:
(1)A溶液与B溶液反应的离子方程式
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某实验小组在常温下,用0.100mol/L的NaOH溶液滴定 20.00mL未知浓度的HCl溶液。

已知:混合溶液的体积等于酸、碱体积的相加,lg2=0.3。可根据图示计算滴定的突跃范围。
(1)该盐酸溶液的浓度为_______________________ 。
(2)若滴加20.02mLNaOH溶液,所得溶液的pH≈9.7,试计算滴加19.98mLNaOH溶液,所得溶液的pH≈________ ;(写出计算过程,保留1位小数)。

已知:混合溶液的体积等于酸、碱体积的相加,lg2=0.3。可根据图示计算滴定的突跃范围。
(1)该盐酸溶液的浓度为
(2)若滴加20.02mLNaOH溶液,所得溶液的pH≈9.7,试计算滴加19.98mLNaOH溶液,所得溶液的pH≈
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)室温下,使用pH计测定0.1 mol/LNH4Cl溶液的pH=5.12。由此可以得到的结论是_______ (填字母)。
a.溶液中c(H+)>c(OH-)
b.NH4+水解是微弱的
c.NH3·H2O是弱碱
d.由H2O电离出的c(H+)<10-7 mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.1 mol/LNaOH溶液分别滴定20.00 mL 0.1 mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是

①表示滴定盐酸的曲线是_______ (填序号)。
②滴定醋酸溶液的过程中:
ⅰ.V(NaOH)=10.00 mL时,溶液中离子浓度由大到小的顺序为_________ 。
ⅱ.当c(Na+)=c(CH3COO—)+c(CH3COOH)时,溶液pH____ 7(填“>”、“=”或“<”)。
a.溶液中c(H+)>c(OH-)
b.NH4+水解是微弱的
c.NH3·H2O是弱碱
d.由H2O电离出的c(H+)<10-7 mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.1 mol/LNaOH溶液分别滴定20.00 mL 0.1 mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是

①表示滴定盐酸的曲线是
②滴定醋酸溶液的过程中:
ⅰ.V(NaOH)=10.00 mL时,溶液中离子浓度由大到小的顺序为
ⅱ.当c(Na+)=c(CH3COO—)+c(CH3COOH)时,溶液pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图为工业上氯碱工业的电解槽示意图,据图回答:
(1)图中a、b物质分别是:a_____________ ;b____________ (填“名称”),c离子是___________ (填“符号”)。
(2)若没有阳离子交换膜,则电解一段时间后在电解槽的溶液中可能发生的化学反应方程式为________________ 。
(3)写出工业上电解饱和食盐水的化学方程式__________________ 。
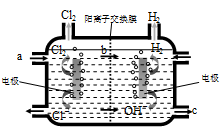
(1)图中a、b物质分别是:a
(2)若没有阳离子交换膜,则电解一段时间后在电解槽的溶液中可能发生的化学反应方程式为
(3)写出工业上电解饱和食盐水的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】海洋蕴藏着中极为丰富的化学资源,如海水中就有80多种元素,所含的盐大部分是氯化钠。十九世纪末工业上开始通过电解饱和食盐水的方法制备氯气、氨气和烧碱,并以它们为原料生产一系列含氯、含钠产品(氯碱工业),请回答下列问题:
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
(2)电解饱和食盐水时,与电源正极相连的电极叫阳极,阳极产物是氯气,可以用______ 检验,现象为______ ,写出检验氯气的离子方程式_____________________
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
(4)新制氧水呈浅黄绿色,是因为氯水中存在______(单选)
(5)有两组学生根据不同的反应原理在实验室制取氯气。

①请按要求填表。
②有同学建议第一组使用图所示装置作为氯气的发生装置,请谈谈你的看法______ 。
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。
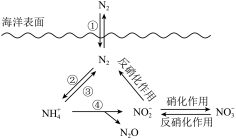
(6)海洋中的氮循环属于固氮作用的一步是______ (填图中的数字序号)。
(7)下列关于海洋氮循环的说法正确的是______(双选)。
(8)有氧时,在硝化细菌作用下, 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。_______ 。

(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是______ ,在最佳反应温度时, 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是____ 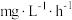 。
。
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
| A.侯德榜 | B.吴蕴初 | C.荣毅仁 | D.戴安邦 |
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
A. | B. | C. | D. |
A. | B. | C. | D. |

①请按要求填表。
实验组 | 实验原理 | 发生装置(填编号) |
第一组 |  | |
第二组 | 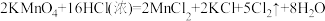 |

氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示。

(6)海洋中的氮循环属于固氮作用的一步是
(7)下列关于海洋氮循环的说法正确的是______(双选)。
| A.海洋中存在游离态的氮 |
| B.海洋中的氮循环起始于氮的氧化 |
C.向海洋排放含 的废水会影响海洋中 的废水会影响海洋中 的含量 的含量 |
| D.海洋中的反硝化作用一定有氧气的参与 |
 可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
可实现过程④的转化,方程式如下,请标出该反应的电子转移的方向与数目。
(9)有人研究了温度对海洋硝化细菌去除氯氮效果的影响.下表为对
 人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是
人工海水样本的监测数据.硝化细菌去除氨氮的最佳反应温度是 内去除氨氮反应的平均速率是
内去除氨氮反应的平均速率是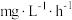 。
。温度/ | 样本氨氮含量/ | 处理 | 处理 |
氨氮含量/ | 氨氮含量/ | ||
20 | 1008 | 838 | 788 |
25 | 1008 | 757 | 468 |
30 | 1008 | 798 | 600 |
40 | 1008 | 977 | 910 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学原理在生产生活中有着广泛的应用。一种利用LiCl、Li2CO3制备金属锂的装置如图所示。

(1)该装置为____ 池,主要将____ 能转化为____ 能。
(2)电极N应与电源的____ 极相连,发生的电极反应式为____ 。
(3)每产生标准状况下22.4LCl2,将有____ molLi+通过隔膜。
(4)每产生1.4gLi,消耗____ gLi2CO3。
(5)写出工业上电解饱和食盐水制取氯气与氢氧化钠的离子方程式____ ,为获得较纯净的产品,选择____ 离子交换膜。
(6)钢铁发生吸氧腐蚀时,正极的电极反应式为____ ,最有效的电化学防止铁生锈的方法叫____ 。

(1)该装置为
(2)电极N应与电源的
(3)每产生标准状况下22.4LCl2,将有
(4)每产生1.4gLi,消耗
(5)写出工业上电解饱和食盐水制取氯气与氢氧化钠的离子方程式
(6)钢铁发生吸氧腐蚀时,正极的电极反应式为
您最近一年使用:0次






