已知0.1 mol·L-1的醋酸中存在电离平衡:CH3COOH CH3COO-+H+,加水稀释后CH3COOH的电离平衡常数K值的变化为
CH3COO-+H+,加水稀释后CH3COOH的电离平衡常数K值的变化为
 CH3COO-+H+,加水稀释后CH3COOH的电离平衡常数K值的变化为
CH3COO-+H+,加水稀释后CH3COOH的电离平衡常数K值的变化为| A.增大 | B.减小 | C.不变 | D.无法判断 |
更新时间:2022-12-20 15:06:11
|
【知识点】 电离平衡常数及影响因素解读
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】下列说法正确的是
| A.相同温度下,pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH) < c(CH3COONa) < c(Na2CO3) |
B.CH3COOH 溶液加水稀释后,溶液中  的值减小 的值减小 |
| C.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
| D.100℃时,pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】已知25℃时,CH3COOH的电离平衡常数K=1.75×10-5。下列说法正确的是
| A.向该溶液中加入一定量的硫酸,K增大 |
| B.升高温度,K增大 |
| C.向CH3COOH溶液中加入少量水,K增大 |
| D.向CH3COOH溶液中加入少量氢氧化钠溶液,K增大 |
您最近一年使用:0次







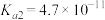
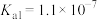
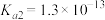


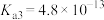
 可以发生
可以发生

