已知: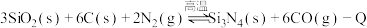 (Q>0),在反应条件下,向
(Q>0),在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子占有_______ 种能量不同的轨道。
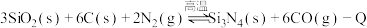 (Q>0),在反应条件下,向
(Q>0),在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子占有
更新时间:2023-01-05 21:10:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据物质结构知识回答下列问题。
Ⅰ.硒是一种非金属,与氧、硫同主族,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为___________ 。
(2)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为___________ ,其中Se原子采用的轨道杂化方式为___________ 。
(3)已知 与CO2结构相似,①
与CO2结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③SeO3分子内的键角
、③SeO3分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为___________ (填序号)。
Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)推算HCN分子中σ键与π键数目之比为___________ 。
(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
Ⅰ.硒是一种非金属,与氧、硫同主族,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为(3)已知
 与CO2结构相似,①
与CO2结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③SeO3分子内的键角
、③SeO3分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)推算HCN分子中σ键与π键数目之比为
(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
A.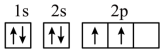 | B.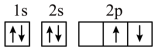 |
C.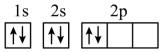 | D.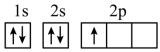 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】储氢材料的研究和应用是科学家努力攻克的课题。钛锰合金即是一种金属氢化物储氢材料。
(1)锰原子在基态时,核外电子排布式为______________________ ;
(2)一种钛的氧化物晶胞结构如图,则该化合物的化学式为___________ ;

(3)钙钛矿(CaTiO3)是典型的立方晶胞:Ca2+处于立方晶胞中心,Ti3+处于立方晶胞顶点,由于O2-处于立方晶胞的______ 形成两种不同的结构。相应的两种结构中每个Ti3+分别与______ 或_____ 个O2-配位。
(4)科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2 HCOONa+H2O
HCOONa+H2O
1 mol NaHCO3中含有δ键的数目为________ ;
HCOONa中碳原子轨道的杂化类型是________ 。
(1)锰原子在基态时,核外电子排布式为
(2)一种钛的氧化物晶胞结构如图,则该化合物的化学式为

(3)钙钛矿(CaTiO3)是典型的立方晶胞:Ca2+处于立方晶胞中心,Ti3+处于立方晶胞顶点,由于O2-处于立方晶胞的
(4)科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2
 HCOONa+H2O
HCOONa+H2O1 mol NaHCO3中含有δ键的数目为
HCOONa中碳原子轨道的杂化类型是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在HF、H2S、PH3、CS2、CCl4、H2O2、N2分子中:(将所选的物质化学式填入空白)
(1)以非极性键结合的非极性分子是_______
(2)以极性键相结合,具有直线型结构的非极性分子是_______
(3)以极性键相结合,具有正四面体结构的非极性分子是_______
(4)以极性键相结合,具有三角锥型结构的极性分子是______
(5)以极性键相结合,具有V型结构的极性分子是_______
(6)以极性键相结合,而且分子极性最大的是_______
(7)与N2O互为等电子体的是_________
(8)含有非极性键的极性分子是________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是
(6)以极性键相结合,而且分子极性最大的是
(7)与N2O互为等电子体的是
(8)含有非极性键的极性分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.有以下物质:①HF ②Cl2 ③H2O ④N2 ⑤C2H4
(1)只含有极性键的是_______ 。
(2)只含有非极性键的是_______ 。
(3)既有极性键又有非极性键的是_______ 。
(4)只含有σ键的是_______ 。
(5)既有σ键又有π键的是_______ 。
(6)属于极性分子的是_______ 。
(7)属于非极性分子的是_______ 。
(1)只含有极性键的是
(2)只含有非极性键的是
(3)既有极性键又有非极性键的是
(4)只含有σ键的是
(5)既有σ键又有π键的是
(6)属于极性分子的是
(7)属于非极性分子的是
Ⅱ.COCl2分子的结构式为 ,COCl2分子内含有
,COCl2分子内含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】①NH3 ②CO2 ③SiCl4 ④BF3 ⑤C2H4 ⑥H2O2 ⑦Cl2 ⑧P4 ⑨H2S
(1)含极性共价键的非极性分子___________ (填序号,下同)
(2)含非极性共价键的非极性分子___________
(3)含极性共价键的极性分子___________
(4)①NH3中心原子杂化方式___________ 分子的空间构型___________
(5)④BF3中心原子杂化方式___________ 分子的空间构型___________
(1)含极性共价键的非极性分子
(2)含非极性共价键的非极性分子
(3)含极性共价键的极性分子
(4)①NH3中心原子杂化方式
(5)④BF3中心原子杂化方式
您最近一年使用:0次



