NH3可消除NO的污染,反应方程式为:6NO+4NH3=5N2+6H2O。现有NO与NH3的混合物共1mol充分反应,若氧化产物与还原产物质量相差1.4g,(相对原子质量:N:14)则下列判断中正确的是
| A.原混合气体中NO、NH3物质的量之比为4∶1 |
| B.转移电子数为0.6NA |
| C.反应中有4.48LNH3被氧化 |
| D.氧化产物与还原产物物质的量之比为3∶2 |
更新时间:2023-01-10 22:29:07
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
A.反应 中氧化剂和还原剂的化学计量数之比为 中氧化剂和还原剂的化学计量数之比为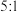 |
B. 的空格内分别为11、15、 的空格内分别为11、15、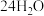 、5、6、15 、5、6、15 |
C.一定条件下,向 溶液中滴加碱性 溶液中滴加碱性 溶液生成纳米铁粉、 溶液生成纳米铁粉、 和 和 的离子方程式为 的离子方程式为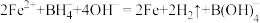 |
D.用酸性 溶液吸收 溶液吸收 生成三种对环境友好物质的化学方程式为 生成三种对环境友好物质的化学方程式为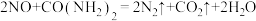 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。下列叙述不正确的是


| A.以上反应中属于氧化还原反应的有①②③④ |
| B.B、C、D分别属于碱性氧化物、碱、盐 |
C.E与C反应的离子方程式为 |
| D.加热5.00gD和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31g,则原混合物中D的质量为4.16g |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列叙述正确的有
①CO2、SiO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4 Cl的反应均既是氧化还原反应,又是吸热反应
⑤需要通电才可进行的有:电离、电解、电镀、电化学腐蚀、电泳
⑥氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸,滴加NaOH溶液都能先生成沉淀后沉淀溶解
⑦苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质
⑧碱石灰、生石灰、玻璃、漂白粉、光导纤维都是混合物
①CO2、SiO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4 Cl的反应均既是氧化还原反应,又是吸热反应
⑤需要通电才可进行的有:电离、电解、电镀、电化学腐蚀、电泳
⑥氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸,滴加NaOH溶液都能先生成沉淀后沉淀溶解
⑦苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质
⑧碱石灰、生石灰、玻璃、漂白粉、光导纤维都是混合物
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】黄铜矿(主要成分CuFeS2)是提取Cu的主要原料。
已知:2CuFeS2+4O2 Cu2S+3SO2+2FeO(Ⅰ)
Cu2S+3SO2+2FeO(Ⅰ)
产物Cu2S在1200 ℃高温下继续反应:2Cu2S+3O2==2Cu2O+2SO2 (Ⅱ)
2Cu2O+Cu2S==6Cu +SO2 ↑ (Ⅲ)
假定各步反应都完全。则下列说法正确的是
已知:2CuFeS2+4O2
 Cu2S+3SO2+2FeO(Ⅰ)
Cu2S+3SO2+2FeO(Ⅰ)产物Cu2S在1200 ℃高温下继续反应:2Cu2S+3O2==2Cu2O+2SO2 (Ⅱ)
2Cu2O+Cu2S==6Cu +SO2 ↑ (Ⅲ)
假定各步反应都完全。则下列说法正确的是
| A.反应Ⅰ中CuFeS2仅作还原剂 |
| B.取12.5g黄铜矿样品,经测定含3.60g硫,则矿样中CuFeS2质量分数一定为82.8% |
| C.由6molCuFeS2生成6molCu消耗O2的物质的量为14.25mol |
| D.6molCuFeS2和15.75molO2反应,理论上可得到铜的物质的量为3mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略): 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是| A.若省略第一次过滤,会使氨水的用量增加 |
B.“氧化”时,发生的化学方程式: |
C.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
D.“还原”时,每生成1molAg,理论上消耗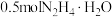 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知:将 通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、
通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、 ,且产物的成分与反应温度有关。常温条件下反应为
,且产物的成分与反应温度有关。常温条件下反应为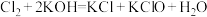 ,加热时反应为
,加热时反应为 ,当
,当 mol时,下列有关说法错误的是
mol时,下列有关说法错误的是
 通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、
通入适量的KOH溶液,反应物恰好完全反应,产物中可能有KCl、KClO、 ,且产物的成分与反应温度有关。常温条件下反应为
,且产物的成分与反应温度有关。常温条件下反应为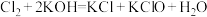 ,加热时反应为
,加热时反应为 ,当
,当 mol时,下列有关说法错误的是
mol时,下列有关说法错误的是| A.参加反应的氯气的物质的量等于0.5a mol |
| B.不管如何改变反应温度,产物中肯定存在KCl |
C.改变反应温度,反应中转移电子的物质的量n的范围是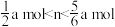 |
D.某温度下反应,若反应后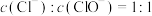 则产物中不可能存在 则产物中不可能存在 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和二氧化氮、一氧化氮的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·L-1氢氧化钠溶液至铜离子恰好完全沉淀,则消耗氢氧化钠溶液的体积是50mL,下列说法正确的是
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
您最近一年使用:0次

 、
、 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。

 过度分解
过度分解 ,可进行循环利用,提高经济效益
,可进行循环利用,提高经济效益
 氧化,每反应lmol GaAs,转移电子的数目为5mol
氧化,每反应lmol GaAs,转移电子的数目为5mol

