X、Y、Z、W四种元素位于元素周期表前四周期,原子序数依次增大。基态X原子价电子排布式为 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
(1) 分子的空间构型为
分子的空间构型为_______ 。
(2)阴离子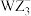 中W原子的杂化类型为
中W原子的杂化类型为_______ 。
(3) 的沸点比Z同主族其他元素氢化物高,原因是
的沸点比Z同主族其他元素氢化物高,原因是_______ 。
(4) 分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为_______ 。
 ;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。
;基态Z原子核外电子有三个能级,p电子总数与s电子总数相等;W是第三周期电负性最大的元素。(1)
 分子的空间构型为
分子的空间构型为(2)阴离子
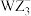 中W原子的杂化类型为
中W原子的杂化类型为(3)
 的沸点比Z同主族其他元素氢化物高,原因是
的沸点比Z同主族其他元素氢化物高,原因是(4)
 分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
分子中各原子都满足最外层8电子结构,分子中π键与σ键数目之比为
更新时间:2023-01-11 11:51:41
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】金属镍在工业上应用广泛,请回答下列问题。
(1) Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是____ (用元素符号表示)。
(2) 过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=____ 。与CO互为等电子体的阴离子是____ (只写一种),CO分子内σ键与π键个数之比为____ 。1mol Ni(CO)n中含σ键为____ mol。
(3) 甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醛分子内C原子的杂化方式为____ ,甲醇分子内的O—C—H键角____ (填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(1) Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
(2) 过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(3) 甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醛分子内C原子的杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
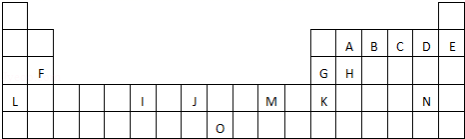
试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为___ , 在周期表中位于______ 区。
(2)写出基态时J元素基态原子原子的价电子排布式_______________ ,J在周期表中的位置是______ 。
(3)ABGH的原子半径由大到小顺序是________________ ;ABCD的第一电离能由大到小顺序是_______ ;ABCD的电负性由大到小顺序是_____________ 。

试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为
(2)写出基态时J元素基态原子原子的价电子排布式
(3)ABGH的原子半径由大到小顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:下图甲表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为___________ (用元素符号表示);
(2)元素b的单质的一个分子中含有___________ 个σ键和___________ 个π键;
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点___________ 乙的熔点(填>或<);
(4)元素d的基态原子的价电子排布式为___________ ;
(5)元素c和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为___________ ,丙的晶体类型为___________ ,在丙中,每个e原子周围最近的e原子数目为___________ 。
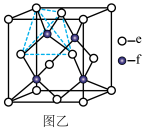

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为
(2)元素b的单质的一个分子中含有
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点
(4)元素d的基态原子的价电子排布式为
(5)元素c和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳及其化合物广泛存在于自然界中,回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,原因是_______ 。
(2)CS2分子中,共价键的类型有_______ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______ 。
(3)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_______ 晶体。
(1)碳在形成化合物时,其键型以共价键为主,原因是
(2)CS2分子中,共价键的类型有
(3)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请依据相关化学知识与原理完成下列各题。
(1)下列一组微粒中键角按由大到小的顺序排列为___________ (填编号)。
①HCN ② ③
③ ④
④  ⑤
⑤
(2) 、
、 、
、 、
、 中,Cl都是以
中,Cl都是以 杂化轨道方式与O原子成键,将它们的立体构型填入表格中:
杂化轨道方式与O原子成键,将它们的立体构型填入表格中:
(3)S单质的常见形式为 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是___________ 杂化。
(4)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。 分子中氮原子轨道的杂化类型是
分子中氮原子轨道的杂化类型是___________ 杂化, 中的六个原子
中的六个原子___________ (填“在”或“不在”)同一个平面上。
(1)下列一组微粒中键角按由大到小的顺序排列为
①HCN ②
 ③
③ ④
④  ⑤
⑤
(2)
 、
、 、
、 、
、 中,Cl都是以
中,Cl都是以 杂化轨道方式与O原子成键,将它们的立体构型填入表格中:
杂化轨道方式与O原子成键,将它们的立体构型填入表格中:| 离子 |  |  |  |  |
| 立体构型 |
(3)S单质的常见形式为
 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是
(4)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。 分子中氮原子轨道的杂化类型是
分子中氮原子轨道的杂化类型是 中的六个原子
中的六个原子
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.有以下物质:①HF、②Cl2、③H2O、④N2、⑤C2H4、⑥C2H6、⑦H2、⑧H2O2和⑨HCN。
(1)只含有σ键的是______ (填序号,下同);既含有σ键又含有π键的是______ 。
(2)含有由两个原子的s轨道重叠形成σ键的是______ 。
(3)写出以下分子或离子的空间构型:NH3:______ ,H2O:______ , SO2:______ ,BeCl2:______ ,CO2:______ 。
II.钴的一种配位聚合物的化学式为{[Co(bte)2(H2O)2](NO3)2}n。
(1)Co2+基态核外电子排布式为______ ;NO 的空间结构为
的空间结构为______ 。
(2)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是______ 和______ (填元素符号)。
②C、H、N的电负性从大到小顺序为______ 。
③bte分子中碳原子轨道杂化类型为______ 和______ 。
④1mol bte分子中含 键的数目为
键的数目为______ mol。
(1)只含有σ键的是
(2)含有由两个原子的s轨道重叠形成σ键的是
(3)写出以下分子或离子的空间构型:NH3:
II.钴的一种配位聚合物的化学式为{[Co(bte)2(H2O)2](NO3)2}n。
(1)Co2+基态核外电子排布式为
 的空间结构为
的空间结构为(2)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是
②C、H、N的电负性从大到小顺序为
③bte分子中碳原子轨道杂化类型为
④1mol bte分子中含
 键的数目为
键的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某有机化合物A在食品,医药等领域中有广泛应用,研究有机化合物A的分子结构,性质如下:
(1)确定A的分子式
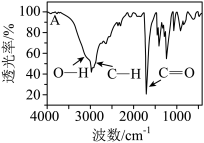
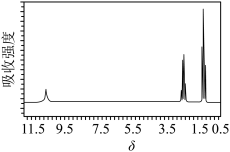
已知该物质含C、H、O三种元素,经元素分析得到有机化合物A的分子内各元素原子个数比N(C)∶N(H)∶N(O)是3∶6∶2,欲确定其分子式还需利用___________ (填仪器名称),测得图谱如下图所示,则该物质分子式为___________ 。
使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:
有机化合物A的结构简式为___________ ,所属的有机化合物类别是___________ 。
(3)研究A的结构和性质的关系
①已知:电离常数 ,
,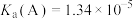 ,分析数据可知A的酸性略弱于乙酸,请从共价键极性的角度解释原因
,分析数据可知A的酸性略弱于乙酸,请从共价键极性的角度解释原因___________ 。
②有机化合物A的同分异构体属于酯类的有___________ 种。
③常温下有机化合物A为液体,面氨基乙酸(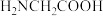 )为固体,请解释其主要原因
)为固体,请解释其主要原因_____ 。
(1)确定A的分子式
已知该物质含C、H、O三种元素,经元素分析得到有机化合物A的分子内各元素原子个数比N(C)∶N(H)∶N(O)是3∶6∶2,欲确定其分子式还需利用

使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:
| 谱图 | 数据分析结果 | |
| 红外光谱 |
| 含有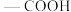 |
| 核磁共振氢谱 |
| 峰面积比为1:2:3 |
(3)研究A的结构和性质的关系
①已知:电离常数
 ,
,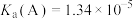 ,分析数据可知A的酸性略弱于乙酸,请从共价键极性的角度解释原因
,分析数据可知A的酸性略弱于乙酸,请从共价键极性的角度解释原因②有机化合物A的同分异构体属于酯类的有
③常温下有机化合物A为液体,面氨基乙酸(
 )为固体,请解释其主要原因
)为固体,请解释其主要原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点
(5)晶体Zn为六方最密堆积,其配位数是
(6)在硒化锌ZnSe晶胞中,Se2—离子作面心立方最密堆积,且Se2—与Se2—之间的最短距离为a nm,则晶胞边长为
(7)假设阿伏伽德罗常数值为NA,则144g 硒化锌ZnSe晶体中的晶胞数是
您最近一年使用:0次

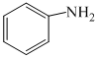 )与甲苯(
)与甲苯(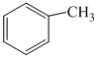 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是

