中国对新冠疫情的防控在世界上得到广泛的认同,其中消毒是重要的措施。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。
(1)84 消毒液是一种常用消毒剂,写出工业上用氯气制备 84 消毒液的离子方程式_______ 。
(2)二氧化氯是一种高效消毒剂。工业制备 ClO2的反应为: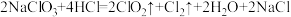
①用单线桥表示电子转移的方向和数目_______ 。
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为 Cl-的是
转化为 Cl-的是_______ (填字母)。
a.O3 b.FeSO4 c.KI d.KMnO4
③常温常压下,ClO2的消毒能力是等物质的量Cl2的_______ 倍(假设 ClO2、Cl2全部被还原为 Cl-,没有其它的含氯产物生成)。
(3)亚氯酸钠(NaClO2)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
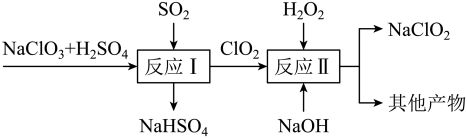
①反应 I 的还原产物是_______ (写化学式)。
②写出反应 II 的化学方程式_______ 。
(1)84 消毒液是一种常用消毒剂,写出工业上用氯气制备 84 消毒液的离子方程式
(2)二氧化氯是一种高效消毒剂。工业制备 ClO2的反应为:
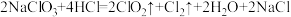
①用单线桥表示电子转移的方向和数目
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为 Cl-的是
转化为 Cl-的是a.O3 b.FeSO4 c.KI d.KMnO4
③常温常压下,ClO2的消毒能力是等物质的量Cl2的
(3)亚氯酸钠(NaClO2)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:

①反应 I 的还原产物是
②写出反应 II 的化学方程式
更新时间:2023-01-12 17:33:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的结构式为___________ 。
(2)美国加利福尼亚大学圣地亚哥的G· N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功。该反应的热化学方程式为___________ 。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=___________ ;联氨和N2O4可作为火箭推进剂的主要原因为___________ 。
(4)火箭推进器中还可以装联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知16 g联氨与足量过氧化氢反应生成氮气和水蒸气,放出321kJ的热量,写出该反应的热化学方程式___________ 。
(5)联氨常由氨气和次氯酸钠溶液反应制得,写出该反应的离子方程式___________ 。
(6)在高温下,N2H4可完全分解为NH3、N2及H2 ,实验测得分解产物中N2与H2的物质的量之比为3:2,则该分解反应的化学方程式为___________ 。
(7)联氨为二元弱碱,在水中的电离方式与氨气相似。写出联氨与过量盐酸反应的离子方程式___________ 。
(1)联氨分子的结构式为
(2)美国加利福尼亚大学圣地亚哥的G· N·SChrauzer等人用氮气和水蒸气在触媒上,光照射下合成高能气态联氨初获成功。该反应的热化学方程式为
| 化学键 | N-H | H-O | O=O | N≡N | N-N |
| 键能/KJ·mol-1 | 391 | 463 | 496 | 946 | 159 |
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ·mol-1
上述反应热效应之间的关系式为ΔH4=
(4)火箭推进器中还可以装联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知16 g联氨与足量过氧化氢反应生成氮气和水蒸气,放出321kJ的热量,写出该反应的热化学方程式
(5)联氨常由氨气和次氯酸钠溶液反应制得,写出该反应的离子方程式
(6)在高温下,N2H4可完全分解为NH3、N2及H2 ,实验测得分解产物中N2与H2的物质的量之比为3:2,则该分解反应的化学方程式为
(7)联氨为二元弱碱,在水中的电离方式与氨气相似。写出联氨与过量盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用Al-CO2电池(工作原理如下图所示)能有效地将CO2转化成化工原料草酸铝。
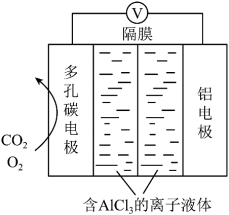
(1)电池的总反应式为_______ 。
(2)电池的正极反应式:2CO2+2e-=C2O (草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
①6O2+6e-=6O
②……
写出反应②的离子方程式:_______ 。

(1)电池的总反应式为
(2)电池的正极反应式:2CO2+2e-=C2O
 (草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:①6O2+6e-=6O

②……
写出反应②的离子方程式:
您最近一年使用:0次
【推荐3】下列四个反应
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g) CO+H2
CO+H2
试从氧化还原的角度,回答下列问题:
(1)水只作还原剂的是__________________ (填序号)
(2)二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是____________ ,生成1.25mol氧化产物共转移电子_________ mol。写出该反应的离子方程式_____________ 。
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g)
 CO+H2
CO+H2试从氧化还原的角度,回答下列问题:
(1)水只作还原剂的是
(2)二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是
您最近一年使用:0次
【推荐1】分析以下A~D四个涉及H2O2的反应(未配平),填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是__ ,H2O2仅体现还原性的反应是___ ,H2O2既体现氧化性,又体现还原性的反应是___ ,H2O2既不作氧化剂又不作还原剂的反应是___ (填序号)。
(2)用单线桥法表示D反应中电子转移的方向和数目:___ 。
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是___ ,氧化产物是___ 。
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:___ 。
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:___ 。
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:___ 。
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是
(2)用单线桥法表示D反应中电子转移的方向和数目:
3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
该反应中氧化剂是
(3)配平下列反应的化学方程式
①P+CuSO4+H2O=Cu+H3PO4+H2SO4:
②FeSO4+H2O+O2=Fe2(SO4)3+Fe(OH)3↓:
③C6H12O6+NaClO3+H2SO4=ClO2↑+CO2↑+H2O+Na2SO4:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用“双桥法”表示下列氧化还原反应中电子转移的方向和数目,并指出氧化剂和还原剂。2KClO3 === 2KCl+3O2↑ _______ 氧化剂_____ 还原剂_____
您最近一年使用:0次
【推荐3】填空。
(1)请用双线桥法表示反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O的电子转移:_______ 。该反应的氧化剂是_______ ,氧化产物是_______ ,若该反应转移的电子数是3mol,则生成的NO气体的体积是_______ L(标准状况下),被还原硝酸的物质的量是_______ mol。
(2)一种制备高效氧化型漂白剂NaClO2的实验流程如图所示
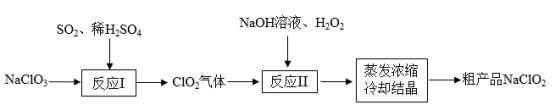
①反应Ⅰ的化学方程式为:3NaClO3+4SO2+3H2O=2ClO2+Na2SO4+3H2SO4+NaCl;反应Ⅰ中氧化产物和还原产物物质的量之比为_______ ,反应Ⅱ中H2O2做_______ (填“氧化剂”或“还原剂”)
②写出NaClO2的电离方程式:_____ ;该漂白剂与HClO的漂白原理______ 相同(填“是”或“否”)
(1)请用双线桥法表示反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O的电子转移:
(2)一种制备高效氧化型漂白剂NaClO2的实验流程如图所示

①反应Ⅰ的化学方程式为:3NaClO3+4SO2+3H2O=2ClO2+Na2SO4+3H2SO4+NaCl;反应Ⅰ中氧化产物和还原产物物质的量之比为
②写出NaClO2的电离方程式:
您最近一年使用:0次
【推荐1】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:

(1)保存过氧化氢的试剂瓶上最适合贴的标签是_____________ (填字母)。
(2)下列反应中,H2O2体现还原性的是______________ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
D.K2Cr2O7+4H2O2+2H+ =2CrO5+5H2O[CrO5称为过氧化铬,可写成CrO(O2)2]
(3)采矿废液中的氰化物(如KCN)一般用H2O2做无毒化处理,化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑(KCN中N为﹣3价),生成1mol NH3时转移的电子数为___________ 。
(4)H2O2被称为绿色氧化剂的理由是_____________________________________ 。

(1)保存过氧化氢的试剂瓶上最适合贴的标签是
(2)下列反应中,H2O2体现还原性的是
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
D.K2Cr2O7+4H2O2+2H+ =2CrO5+5H2O[CrO5称为过氧化铬,可写成CrO(O2)2]
(3)采矿废液中的氰化物(如KCN)一般用H2O2做无毒化处理,化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑(KCN中N为﹣3价),生成1mol NH3时转移的电子数为
(4)H2O2被称为绿色氧化剂的理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高锰酸钾( )和过氧化氢(
)和过氧化氢( )在化学品生产中广泛用作氧化剂。在医药和水处理等领域还用作防腐剂、消毒剂、漂白剂等。已知
)在化学品生产中广泛用作氧化剂。在医药和水处理等领域还用作防腐剂、消毒剂、漂白剂等。已知 参与的部分反应如下:
参与的部分反应如下:
A.
B.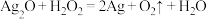
C.
D.
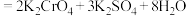
回答下列问题:
(1)上述反应中,不属于氧化还原反应的是___________ (填字母)。
(2)反应D中还原剂是___________ (填化学式)。
(3)反应B中当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为___________  。
。
(4)上述反应说明,一定条件下 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(5)某同学设计实验在某强酸性反应体系中探究 的性质。
的性质。
实验一:向含 的酸性溶液中滴加淀粉
的酸性溶液中滴加淀粉 溶液,溶液变蓝。写出该反应的离子方程式
溶液,溶液变蓝。写出该反应的离子方程式___________ 。
实验二:向含 的溶液中滴加酸性
的溶液中滴加酸性 溶液。已知反应物和生成物共六种粒子:
溶液。已知反应物和生成物共六种粒子: 、
、 、
、 、
、 、
、 、
、 ,且该反应中
,且该反应中 只发生了如下过程:
只发生了如下过程: ,则:
,则:
①实验二的实验现象为a.___________ ;b.有气泡产生。
②该反应应选择下列哪一种酸___________ (填字母)。
a.醋酸b.稀硫酸c.盐酸
 )和过氧化氢(
)和过氧化氢( )在化学品生产中广泛用作氧化剂。在医药和水处理等领域还用作防腐剂、消毒剂、漂白剂等。已知
)在化学品生产中广泛用作氧化剂。在医药和水处理等领域还用作防腐剂、消毒剂、漂白剂等。已知 参与的部分反应如下:
参与的部分反应如下:A.

B.
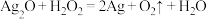
C.

D.

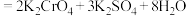
回答下列问题:
(1)上述反应中,不属于氧化还原反应的是
(2)反应D中还原剂是
(3)反应B中当有
 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为 。
。(4)上述反应说明,一定条件下
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)某同学设计实验在某强酸性反应体系中探究
 的性质。
的性质。实验一:向含
 的酸性溶液中滴加淀粉
的酸性溶液中滴加淀粉 溶液,溶液变蓝。写出该反应的离子方程式
溶液,溶液变蓝。写出该反应的离子方程式实验二:向含
 的溶液中滴加酸性
的溶液中滴加酸性 溶液。已知反应物和生成物共六种粒子:
溶液。已知反应物和生成物共六种粒子: 、
、 、
、 、
、 、
、 、
、 ,且该反应中
,且该反应中 只发生了如下过程:
只发生了如下过程: ,则:
,则:①实验二的实验现象为a.
②该反应应选择下列哪一种酸
a.醋酸b.稀硫酸c.盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.按要求写出下列反应的方程式:
(1)碳酸氢铵与少量的氢氧化钠溶液反应(离子方程式)__________ 。
(2)氯化铁溶液中通入二氧化硫气体(离子方程式)__________ 。
(3)一定量的硫酸铝钾加入氢氧化钡溶液生成沉淀质量最大时的反应(化学方程式)__________ 。
(4)碘化亚铁和氯气以5:7的物质的量比反应(化学方程式)__________ 。
Ⅱ.已知Fe2O3在高炉中有下列反应:Fe2O3+CO=2FeO+CO2,反应形成的固体混合物(Fe2O3和FeO)中,元素铁和氧的质量比用m(Fe):m(O)表示。
(1)上述固体混合物中,m(Fe):m(O)可能是____________ 。
a.7:5 b.3:1 c.7:1
(2)设Fe2O3被CO还原的百分率为A%,则用含m(Fe)、m(O)的代数式表示A%的关系式为_________ 。
(1)碳酸氢铵与少量的氢氧化钠溶液反应(离子方程式)
(2)氯化铁溶液中通入二氧化硫气体(离子方程式)
(3)一定量的硫酸铝钾加入氢氧化钡溶液生成沉淀质量最大时的反应(化学方程式)
(4)碘化亚铁和氯气以5:7的物质的量比反应(化学方程式)
Ⅱ.已知Fe2O3在高炉中有下列反应:Fe2O3+CO=2FeO+CO2,反应形成的固体混合物(Fe2O3和FeO)中,元素铁和氧的质量比用m(Fe):m(O)表示。
(1)上述固体混合物中,m(Fe):m(O)可能是
a.7:5 b.3:1 c.7:1
(2)设Fe2O3被CO还原的百分率为A%,则用含m(Fe)、m(O)的代数式表示A%的关系式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多_______ (填数值)。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。
① 的电子式为
的电子式为_______ 。
②Gutzeit试砷法中 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为_______ ;砷化镓也可用于制造太阳能电池,该电池工作时的能量转化形式为_______ 。
(5)已知 的电离平衡常数分别为
的电离平衡常数分别为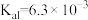 、
、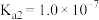 、
、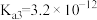 。
。
①25℃时,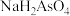 ,溶液中:
,溶液中: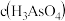
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②25℃时,向 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中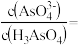
_______ 。
(1)砷只有一种稳定的同位素
 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
A.沸点: |
B.等物质的量浓度溶液的酸性: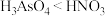 |
C.分解温度: |
D.相对分子质量: |
 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。①
 的电子式为
的电子式为②Gutzeit试砷法中
 被氧化的离子方程式为
被氧化的离子方程式为(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用
 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为(5)已知
 的电离平衡常数分别为
的电离平衡常数分别为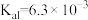 、
、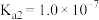 、
、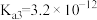 。
。①25℃时,
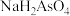 ,溶液中:
,溶液中: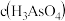
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②25℃时,向
 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中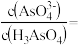
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是______ (写化学式)。
(2)写出并配平该反应的化学方程式:______ ;
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)______ 。
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为______ 。
(1)根据题意,可判断出X是
(2)写出并配平该反应的化学方程式:
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求写出下列离子方程式或化学方程式:
(1)硫酸酸化的高锰酸钾与草酸反应的离子方程式:________ 。
(2)硫代硫酸钠与稀硫酸反应的化学方程式:_________ 。
(3)硫酸酸化的碘化钾溶液与氧气反应的离子方程式:____________ 。
(4)CH3COONa的水溶液呈_______ (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_________ ;
(5)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。常温时的pH_____ 7,该溶液中HSO3-的电离程度______ HSO3-的水解程度。(填“>”、“=”、“<”)
(1)硫酸酸化的高锰酸钾与草酸反应的离子方程式:
(2)硫代硫酸钠与稀硫酸反应的化学方程式:
(3)硫酸酸化的碘化钾溶液与氧气反应的离子方程式:
(4)CH3COONa的水溶液呈
(5)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。常温时的pH
您最近一年使用:0次



