砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多_______ (填数值)。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。
① 的电子式为
的电子式为_______ 。
②Gutzeit试砷法中 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为_______ ;砷化镓也可用于制造太阳能电池,该电池工作时的能量转化形式为_______ 。
(5)已知 的电离平衡常数分别为
的电离平衡常数分别为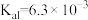 、
、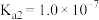 、
、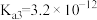 。
。
①25℃时,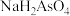 ,溶液中:
,溶液中: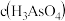
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②25℃时,向 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中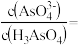
_______ 。
(1)砷只有一种稳定的同位素
 ,其原子核内的中子数比核外电子数多
,其原子核内的中子数比核外电子数多(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(填标号)。
A.沸点: |
B.等物质的量浓度溶液的酸性: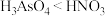 |
C.分解温度: |
D.相对分子质量: |
 (剧毒)转化为
(剧毒)转化为 ,前者让:
,前者让: 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。①
 的电子式为
的电子式为②Gutzeit试砷法中
 被氧化的离子方程式为
被氧化的离子方程式为(4)砷化镓(GaAs)是现代科技中制造芯片的一种原料,可用
 溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为
溶液对其进行刻蚀,As元素的化合价变为+5价,则该反应中还原剂与氧化剂的物质的量之比为(5)已知
 的电离平衡常数分别为
的电离平衡常数分别为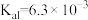 、
、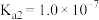 、
、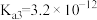 。
。①25℃时,
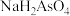 ,溶液中:
,溶液中: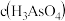
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②25℃时,向
 溶液中加入NaOH溶液至中性,此时溶液中
溶液中加入NaOH溶液至中性,此时溶液中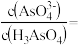
更新时间:2021-12-06 17:11:25
|
相似题推荐
【推荐1】已知NaNO2能发生如下反应(未配平):NaNO2+HI→NO+I2+NaI+H2O
(1)配平方程式,并用单线桥表示电子的转移方向和数目:_______ 。
NaNO2+_______HI—_______NO+_______I2+_______NaI+_______H2O
(2)反应中_______ 元素被氧化(填元素名称),_______ 是氧化剂(填化学式);
(3)氧化产物是_______ (填写化学式,下同),还原产物是_______ 。
(4)反应中,每生成1分子I2,转移的电子数为_______ ;消耗128g还原剂,生成还原产物的质量为_______ 。
(1)配平方程式,并用单线桥表示电子的转移方向和数目:
NaNO2+_______HI—_______NO+_______I2+_______NaI+_______H2O
(2)反应中
(3)氧化产物是
(4)反应中,每生成1分子I2,转移的电子数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2023年10月26日11时14分,神舟十七号载人飞船在酒泉卫星发射中心点火发射。飞船返回地球时,为了减弱返回舱着陆的速度,反推发动机的燃料是高氯酸铵 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
(1)二氧化氯 和过氧化氢均有强氧化性。
和过氧化氢均有强氧化性。
①Cl和O分别形成简单氢化物的稳定性比较_______ >_______
②在酸性条件下,由 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为_______ ;该反应中还原剂与氧化剂的物质的量之比为_______ 。
(2)高氯酸铵中铵根离子的电子式为_______ ;高氯酸铵和铝粉中的元素所形成的简单离子中,核外电子数相同、半径由小到大的顺序是_______ (用离子符号表示)。
(3)氮元素的非金属性较强,N2分子的性质比较稳定,其原因是_______ 。
(4)高氯酸铵和铝粉反应除了生成 和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式_______ 。
 和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:
和铝粉混合物。请回答与高氮酸铵和铝粉相关元素的问题:(1)二氧化氯
 和过氧化氢均有强氧化性。
和过氧化氢均有强氧化性。①Cl和O分别形成简单氢化物的稳定性比较
②在酸性条件下,由
 和双氧水反应制备
和双氧水反应制备 ,其反应的离子方程式为
,其反应的离子方程式为(2)高氯酸铵中铵根离子的电子式为
(3)氮元素的非金属性较强,N2分子的性质比较稳定,其原因是
(4)高氯酸铵和铝粉反应除了生成
 和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
和N2外,还有另外两种不含氮元素的物质生成,请写出其化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于___________ ,因此可以与某些碱反应。
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现___________ 性。
(3)预测FeCl2具有还原性,预测依据是___________ ,因此可以与酸性KMnO4溶液反应。
(4)进行如下实验操作:
①i中的现象是___________ ,用化学方程式表示产生该现象的原因:___________ 、___________ 。
②ii中反应的离子方程式是___________ 。
③iii中的现象是___________ 。
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②___________ , 为证实该反应中Fe2+确实被氧化,需要在反应后的溶液中加入试剂___________ ,观察到现象___________ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
(6)iv中反应的离子方程式是___________ 。
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(9)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________ 。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(3)预测FeCl2具有还原性,预测依据是
(4)进行如下实验操作:
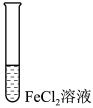 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②ii中反应的离子方程式是
③iii中的现象是
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 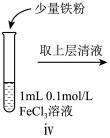 |  | 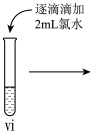 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色, 而后红色褪去 |
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(9)进一步预测SCN-可能被转化为SO
 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为_______ 。
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为_______ 。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_______ (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为_______ 。

注:氢化物指的是由氢元素和另一种元素组成的化合物, CH4就是碳元素的一种氢化物。
(1)X的化学式为
(2)已知SO3是一种酸性氧化物,请写出SO3与NaOH溶液反应的离子方程式为
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
(4)将X与Y混合,可生成硫单质。该反应的氧化剂与还原剂的个数之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:将SO2通入FeCl3溶液中,溶液颜色会变为浅绿色,其原理可表示为:Fe3++SO2+H2O ——Fe2++ +H+
+H+
(1)请配平上述离子方程式_______ ;
(2)若参加反应的SO2在标准状况下的体积为1.12 L,则该反应转移的电子的物质的量为____ mol;
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、 、HNO3的氧化性强弱顺序为
、HNO3的氧化性强弱顺序为_______ 。
 +H+
+H+(1)请配平上述离子方程式
(2)若参加反应的SO2在标准状况下的体积为1.12 L,则该反应转移的电子的物质的量为
(3)已知向Fe2+溶液中滴加少量硝酸时,溶液由浅绿色变为黄色。则Fe3+、
 、HNO3的氧化性强弱顺序为
、HNO3的氧化性强弱顺序为
您最近半年使用:0次
【推荐3】(1)被称为“万能还原剂”的NaBH4溶于水发生反应:NaBH4+2H2O==NaBO2+4H2↑(已知:NaBH4中H为-1价),用双线桥分析电子转移情况:________________________________________ ;
反应中的还原剂是__________ ,被氧化的元素和被还原的元素的质量比是__________
(2)已知8NH3+3Cl2=6NH4Cl+N2反应中电子转移数为1.806×1023,则被氧化的物质的体积是_________ (标准状况)
(3)在一定条件下, RO3n-和氟气发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O。从而可知在RO3n-中,元素R的化合价是________
反应中的还原剂是
(2)已知8NH3+3Cl2=6NH4Cl+N2反应中电子转移数为1.806×1023,则被氧化的物质的体积是
(3)在一定条件下, RO3n-和氟气发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O。从而可知在RO3n-中,元素R的化合价是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
①亚硫酸发生电离的方程式为____________________________________________ 。
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:_____________________ 。
③在相同条件下,试比较 、
、 和
和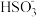 的酸性强弱:
的酸性强弱:_______ > ______ >_______ 。
④将pH=4的 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是______________________ ,图中的纵坐标可以是_______________________ 。
a.溶液的pH b.醋酸的电离平衡常数 c.溶液的导电能力 d.醋酸的电离程度
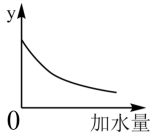
⑤若醋酸的初始浓度为0.01 mol/L,平衡时氢离子浓度是________________________ (写出详细解题步骤)
⑥写出亚硫酸氢钠与碳酸钠反应的离子方程式_________________________
| 酸 | 电离平衡常数 |
| 醋酸 |  |
| 碳酸 |  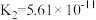 |
| 亚硫酸 | 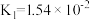  |
①亚硫酸发生电离的方程式为
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:
③在相同条件下,试比较
 、
、 和
和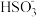 的酸性强弱:
的酸性强弱:④将pH=4的
 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是a.溶液的pH b.醋酸的电离平衡常数 c.溶液的导电能力 d.醋酸的电离程度

⑤若醋酸的初始浓度为0.01 mol/L,平衡时氢离子浓度是
⑥写出亚硫酸氢钠与碳酸钠反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
Ⅰ.常温下向100 mL 0.2 mol·L-l的氨水中逐滴加入0.2mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。

(1)表示NH3·H2O浓度变化的曲銭是____________ (填“A”或“B”)。
(2)NH3·H2O的电离常数为____________ (已知 lg1.8=0.26)。
(3)当加入盐酸体积为50mL时,溶液中c(NH4+)·c(NH3·H2O)=____________ mol·L-1(用数字表示精确值)。
Ⅱ.若液氨中也存在类似水的电离(H2O+H2O H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式__________________________ 。
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式____________________________________ 。
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________________________________ 。
Ⅰ.常温下向100 mL 0.2 mol·L-l的氨水中逐滴加入0.2mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。

(1)表示NH3·H2O浓度变化的曲銭是
(2)NH3·H2O的电离常数为
(3)当加入盐酸体积为50mL时,溶液中c(NH4+)·c(NH3·H2O)=
Ⅱ.若液氨中也存在类似水的电离(H2O+H2O
 H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。(1)写出液氨的电离方程式
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知醋酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO-+H+ K=1.75×10-5。
(1)计算0.01mol/L的CH3COOH溶液的pH=_________ 。(已知lg1.75=0.24)
(2)25℃,将0.1mol/L的CH3COOH溶液和0.1mol/L的NaOH溶液等体积混合后溶液的pH=10,则该混合溶液中由水电离出的c(OH-)=___________ mol/L,写出该混合溶液中下列算式的精确结果(不能做近似计算),c(Na+)-c(CH3COO-)=______________ mol/L。
(3)下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是___________ 。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量镁粉 f.加入少量0.10 mol·L-1的NaOH溶液
(4)SOCl2是一种液态化合物,向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有雾形成,产生可以使品红溶液褪色的气体,往溶液中滴加AgNO3溶液,有白色沉淀析出,请写出SOCl2与水反应的化学方程式______________________________ ,蒸干AlCl3溶液不能得到无水AlCl3,用SOCl2和AlCl3·6H2O混合加热可以得到无水AlCl3,试解释原因______________________
(5)常温下,反应 的平衡常数K=
的平衡常数K=__________ 。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
(1)计算0.01mol/L的CH3COOH溶液的pH=
(2)25℃,将0.1mol/L的CH3COOH溶液和0.1mol/L的NaOH溶液等体积混合后溶液的pH=10,则该混合溶液中由水电离出的c(OH-)=
(3)下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量镁粉 f.加入少量0.10 mol·L-1的NaOH溶液
(4)SOCl2是一种液态化合物,向盛有10mL水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有雾形成,产生可以使品红溶液褪色的气体,往溶液中滴加AgNO3溶液,有白色沉淀析出,请写出SOCl2与水反应的化学方程式
(5)常温下,反应
 的平衡常数K=
的平衡常数K=
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】有X、Y、Z三种短周期元素,已知X原子的L层电子比M层电子多2个; 的电子层结构与Ne的相同;Z与X处于同一周期,其气态单质呈黄绿色。回答下列问题:
的电子层结构与Ne的相同;Z与X处于同一周期,其气态单质呈黄绿色。回答下列问题:
(1)分别写出X、Y、Z元素的名称:_______ 、_______ 、_______ 。
(2)与Z同主族的元素中,氢化物的稳定性最强的是_______ (填化学式)。
(3)与Z元素同周期的元素,形成的含氧酸酸性最强的是_______ (填化学式)。
(4)写出Y单质与氢氧化钠溶液反应的化学方程式:_______ 。
(5)标准状况下,2.24L Z单质与足量氢氧化钙完全反应时,转移电子_______ mol。
(6)22.2g某二价金属与Z形成的化合物中含有0.4mol Z阴离子,则该金属的摩尔质量是_______ g/mol。
 的电子层结构与Ne的相同;Z与X处于同一周期,其气态单质呈黄绿色。回答下列问题:
的电子层结构与Ne的相同;Z与X处于同一周期,其气态单质呈黄绿色。回答下列问题:(1)分别写出X、Y、Z元素的名称:
(2)与Z同主族的元素中,氢化物的稳定性最强的是
(3)与Z元素同周期的元素,形成的含氧酸酸性最强的是
(4)写出Y单质与氢氧化钠溶液反应的化学方程式:
(5)标准状况下,2.24L Z单质与足量氢氧化钙完全反应时,转移电子
(6)22.2g某二价金属与Z形成的化合物中含有0.4mol Z阴离子,则该金属的摩尔质量是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据①~⑧元素的编号所在周期表中的位置,用相应的元素符号 或者化学用语 回答有关问题:
(1)能显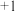 价,还能显
价,还能显 价的元素是
价的元素是_________ 。
(2)最高价氧化物对应水化物是强酸的元素是_________ 。
(3)最难形成化合物的元素是_________ 。
(4)①和④可形成原子数目比为1∶1的化合物,其电子式为_________ 。
(5)③、④、⑤分别与①形成的10电子分子的沸点由低到高的顺序为_________ 。
(6)⑥和⑦最高价氧化物对应水化物相互反应的离子方程式是________ 。
(7)第三周期某元素氢化物(组成为RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为_____ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | |||||
3 | ⑥ | ⑦ | ⑧ |
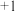 价,还能显
价,还能显 价的元素是
价的元素是(2)最高价氧化物对应水化物是强酸的元素是
(3)最难形成化合物的元素是
(4)①和④可形成原子数目比为1∶1的化合物,其电子式为
(5)③、④、⑤分别与①形成的10电子分子的沸点由低到高的顺序为
(6)⑥和⑦最高价氧化物对应水化物相互反应的离子方程式是
(7)第三周期某元素氢化物(组成为RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表中的一部分,列出10种元素在周期表中的位置,用化学符号回答下列各题。
(1)10种元素中,化学性质最不活泼的是___________ 。
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是___________ 。
(4)元素⑦的氢化物的化学式为___________ 。
(5)①和⑨两元素形成化合物的电子式为___________ :该化合物焰色试验为___________ 色。
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为___________ 。
| 主族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)以上元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子中,离子半径由大到小的顺序是
(4)元素⑦的氢化物的化学式为
(5)①和⑨两元素形成化合物的电子式为
(6)⑤的最高价氧化物与氢氧化钠反应的离子方程式为
您最近半年使用:0次



