用一定浓度的H2SO4溶液分别滴定体积均为20.00mL浓度均为0.200mol•L-1的Ba(OH)2、NaOH和NH3•H2O三种溶液,滴定过程中用传感器测得三种溶液的电导率如图所示。下列说法错误的是
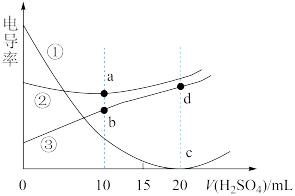

| A.滴定前三种溶液的pH大小关系:Ba(OH)2>NaOH>NH3•H2O |
B.b、d两点的c(NH )大小关系:d=b )大小关系:d=b |
| C.水的电离程度:b>a>d |
| D.H2SO4的浓度为0.200mol•L-1 |
更新时间:2023-01-12 16:19:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液浓度和混合所得溶液的pH如下表所示:
下列说法中,不正确的是
| 实验编号 | c(HA)/ mol·L-1 | c(NaOH)/ mol·L-1 | 混合液的pH |
| ① | 0.2 | 0.1 | pH>7 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.1 | pH=9 |
下列说法中,不正确的是
| A.由实验①可知,HA为弱酸; |
| B.实验①所得混合溶液:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.实验②所得混合溶液:c(Na+)=c(A-) |
| D.实验③所得混合溶液中由水电离出的OH-的浓度为1×10-9mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下,通过下列实验探究 溶液的性质。
溶液的性质。
下列说法错误的是
 溶液的性质。
溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定某种浓度的 溶液的pH,测得pH约为12 溶液的pH,测得pH约为12 |
| 2 | 向 溶液中加入过量的 溶液中加入过量的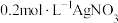 溶液,产生黑色沉淀 溶液,产生黑色沉淀 |
| 3 | 向 溶液中通入 溶液中通入 气体 气体 |
| 4 | 向 溶液中滴加几滴 溶液中滴加几滴 溶液,观察不到明显现象 溶液,观察不到明显现象 |
A. 溶液中存在 溶液中存在 |
B.实验2反应静置后的上层清液中有 |
| C.实验3过程中,水的电离程度逐渐增大 |
D.实验4发生反应的离子方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,同浓度为 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和HA的混合溶液,滴定过程中溶液的pH随
和HA的混合溶液,滴定过程中溶液的pH随 (
(
 )的变化曲线如图所示。下列说法错误的是
)的变化曲线如图所示。下列说法错误的是

 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和HA的混合溶液,滴定过程中溶液的pH随
和HA的混合溶液,滴定过程中溶液的pH随 (
(
 )的变化曲线如图所示。下列说法错误的是
)的变化曲线如图所示。下列说法错误的是
A.HA为弱酸,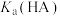 约为 约为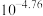 |
B.点c: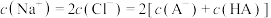 |
C.点b: |
| D.水的电离程度:a<b<c<d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.1mol·L-1氨水滴定10mL浓度均为0.1mol·L-1的HCl和CH3COOH的混合液,已知醋酸的电离常数为Ka=1.8×10-5,下列说法错误的是
| A.在氨水滴定前,混合溶液c(Cl-)>c(CH3COOH) |
| B.在氨水滴定前,混合溶液c(CH3COO-)≈Ka |
C.当滴入氨水10mL时,c( )+c(NH3·H2O)=c(CH3COOH)+c(CH3COO-) )+c(NH3·H2O)=c(CH3COOH)+c(CH3COO-) |
D.当溶液呈中性时,氨水滴入量等于20mL,且c( )<c(Cl-) )<c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】乙二胺四乙酸(EDTA)可与金属离子形成稳定的配合物。常用EDTA测定水中钙含量(EDTA与钙反应时物质的量之比均为1∶1)。基本步骤如下:
①EDTA标定:取10.00 mL 0.1 标准
标准 溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液
溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。
②钙提取:取一定质量的有机物,并用酸性 溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。
对于上述实验,下列说法正确的是
①EDTA标定:取10.00 mL 0.1
 标准
标准 溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液
溶液,加入3滴甲基橙溶液作指示剂,用已配制好的EDTA溶液滴定至终点,消耗EDTA溶液 mL。
mL。②钙提取:取一定质量的有机物,并用酸性
 溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
溶液氧化,再经萃取、反萃取将金属转移到水中,得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液
 mL。
mL。对于上述实验,下列说法正确的是
A.量取标准 溶液时,选用规格为10mL的量筒 溶液时,选用规格为10mL的量筒 |
| B.实验室中萃取、反萃取时,使用的主要仪器为长颈漏斗 |
| C.提取液调pH时,不能使用广泛pH试纸进行测定 |
| D.EDTA滴定时,溶液绿色荧光消失即可判定滴定终点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】电位滴定是利用溶液电位突变指示终点的滴定法。常温下,用cmol·L−1HCl标准溶液测定VmL某生活用品中Na2CO3的含量(假设其它物质均不反应,且不含碳、钠元素),得到滴定过程中溶液电位与V(HCl)的关系如图所示。已知:两个滴定终点时消耗盐酸的体积差可计算出Na2CO3的量。
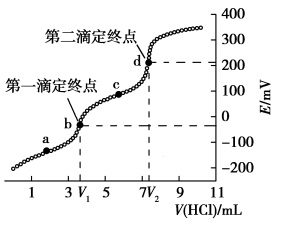
下列说法正确的是

下列说法正确的是
A.a至c点对应溶液中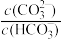 逐渐增大 逐渐增大 |
| B.水的电离程度:a>b>d>c |
C.a溶液中存在:c(Na+)+c(H+)=c( )+2c( )+2c( )+c(OH−) )+c(OH−) |
| D.VmL生活用品中含有Na2CO3的质量为0.106c(V2−V1)g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,向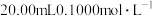 盐酸中滴加
盐酸中滴加 溶液,溶液的
溶液,溶液的 随
随 溶液体积的变化如图。已知
溶液体积的变化如图。已知 。下列说法
。下列说法正确 的是

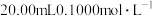 盐酸中滴加
盐酸中滴加 溶液,溶液的
溶液,溶液的 随
随 溶液体积的变化如图。已知
溶液体积的变化如图。已知 。下列说法
。下列说法
| A.当接近终点时,应加快滴定速度便于观察颜色突变 |
B.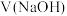 从 从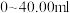 过程中盐酸中水的电离程度先增大后减小 过程中盐酸中水的电离程度先增大后减小 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
D.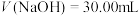 时, 时, |
您最近一年使用:0次

 溶液,②pH=10的Na2S溶液中,由水电离所产生的
溶液,②pH=10的Na2S溶液中,由水电离所产生的 的物质的量之比是
的物质的量之比是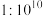
 的氨水溶液,稀释10倍后,其
的氨水溶液,稀释10倍后,其 ,则
,则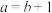

 :①<②<③
:①<②<③ 时,用
时,用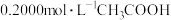 溶液滴定
溶液滴定
 溶液体积的变化如图所示。下列有关说法正确的是
溶液体积的变化如图所示。下列有关说法正确的是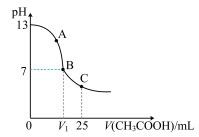
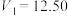
 点处的溶液中:
点处的溶液中:
 过程中,
过程中,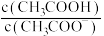 的值逐渐减小
的值逐渐减小 点处的溶液中:
点处的溶液中: