每年10月23日上午6:02到晩上6:02被誉为“摩尔日”(MoleDay),用NA表示阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,92 g NO2气体中含有的原子总数为6NA |
| B.50 mL18 mol/LH2SO4溶液与足量的Cu反应能产生SO2气体分子数为0.45NA |
| C.7.8 g Na2O2中含有阴离子的数目为0.2NA |
| D.1 mol Cl2与足量Fe反应,转移电子数为3NA |
更新时间:2023-01-19 14:26:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.2L 0.5 mol·L—1的亚硫酸溶液中H+数目为2NA |
| B.0.1mol铜与足量浓硝酸反应产生的气体分子数一定为0.2NA个 |
| C.T ℃ 时,1L pH=6的纯水中,含OH—数目为10—8NA个 |
| D.1L 0.1 mol·L—1的NaHCO3溶液中,HCO3—和CO32—离子数目之和小于0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】含有分子数为b的某气体质量为a g,则V L标况下的该气体的质量为(式中NA为阿伏加德罗常数)
A. g g | B. g g |
C. g g | D. g g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醛(HCHO)是室内污染物之一。可利用光催化氧化HCHO为CO2和H2O。下列说法正确的是
| A.1 mol O2含有12 mol电子 |
| B.1 mol HCHO的质量为30 g |
C.光催化氧化甲醛的化学方程式为: |
| D.1 mol H2O(g)的体积为22.4 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知一个SO2分子的质量为n kg,一个SO3分子的质量为m kg(设两种分子中S、O原子分别具有相同的中子数),若以硫原子质量的1/32作标准,SO2的相对分子质量为
A. | B.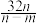 | C.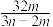 | D.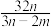 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】可逆反应 N2(g)+3H2(g) 2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
 2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )| A.0.01mol·L-1 | B.0.02mol·L-1 |
| C.0.05mol·L-1 | D.0.15mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 表示阿伏加德罗常数的值。下列说法不正确的是
表示阿伏加德罗常数的值。下列说法不正确的是
 表示阿伏加德罗常数的值。下列说法不正确的是
表示阿伏加德罗常数的值。下列说法不正确的是A.14 g戊烯中含极性键的数目为2 |
B.12.0 g石墨烯(单层石墨)中含有C—C键的数目为3 |
C.已知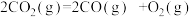 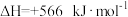 ,则该反应吸热283.0 kJ时产生CO分子的数目为 ,则该反应吸热283.0 kJ时产生CO分子的数目为 |
D.将 和 和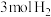 在一定条件下充分反应,产生 在一定条件下充分反应,产生 分子的数目可能是0.6 分子的数目可能是0.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是一种综合处理含SO2尾气的工艺流程。
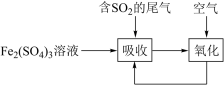
已知“吸收”步骤和“氧化”步骤发生的反应分别为:
①2H2O+ SO2 +Fe2(SO4)3=2FeSO4 +2H2SO4
②4FeSO4 + O2 +2H2SO4 =2Fe2 (SO4)3+2H2O
若每步反应都完全,下列说法正确的是

已知“吸收”步骤和“氧化”步骤发生的反应分别为:
①2H2O+ SO2 +Fe2(SO4)3=2FeSO4 +2H2SO4
②4FeSO4 + O2 +2H2SO4 =2Fe2 (SO4)3+2H2O
若每步反应都完全,下列说法正确的是
| A.“吸收”步骤中Fe2(SO4)3为还原剂 |
B.由反应过程可推知氧化性的强弱顺序:O2>Fe3+> |
| C.处理100L含SO2体积分数为0.336%的尾气,反应①中转移电子0.03mol |
| D.Fe2(SO4)3溶液在上述流程中不可以循环使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】硝酸工业尾气中的NO、NO2可用火碱溶液吸收,有关化学反应为:
① ;
;
②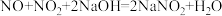 。
。
下列说法错误的是
①
 ;
;②
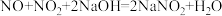 。
。下列说法错误的是
| A.反应①、②均为氧化还原反应 |
| B.反应①中氧化产物与还原产物的物质的量之比为1:1 |
C.若尾气可以被完全吸收,则尾气中 与NO的体积之比可能大于1:1 与NO的体积之比可能大于1:1 |
D.反应②中,生成2 mol  共转移电子的物质的量为2 mol 共转移电子的物质的量为2 mol |
您最近一年使用:0次

 1023个硫酸分子
1023个硫酸分子 )可用作有机合成的催化剂。工业上用黄铜矿(主要成分是
)可用作有机合成的催化剂。工业上用黄铜矿(主要成分是 ,还含有少量
,还含有少量 )制备
)制备

 至少反应消耗
至少反应消耗
 效果更好
效果更好 ,反应的离子方程式为
,反应的离子方程式为
 周围与之距离最近的
周围与之距离最近的

