已知一定温度和压强下,N2(g)和H2 (g)反应生成2molNH3(g),放出92.4kJ热量。在同温同压下向密闭容器中通入1mol N2和3mol H2,达平衡时放出热量为Q1kJ;向另一体积相同的容器中通入0.5molN2和1.5molH2,相同温度下达到平衡时放出热量为Q2kJ。则下列叙述正确的是
| A.2Q2<Q1<92.4kJ | B.2Q2=Q1=92.4kJ |
| C.2Q2>Q1=92.4kJ | D.2Q2=Q1<92.4kJ |
10-11高二上·江西九江·阶段练习 查看更多[5]
(已下线)2010年江西省九江一中高二上学期第一次月考(化学)(已下线)2011—2012学年辽宁省沈阳二中高二上学期10月月考化学试卷山西省吕梁市高级中学2018-2019学年高二上学期期中考试化学试题吉林省白城市通榆县第一中学2019-2020学年高二上学期第一次月考化学试题四川省泸县第四中学2022-2023学年高一下学期5月期中考试化学试题
更新时间:2018-11-29 14:18:02
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知: 





若使46g液态乙醇完全燃烧,最后恢复至室温,则放出的热量为






若使46g液态乙醇完全燃烧,最后恢复至室温,则放出的热量为

A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) ΔH=-452kJ/mol
下列说法正确的是
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) ΔH=-452kJ/mol
下列说法正确的是
| A.28克CO完全燃烧,放出热量为283J |
B.Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=+226kJ/mol O2(g) ΔH=+226kJ/mol |
| C.CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为1.204×1024 |
| D.CO的燃烧热为283kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】  是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。
是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。 在生产生活中具有广泛应用,如可生产
在生产生活中具有广泛应用,如可生产 并进而制得硫酸等,其反应原理为:
并进而制得硫酸等,其反应原理为: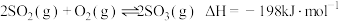 。在一定温度下,体积不变的容器中加入
。在一定温度下,体积不变的容器中加入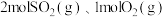 ,发生反应
,发生反应 ,下列说法正确的是
,下列说法正确的是
 是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。
是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。 在生产生活中具有广泛应用,如可生产
在生产生活中具有广泛应用,如可生产 并进而制得硫酸等,其反应原理为:
并进而制得硫酸等,其反应原理为: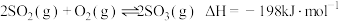 。在一定温度下,体积不变的容器中加入
。在一定温度下,体积不变的容器中加入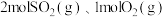 ,发生反应
,发生反应 ,下列说法正确的是
,下列说法正确的是
A.加入 不会影响反应速率 不会影响反应速率 | B.充分反应后,会放出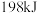 的热量 的热量 |
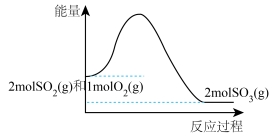
| C.该反应过程中的能量变化如图所示 | D.一段时间后,容器中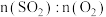 可能为 可能为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】阿伏加德罗常数的值为NA。下列说法正确的是
| A.0.1mol的11B中,含有0.5NA个中子 |
| B.1L0.1mol•L-1Na2S溶液中,阴离子数为0.1NA |
| C.0.1molH2和0.1molI2充分反应后,其分子总数为0.2NA |
| D.标准状况下,2.24L苯完全燃烧,得到0.6NA个CO2分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.向Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| B.实验室用排饱和食盐水的方法收集Cl2 |
C.重铬酸钾溶液中存在:Cr2O (橙色)+H2O (橙色)+H2O 2CrO 2CrO (黄色)+2H+,若滴加少量NaOH溶液,溶液由橙色变黄色 (黄色)+2H+,若滴加少量NaOH溶液,溶液由橙色变黄色 |
| D.实验室保存FeSO4溶液时,常加入少量铁粉 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CO2热还原制CH4和CO。在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4)进行反应,测得CO2转化率、CH4和CO的选择性随温度变化如图所示。
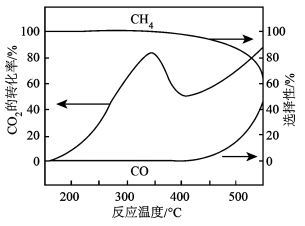
反应I:
反应II: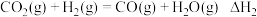
下列说法正确的是

反应I:

反应II:
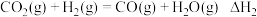
下列说法正确的是
| A.温度为320℃至370℃,CH4的产率降低 |
| B.一定温度下,加入CaO(s)能提高CO的平衡产率 |
| C.其他条件不变,升高温度,CH4的平衡转化率增大 |
D.其他条件不变,在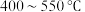 范围,CH4选择性减小是因为反应1平衡逆向移动 范围,CH4选择性减小是因为反应1平衡逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】完成下列实验目的对应的实验操作不正确的是
| 实验目的 | 实验操作 | |
| A | 验证化学反应中的能量变化 | 将NO2球浸泡在冰水、热水中观察颜色变化 |
| B | 探究相同条件下,溶液温度对反应速率的影响 | 在两支试管中各加入5mL0.1mol/L的Na2S2O3和5mL0.1mol/L的H2SO4溶液,再分别放入冷水、热水中,记录出现浑浊所需时间 |
| C | 探究相同条件下,溶液浓度对反应速率的影响 | 在两支试管中各加入4mL0.01mol/L的KMnO4酸性溶液,再分别加入0.1mol/LH2C2O4溶液2mL、0.2mol/LH2C2O4溶液2mL,分别记录溶液褪色所需时间 |
| D | 探究相同条件下,溶液浓度对化学平衡移动的影响 | 在两支试管中各加入5mL0.1mol/L的K2Cr2O7溶液,再分别加入3~10滴浓硫酸和10~20滴6mol/L的NaOH溶液(忽略溶液体积的变化),观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
 CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是| A.容器I、II中正反应速率相同 |
| B.容器I、III中反应的平衡常数相同 |
| C.容器I中CO的物质的量比容器II中的多 |
| D.容器I中CO的转化率与容器II中CO2的转化率之和等于1 |
您最近一年使用:0次
【推荐2】某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数
H2O(g)+CO(g)的平衡常数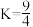 。该温度下在甲、乙、丙三个恒容密闭容器中,
。该温度下在甲、乙、丙三个恒容密闭容器中,
投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
 H2O(g)+CO(g)的平衡常数
H2O(g)+CO(g)的平衡常数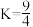 。该温度下在甲、乙、丙三个恒容密闭容器中,
。该温度下在甲、乙、丙三个恒容密闭容器中,| 起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol L-1 L-1 | 0.010 | 0.020 | 0.020 |
c(CO2)/mol L-1 L-1 | 0.010 | 0.010 | 0.020 |
| A.平衡时,乙中CO2的转化率大于60% |
| B.平衡时,甲中和丙中H2的转化率均是60% |
| C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L |
| D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
您最近一年使用:0次

 并通入
并通入 ,发生反应:
,发生反应: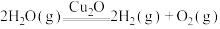
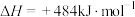 ,不同时间产生
,不同时间产生 的物质的量见下表,下列说法错误的是
的物质的量见下表,下列说法错误的是
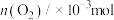
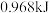
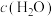 ,可以改变反应的限度
,可以改变反应的限度


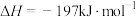 。一定温度下,向甲、乙、丙三个容积相等的恒容密闭容器中投入
。一定温度下,向甲、乙、丙三个容积相等的恒容密闭容器中投入 和
和 ,下列说法正确的是。
,下列说法正确的是。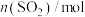
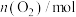


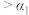
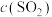 是甲中的2倍
是甲中的2倍

