几种主族元素在周期表中的位置如下:
根据上表回答下列问题:
(1)画出⑩的原子结构示意图:_______ 。
(2)④和⑨两种元素形成的化合物的电子式是_______ 。
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:_______ 。
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
(6)由①、③、⑦组成的化合物中含有的化学键有_______ 。
(7)在含有①、④、⑤简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
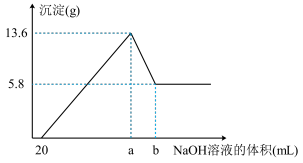
i.沉淀减少时发生的离子方程式:_______ 。
ii.a点的数值为_______  。
。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ④ | ⑤ | ⑧ | ⑨ | |||
| 4 | ③ | ⑩ | ||||||
(1)画出⑩的原子结构示意图:
(2)④和⑨两种元素形成的化合物的电子式是
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
A.②与 反应比④与 反应比④与 反应剧烈 反应剧烈 |
| B.②单质的熔、沸点比④的低 |
| C.②的最高价氧化物对应的水化物的碱性比④的最高价氧化物对应的水化物的碱性强 |
| D.与非金属单质反应时,②原子失电子数目比④原子失电子数目少 |
(7)在含有①、④、⑤简单阳离子的
 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
i.沉淀减少时发生的离子方程式:
ii.a点的数值为
 。
。
更新时间:2023-02-08 09:30:09
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应, 1mol E单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
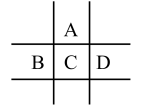
(1)A元素的名称为____________ ,D离子的结构示意图为_____________ 。
(2)C在周期表中的位置为______________________ 。
(3)元素C与元素D相比,非金属性较强的是__________ (用元素符号表示),下列表述中能证明这一事实的是________ 。(填字母序号)
a.常温下C的单质和D的单质状态不同
b.D的气态氢化物比C的气态氢化物稳定
c.一定条件下C和D的单质都能与氢氧化钠溶液反应
d.D的最高价氧化物的水化物的酸性比C的最高价氧化物的水化物的酸性强
e.D的单质能和C的钠盐溶液反应生成C的单质
(4)元素A的一种氢化物含有非极性键,A的这种氢化物的电子式是____________ 。
(5)A、C、D、E元素形成的简单离子半径的大小顺序是________ 。(用离子符号表示)
(6)E的最高价氧化物对应的水化物跟氢氧化钠溶液反应的化学方程式是________________ 。

(1)A元素的名称为
(2)C在周期表中的位置为
(3)元素C与元素D相比,非金属性较强的是
a.常温下C的单质和D的单质状态不同
b.D的气态氢化物比C的气态氢化物稳定
c.一定条件下C和D的单质都能与氢氧化钠溶液反应
d.D的最高价氧化物的水化物的酸性比C的最高价氧化物的水化物的酸性强
e.D的单质能和C的钠盐溶液反应生成C的单质
(4)元素A的一种氢化物含有非极性键,A的这种氢化物的电子式是
(5)A、C、D、E元素形成的简单离子半径的大小顺序是
(6)E的最高价氧化物对应的水化物跟氢氧化钠溶液反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】过渡元素钒、锰、铁、镍等在生活、科研中应用广泛。回答下列问题:
(1)钒广泛应用于航天、化工及能源等行业,与钒同周期且基态原子未成对电子数相同的元素可能位于周期表
(2)
 与水杨醛缩邻氨基苯酚
与水杨醛缩邻氨基苯酚 可形成黄色配合物,应用于科研光度法测定离子浓度。锰在元素周期表中的位置是
可形成黄色配合物,应用于科研光度法测定离子浓度。锰在元素周期表中的位置是 与其同分异构体
与其同分异构体 的结构如图1所示,沸点较高的是
的结构如图1所示,沸点较高的是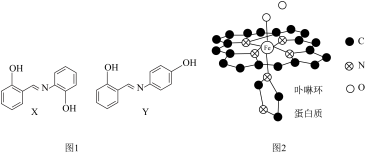
(3)铁是构成血红蛋白的必要成分,血红蛋白携氧后的配合物结构如图2所示(部分氢未画出)。中心
 的配位数为
的配位数为 与血红蛋白中
与血红蛋白中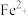 的配位能力
的配位能力 ,原因是
,原因是(4)砷化镍激光在医学上用于治疗皮肤及黏膜创面的感染及溃疡等,人工合成的砷化镍常存在各种缺陷,已知某缺陷砷化镍的组成为
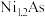 ,其中
,其中 元数只有+2和+3两种价态,则
元数只有+2和+3两种价态,则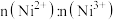 为
为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】现有10种元素的性质、数据如下表所列,它们均为短周期元素.
回答下列问题:
(1)D的元素名称是_______ ,H的元素符号是_______ ,B在元素周期表中的位置是(周期、族)_______ 。
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ .化合物F2A2的电子式是:_______ ,构成该物质的化学键类型为_______ 。
(3)用电子式表示A的简单氢化物的形成过程如下:_______ ;G的氢化物的结构式为_______ 。
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式_______ 。
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:_______ 。
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10﹣10m) | 0.74 | 1.60 | 1.52 | 1.10[ | 0.99 | 1.86 | 0.75 | 0.82 | 0.102 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5[ | +7 | +1 | +5 | +3 | +6 | +1 | |
| ﹣2 | ﹣3 | ﹣1 | ﹣3 | ﹣2 |
(1)D的元素名称是
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)用电子式表示A的简单氢化物的形成过程如下:
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:
您最近一年使用:0次
【推荐1】化合物X(仅含三种短周期元素)是一种络合氢化物的储氢材料,在400℃下隔绝空气加热分解。X中某种元素的单质常用来制作信号弹和烟火。某研究小组为了探究X的组成,设计并完成了如图实验:
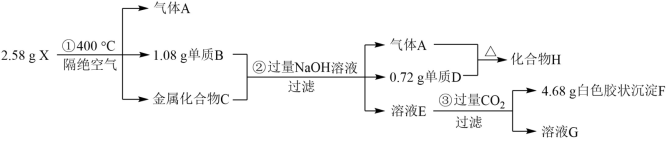
已知A为气体单质,回答下列问题:
(1)X中所含元素为___ (填写元素符号),写出化合物H的化学式___ 。
(2)写出X在400℃下隔绝空气加热分解的化学方程式___ 。
(3)写出溶液E中一种溶质与溶液G反应生成F的离子方程式___ 。
(4)设计实验比较C中两种元素的金属性强弱___ 。
(5)化合物H___ (填“能”或“不能”)与水反应生成H2,理由是___ 。

已知A为气体单质,回答下列问题:
(1)X中所含元素为
(2)写出X在400℃下隔绝空气加热分解的化学方程式
(3)写出溶液E中一种溶质与溶液G反应生成F的离子方程式
(4)设计实验比较C中两种元素的金属性强弱
(5)化合物H
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】高岭土主要由高岭石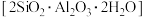 长期风化而成,其中还含有一定量的白云石
长期风化而成,其中还含有一定量的白云石 ,高岭土是制作陶瓷的原料。完成下列填空:
,高岭土是制作陶瓷的原料。完成下列填空:
(1)矿石中除 外的三种非金属元素的原子半径从小到大的顺序是
外的三种非金属元素的原子半径从小到大的顺序是______ 。硅原子的核外电子排布式是___ ,镁原子核外有_________ 种能量不同的电子。
(2)判断 的金属性强于
的金属性强于 的事实是
的事实是____________ 。
a. 的碱性强于
的碱性强于
b. 微溶于水,
微溶于水, 难溶于水
难溶于水
c. 与热水反应,钙比镁剧烈
d. 单质钙保存在煤油里,单质镁不需要
(3) 和
和 同是ⅣA族元素的氧化物,
同是ⅣA族元素的氧化物, 的熔点明显比
的熔点明显比 高的原因是
高的原因是________ 。
(4)氮化硅( )是一种新型陶瓷材料,制备反应如下:
)是一种新型陶瓷材料,制备反应如下: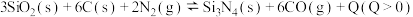 ,该反应的平衡常数表达式
,该反应的平衡常数表达式___________ ;反应达到平衡后,若增大 浓度,则
浓度,则 值
值____________ (填“增大”“减小”或“不变”)。
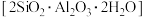 长期风化而成,其中还含有一定量的白云石
长期风化而成,其中还含有一定量的白云石 ,高岭土是制作陶瓷的原料。完成下列填空:
,高岭土是制作陶瓷的原料。完成下列填空:(1)矿石中除
 外的三种非金属元素的原子半径从小到大的顺序是
外的三种非金属元素的原子半径从小到大的顺序是(2)判断
 的金属性强于
的金属性强于 的事实是
的事实是a.
 的碱性强于
的碱性强于
b.
 微溶于水,
微溶于水, 难溶于水
难溶于水c. 与热水反应,钙比镁剧烈
d. 单质钙保存在煤油里,单质镁不需要
(3)
 和
和 同是ⅣA族元素的氧化物,
同是ⅣA族元素的氧化物, 的熔点明显比
的熔点明显比 高的原因是
高的原因是(4)氮化硅(
 )是一种新型陶瓷材料,制备反应如下:
)是一种新型陶瓷材料,制备反应如下: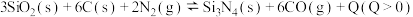 ,该反应的平衡常数表达式
,该反应的平衡常数表达式 浓度,则
浓度,则 值
值
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】第五代隐身战机运用了先进的吸波材料。钡铁氧体是一种应用最广的吸波材料之一。回答下列问题:
(1)铝与钡处于相邻主族,铝的原子核外有_______ 种能量不同的电子。氢氧化铝可以溶于氢氧化钡得到无色溶液,写出离子方程式_______ 。
(2)钡的金属性_______ (大于或小于)铝,下列能比较铝与钡的金属性强弱的是_______ 。
a.高温下铝冶炼钡4BaO+2Al→BaO·Al2O3+3Ba↑
b.铝与水反应需加热,钡与水剧烈反应
c.氧化铝熔点高于氧化钡
(3)某钡铁氧体化学式为BaFe18O27,将其写为氧化物的形式_______ 。将0.030mol该铁氧体溶于2.0mol/L的稀硝酸,恰好溶解时需要硝酸_______ mL。
(4)碳酸钡可用于制钡铁氧体,一种制纳米碳酸钡的原料为BaCl2、NH4HCO3和氨水,从电离平衡的角度分析氨水的作用_______ 。
(5)实验室中,氧化钡是一种高效干燥剂,可以除去乙醚等有机试剂中的少量水,但不能用于除乙酸乙酯中的少量水,原因是_______ 。
(1)铝与钡处于相邻主族,铝的原子核外有
(2)钡的金属性
a.高温下铝冶炼钡4BaO+2Al→BaO·Al2O3+3Ba↑
b.铝与水反应需加热,钡与水剧烈反应
c.氧化铝熔点高于氧化钡
(3)某钡铁氧体化学式为BaFe18O27,将其写为氧化物的形式
(4)碳酸钡可用于制钡铁氧体,一种制纳米碳酸钡的原料为BaCl2、NH4HCO3和氨水,从电离平衡的角度分析氨水的作用
(5)实验室中,氧化钡是一种高效干燥剂,可以除去乙醚等有机试剂中的少量水,但不能用于除乙酸乙酯中的少量水,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性.回答下列问题:
(1)五种元素中,原子半径最大的是_________ ,非金属性最强的是__________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是____________ (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为____________ ;
(4)E的最高价氧化物的水化物的化学式为____________ ;
(5)单质C在空气中燃烧的产物存在的化学键类型为__________ ;其反应化学方程式为___________ ;
(6)单质E与水反应的离子方程式为____________ .
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为
(4)E的最高价氧化物的水化物的化学式为
(5)单质C在空气中燃烧的产物存在的化学键类型为
(6)单质E与水反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
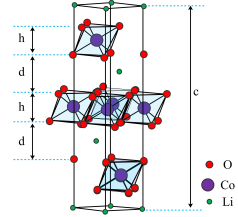
【推荐2】钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如图。晶体中O围绕Co形成八面体,八面体共棱形成带负电的层状空间结构,与Li+层交替排列。在充放电过程中,Li+在层间脱出或嵌入。
(1)下列Li原子电子排布图表示的状态中,能量最低的是______ 。
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是______ 。
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为______ 。
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=______ nm。(列出计算式)
(5)Li+在______ (填“充电”或“放电”)过程中会从八面体层间脱出。该过程会导致晶胞高度c变大,解释原因:______ 。

(1)下列Li原子电子排布图表示的状态中,能量最低的是
A.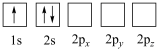 | B.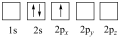 |
C.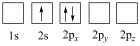 | D. |
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=
(5)Li+在
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】分现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D、C与E分别同主族,D、E、F同周期,B原子的最外层电子数是内层电子数的2.5倍,A与C形成的常见化合物在常温下为液态。
(1)元素A在周期表中的位置是________ ;D、E、F形成的简单离子中半径最大的是_______ (填离子符号)。
(2)常温下,F的单质能与由A、C、D三种元素组成的一种常见化合物发生反应,该反应的化学方程式为________ 。
(3) E与F的最简单气态氢化物中稳定性较强的是________ (填化学式)。
(4)元素B和元素F能形成一种化合物BF3,其中F显+1价。BF3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:________ 。
(1)元素A在周期表中的位置是
(2)常温下,F的单质能与由A、C、D三种元素组成的一种常见化合物发生反应,该反应的化学方程式为
(3) E与F的最简单气态氢化物中稳定性较强的是
(4)元素B和元素F能形成一种化合物BF3,其中F显+1价。BF3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为_______ ; M在元素周期表中的位置为___________________ 。
(2)X与Y按原子个数比1:1构成的物质的电子式为________ ;所含化学键类型________ 。
(3)X+, Y2‾,M2‾ 离子半径大小顺序为________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式_________________________________ 。
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式_________________________ 。
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______________________________ 。
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1:1构成的物质的电子式为
(3)X+, Y2‾,M2‾ 离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下表列出了A﹣R 9种元素在周期表中的位置
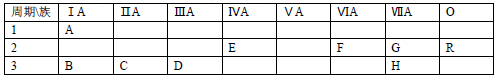
(1)这 9种元素中化学性质最不活泼的是________ (以上均填元素符号)
(2)B、C、D三种元素按原子半径由大到小的顺序排列为________ (用元素符号表示)
(3)F元素简单氢化物的化学式是________ ,H元素跟B元素形成化合物的化学式是______ ,高温灼烧该化合物时,火焰呈________ 色.
(4)G元素和 H元素两者核电荷数之差是________ .

(1)这 9种元素中化学性质最不活泼的是
(2)B、C、D三种元素按原子半径由大到小的顺序排列为
(3)F元素简单氢化物的化学式是
(4)G元素和 H元素两者核电荷数之差是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】A、B、C、D、E、F六种元素均是短周期元素,且原子序数依次增大。B、F原子的最外层电子数均为其电子层数的两倍,D、F元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)转化关系如图(反应条件略去),元素E形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:
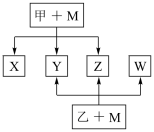
(1)写出M与甲的浓溶液加热时反应的化学方程式___________
(2)X、Y、Z、W属于同一类物质,这类化合物通常熔沸点较___________ (填“高”或“低”); X、Y、W都能与Z反应,则Z的结构式为___________
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=___________ ,写出反应的化学方程式___________
(4)化合物ED2与元素B形成的某种单质能在高温下能发生置换反应,若反应中有1mol电子发生了转移,则参加反应的化合物ED2的质量为___________ g。
(5)元素B的另一种单质能导电,具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12g该单质中含有___________ NA个正六边形。

(1)写出M与甲的浓溶液加热时反应的化学方程式
(2)X、Y、Z、W属于同一类物质,这类化合物通常熔沸点较
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=
(4)化合物ED2与元素B形成的某种单质能在高温下能发生置换反应,若反应中有1mol电子发生了转移,则参加反应的化合物ED2的质量为
(5)元素B的另一种单质能导电,具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12g该单质中含有
您最近一年使用:0次



