过渡元素钒、锰、铁、镍等在生活、科研中应用广泛。回答下列问题:
(1)钒广泛应用于航天、化工及能源等行业,与钒同周期且基态原子未成对电子数相同的元素可能位于周期表
(2)
 与水杨醛缩邻氨基苯酚
与水杨醛缩邻氨基苯酚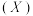 可形成黄色配合物,应用于科研光度法测定离子浓度。锰在元素周期表中的位置是
可形成黄色配合物,应用于科研光度法测定离子浓度。锰在元素周期表中的位置是 与其同分异构体
与其同分异构体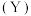 的结构如图1所示,沸点较高的是
的结构如图1所示,沸点较高的是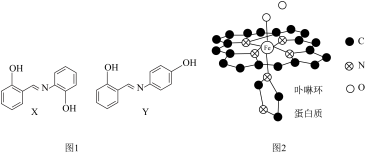
(3)铁是构成血红蛋白的必要成分,血红蛋白携氧后的配合物结构如图2所示(部分氢未画出)。中心
 的配位数为
的配位数为 与血红蛋白中
与血红蛋白中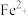 的配位能力
的配位能力 ,原因是
,原因是(4)砷化镍激光在医学上用于治疗皮肤及黏膜创面的感染及溃疡等,人工合成的砷化镍常存在各种缺陷,已知某缺陷砷化镍的组成为
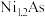 ,其中
,其中 元数只有+2和+3两种价态,则
元数只有+2和+3两种价态,则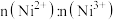 为
为
更新时间:2023-08-03 11:21:36
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)请写出F离子的电子排布式_________ 。
(2)写出X的化学式________ ,X的化学名称为______ 。
(3)写出X涉及化工生产中的一个化学方程式:__________ 。
(4)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:____________ 。
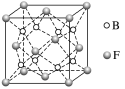
(5)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为__________ ;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是________ (只要求列出算式)。
(1)请写出F离子的电子排布式
(2)写出X的化学式
(3)写出X涉及化工生产中的一个化学方程式:
(4)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
(5)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】[Cu(NH3)4]SO4·H2O是一种重要的染料及合成农药中间体。 请回答下列问题:
(1)[Cu(NH3)4]2+在水溶液中的颜色是________ 。
(2)NH3中N原子的杂化轨道类型是________ 。
(3)Cu2+基态核外电子排布式为_________________ 。
(4)[Cu(NH3)4]SO4中存在的化学键类型除了极性共价键外,还有________ 。
(5)S、O、N三种元素的第一电离能由大到小的顺序为_____________ 。
(6)将金属铜投入到氨水和H2O2的混合溶液中,铜片溶解,溶液是深蓝色,其反应的离子方程式为________ 。
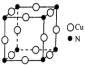
(7)铜氮合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子核间的距离为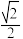 a pm,则该晶体的密度为
a pm,则该晶体的密度为________ g/cm3( 设NA为阿伏伽德罗常数值)。
(1)[Cu(NH3)4]2+在水溶液中的颜色是
(2)NH3中N原子的杂化轨道类型是
(3)Cu2+基态核外电子排布式为
(4)[Cu(NH3)4]SO4中存在的化学键类型除了极性共价键外,还有
(5)S、O、N三种元素的第一电离能由大到小的顺序为
(6)将金属铜投入到氨水和H2O2的混合溶液中,铜片溶解,溶液是深蓝色,其反应的离子方程式为
(7)铜氮合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子核间的距离为
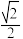 a pm,则该晶体的密度为
a pm,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义。
(1)镍氢电池放电时的总反应为NiOOH+MH=Ni(OH)2+M,M表示储氢合金。基态Ni3+的价层电子排布图为_______ ,Ni3+最高能量的电子的能层符号为____ 。
(2)可用KBH4和NaH2PO4处理储氢合金电极。
①KBH4中阴离子的空间构型是_______ ,写出一种与该阴离子互为等电子体的微粒是_______ 。
②NaH2PO4中各元素的电负性由大到小的顺序为_______ 。NaH2PO4阴离子的中心原子的杂化类型是_______ 。
(3)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示。M是_______ (填元素符号),判断理由为_______ 。
(4)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,晶胞结构如图所示。

①若铁镁合金晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示Fe原子的投影),请在图乙中用实心圆点画出Mg原子的投影位置_____ 。
②储氢时,H2分子在晶胞的体心和棱的中心位置,且最近的两个铁原子之间的距离为dnm,NA表示阿伏加德罗常数的值。则储氢后的晶体密度计算式为____ g/cm3。
(1)镍氢电池放电时的总反应为NiOOH+MH=Ni(OH)2+M,M表示储氢合金。基态Ni3+的价层电子排布图为
(2)可用KBH4和NaH2PO4处理储氢合金电极。
①KBH4中阴离子的空间构型是
②NaH2PO4中各元素的电负性由大到小的顺序为
(3)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示。M是
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |

①若铁镁合金晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示Fe原子的投影),请在图乙中用实心圆点画出Mg原子的投影位置
②储氢时,H2分子在晶胞的体心和棱的中心位置,且最近的两个铁原子之间的距离为dnm,NA表示阿伏加德罗常数的值。则储氢后的晶体密度计算式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】氧族元素Se(硒)及其化合物有着广泛应用价值。
(1)Na2SeSO3(硒代硫酸钠,其中SeSO 可看作是SO
可看作是SO 中的一个O原子被Se原子取代的产物)在某些肿瘤治疗中能够提高治愈率。其制备和转化关系如下:
中的一个O原子被Se原子取代的产物)在某些肿瘤治疗中能够提高治愈率。其制备和转化关系如下:
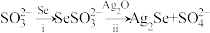
①按照核外电子排布,可把元素周期表划分为5个区。Se位于元素周期表___________ 区。
②SeSO 的空间结构是
的空间结构是___________ 。
③过程ii中SeSO 一定断裂的化学键是
一定断裂的化学键是___________ 。
(2)非铅双钙钛矿材料[(NH4)2SeBr6]有望大规模应用于太阳能电池。一定压力下合成的[(NH4)2SeBr6]晶体的晶胞结构如下图,其中[SeBr6]2-位于正方体的顶点和面心。

①比较Se原子和Br原子的第一电离能大小,并从原子结构的角度说明理由___________ 。
②NH 中H—N—H键角
中H—N—H键角___________ (填“>”或“<”)NH3中H—N—H键角。
③ 一定压力下形成的[(NH4)2SeBr6]晶胞形状为正方体,边长为a nm。已知[(NH4)2SeBr6]的摩尔质量是M g·mol-1,阿伏伽德罗常数为NA,该晶体密度为___________ g·cm-3。(1nm=10-7cm)
(3)Cu2-xSe是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价Cu原子)。
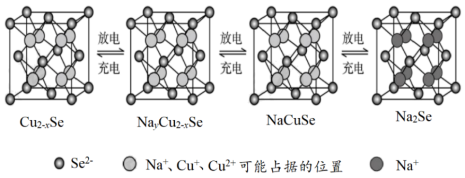
每个Na2Se晶胞完全转化为Cu2-xSe晶胞,转移电子数为___________ 。
(1)Na2SeSO3(硒代硫酸钠,其中SeSO
 可看作是SO
可看作是SO 中的一个O原子被Se原子取代的产物)在某些肿瘤治疗中能够提高治愈率。其制备和转化关系如下:
中的一个O原子被Se原子取代的产物)在某些肿瘤治疗中能够提高治愈率。其制备和转化关系如下: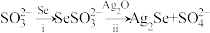
①按照核外电子排布,可把元素周期表划分为5个区。Se位于元素周期表
②SeSO
 的空间结构是
的空间结构是③过程ii中SeSO
 一定断裂的化学键是
一定断裂的化学键是(2)非铅双钙钛矿材料[(NH4)2SeBr6]有望大规模应用于太阳能电池。一定压力下合成的[(NH4)2SeBr6]晶体的晶胞结构如下图,其中[SeBr6]2-位于正方体的顶点和面心。

①比较Se原子和Br原子的第一电离能大小,并从原子结构的角度说明理由
②NH
 中H—N—H键角
中H—N—H键角③ 一定压力下形成的[(NH4)2SeBr6]晶胞形状为正方体,边长为a nm。已知[(NH4)2SeBr6]的摩尔质量是M g·mol-1,阿伏伽德罗常数为NA,该晶体密度为
(3)Cu2-xSe是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价Cu原子)。

每个Na2Se晶胞完全转化为Cu2-xSe晶胞,转移电子数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】如图是部分短周期元素化合价与原子序数的关系图
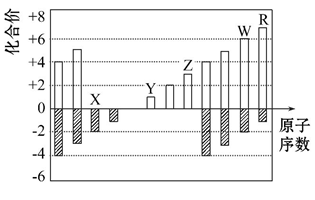
请回答下列问题(用元素符号表达):
(1) X、Y、Z 三种元素的原子半径大小顺序是____________
(2)X 与 Y 形成化合物Y2X2,写出该化合物的电子式____________
(3)RX2是一种强氧化性气体,可用于污水处理,能将 CN-氧化,生成两种无毒气体,该反应离子方程式为____________
(4)某阴离子 Wa2-(a 为2 − 6之间的数字)在碱性溶液中被 BrO3‾离子氧化为 WO42-,而BrO3-离子被还原为Br-,反应中消耗的 BrO3-离子和 OH ‾离子的物质的量之比为 2:3,则 a =____________ 。

请回答下列问题(用元素符号表达):
(1) X、Y、Z 三种元素的原子半径大小顺序是
(2)X 与 Y 形成化合物Y2X2,写出该化合物的电子式
(3)RX2是一种强氧化性气体,可用于污水处理,能将 CN-氧化,生成两种无毒气体,该反应离子方程式为
(4)某阴离子 Wa2-(a 为2 − 6之间的数字)在碱性溶液中被 BrO3‾离子氧化为 WO42-,而BrO3-离子被还原为Br-,反应中消耗的 BrO3-离子和 OH ‾离子的物质的量之比为 2:3,则 a =
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
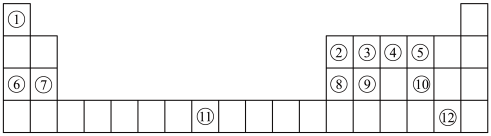
(1)元素①和⑥形成的化合物中存在的化学键类型为_______ 。
(2)用化学方程式表示④的简单氢化物的工业制法_______ 。
(3)写出由③④⑥形成的化合物的电子式_______ 。
(4)列举元素⑨形成的氧化物的一种用途_______ ,元素⑪在周期表中的位置_______ 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为_______ 。
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为_______ 。
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为_______ 。

(1)元素①和⑥形成的化合物中存在的化学键类型为
(2)用化学方程式表示④的简单氢化物的工业制法
(3)写出由③④⑥形成的化合物的电子式
(4)列举元素⑨形成的氧化物的一种用途
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol
 ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】氮及其化合物在生产、环保研究等方面用途非常广泛,回答下列问题:
(1)用浓氨水除去Fe(OH)3样品中少量的Cu(OH)2,生成[Cu(NH3)4]2+,1mol[Cu(NH3)4]2+含______ molσ键。
(2)硝酸厂尾气可以回收制备硝酸。已知:
①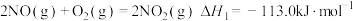
②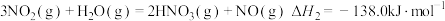
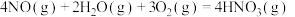 ,
,
______  。
。
(3)在隔绝空气的密闭容器中发生反应:FeSO4(aq)+NO(g) Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
(4)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,反应物和生成物的浓度与温度关系如图所示:______ (填化学式),写出该反应的化学方程式:______ 。
②正反应
______ (填“>”“<”或“=”)0,判断依据是______
③T3℃时NH3的平衡转化率为______ 。
(1)用浓氨水除去Fe(OH)3样品中少量的Cu(OH)2,生成[Cu(NH3)4]2+,1mol[Cu(NH3)4]2+含
(2)硝酸厂尾气可以回收制备硝酸。已知:
①
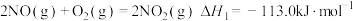
②
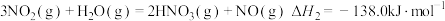
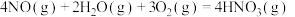 ,
,
 。
。(3)在隔绝空气的密闭容器中发生反应:FeSO4(aq)+NO(g)
 Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)
Fe(NO)SO4(aq)(棕黄色),下列叙述正确的是______。(填标号)| A.溶液颜色不变,反应达到平衡状态 | B.其他条件不变,充入少量O2,平衡不移动 |
| C.其他条件不变,加少量FeSO4,溶液颜色加深 | D.其他条件不变,微热,溶液颜色加深 |
(4)向一恒容密闭容器中充入适量NH3和O2,在一定条件下发生反应,氧化产物是N2、NO、NO2、N2O中的一种,达到平衡时改变温度,反应物和生成物的浓度与温度关系如图所示:

②正反应

③T3℃时NH3的平衡转化率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】根据所学物质结构与性质的知识回答下列问题。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
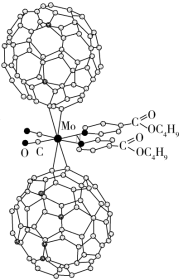
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是___________ ,该超分子中存在的化学键类型有___________ (填选项字母)。
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
②AsF3、IF 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是___________ (填化学式,下同),其立体构型为___________ 。
③室温氟穿梭电池的电解质为氟氢离子液体,含HF 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式___________ 。
④基于CaF2设计的Born-Haber循环如图所示。
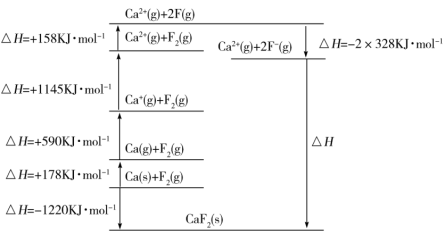
钙的第一电离能为___________ kJ·mol-1;F-F键的键能为___________ kJ·mol-1。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过
②AsF3、IF
 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是③室温氟穿梭电池的电解质为氟氢离子液体,含HF
 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式④基于CaF2设计的Born-Haber循环如图所示。

钙的第一电离能为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】“中国紫”----硅酸铜钡 ( ),其合成原料为
),其合成原料为 、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。回答下列问题:
、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。回答下列问题:
(1)基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有___________ 种;基态 原子的价电子排布式
原子的价电子排布式___________ 。
(2) 中
中 的键角为
的键角为___________ ,与 互为等电子体的分子是
互为等电子体的分子是___________ 。
(3)孔雀石溶于强酸可生成Cu2+,Cu2+与过量氨水可形成配离子 ;Cu2+还可与其他微粒形成配离子,如与乙二胺形成
;Cu2+还可与其他微粒形成配离子,如与乙二胺形成 。
。
①此配离子内部不含有的化学键类型是___________ 。
A.离子键 B.非极性键 C.配位键 D.氢键
② 的VSEPR模型名称为
的VSEPR模型名称为___________ ,比较 键角
键角 小于
小于 ,原因是
,原因是___________ 。
(4) 晶体虽然硬度大,却很容易经锤击而破碎,其原因是
晶体虽然硬度大,却很容易经锤击而破碎,其原因是___________ 。
(5)已知 的立方晶胞结构如图所示,若晶体的密度为
的立方晶胞结构如图所示,若晶体的密度为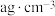 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 与
与 之间最短距离为
之间最短距离为___________ pm(用含a、 的代数式表示)。
的代数式表示)。

 ),其合成原料为
),其合成原料为 、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。回答下列问题:
、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。回答下列问题:(1)基态
 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有 原子的价电子排布式
原子的价电子排布式(2)
 中
中 的键角为
的键角为 互为等电子体的分子是
互为等电子体的分子是(3)孔雀石溶于强酸可生成Cu2+,Cu2+与过量氨水可形成配离子
 ;Cu2+还可与其他微粒形成配离子,如与乙二胺形成
;Cu2+还可与其他微粒形成配离子,如与乙二胺形成 。
。①此配离子内部不含有的化学键类型是
A.离子键 B.非极性键 C.配位键 D.氢键
②
 的VSEPR模型名称为
的VSEPR模型名称为 键角
键角 小于
小于 ,原因是
,原因是(4)
 晶体虽然硬度大,却很容易经锤击而破碎,其原因是
晶体虽然硬度大,却很容易经锤击而破碎,其原因是(5)已知
 的立方晶胞结构如图所示,若晶体的密度为
的立方晶胞结构如图所示,若晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 与
与 之间最短距离为
之间最短距离为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】短周期元素A、B、C、D、E、F、G、H、I、J在周期表中的位置如下:

按要求回答下列问题。
(1)上表元素中,形成气态氢化物最稳定的是_______ 元素(填元素符号)。
(2)32Ge与B同族,32Ge的最高价的氧化物与氢氧化钠反应的化学方程式为
_______ 。
(3)等电子的D、F、G、H四种元素形成的离子,离子半径由大到小的顺序是(填离子符号)
________________________________
(4)D、I元素形成的氢化物中,沸点较高的是_______ ,理由_______ 。
(5)34Se非金属性比D_______ (填“强”或“弱”),从原子结构的角度解释其原因为_______ 。
(6)用电子式表示E、G形成化合物的过程_______ 。

按要求回答下列问题。
(1)上表元素中,形成气态氢化物最稳定的是
(2)32Ge与B同族,32Ge的最高价的氧化物与氢氧化钠反应的化学方程式为
(3)等电子的D、F、G、H四种元素形成的离子,离子半径由大到小的顺序是(填离子符号)
(4)D、I元素形成的氢化物中,沸点较高的是
(5)34Se非金属性比D
(6)用电子式表示E、G形成化合物的过程
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】第IIIA主族元素有着广泛的应用,B可用作特种玻璃,Al可用作火箭和飞机外壳,In可用于电子仪器中,Tl可用于红外技术。回答下列问题:
(1)B能形成很多类似于烃类的物质,B与N元素可形成无机苯B3N3H6,它与苯的结构很相似,该分子中N的杂化方式是_______ 。
(2)电解氧化铝需要添加冰晶石Na3AlF6,它的阴离子的空间结构为_______ ,它可通过以下反应制备:Al(OH)3+3NaOH+6HF=Na3AlF6+6H2O,该反应涉及的5种元素电负性最大的是_______ 。
(3)AlF3、AlCl3熔点分别为1290°C和192°C,熔点呈现如此变化的原因是_______ 。
(4)H3BO3晶体形成层状结构,每一层的结构如下图所示,层与层之间距离为318pm(大于氢键的长度),硼酸晶体属于_______ 晶体,晶体中含有的作用力有_______ ,则1molH3BO3的晶体中有_______ mol氢键。

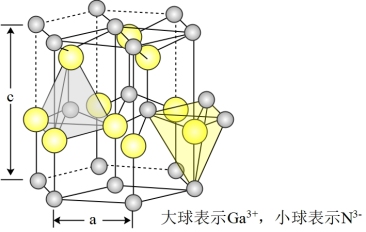
(5)GaN是二元III-VA族的直接带隙半导体,非常适合制造光电器件,GaN具有六方纤锌矿结构,晶胞示意图如下图所示,该晶胞的边长a=318pm,c=517pm。该GaN晶体的密度ρ=_______ g·cm-3。(只列计算式,NA表示阿伏加德罗常数)
(1)B能形成很多类似于烃类的物质,B与N元素可形成无机苯B3N3H6,它与苯的结构很相似,该分子中N的杂化方式是
(2)电解氧化铝需要添加冰晶石Na3AlF6,它的阴离子的空间结构为
(3)AlF3、AlCl3熔点分别为1290°C和192°C,熔点呈现如此变化的原因是
(4)H3BO3晶体形成层状结构,每一层的结构如下图所示,层与层之间距离为318pm(大于氢键的长度),硼酸晶体属于

(5)GaN是二元III-VA族的直接带隙半导体,非常适合制造光电器件,GaN具有六方纤锌矿结构,晶胞示意图如下图所示,该晶胞的边长a=318pm,c=517pm。该GaN晶体的密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为__ 。
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是__ (填元素符号)。
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素称为__ 。
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力__ (“减弱”或“不变”)。
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是_ ;
②CH4和HCHO比较,键角较大的是__ ,主要原因是__ 。
(1)在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为
(2)在3d过渡金属中,基态原子未成对电子数最多的元素是
(3)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素称为
(4)石墨烯限域单原子铁能活化CH4分子中的C-H键,导致C与H之间的作用力
(5)常温下,H2O2氧化CH4生成CH3OH、HCHO、HCOOH等。
①它们的沸点分别为64.7℃、-19.5℃、100.8℃,其主要原因是
②CH4和HCHO比较,键角较大的是
您最近一年使用:0次



