根据所学物质结构与性质的知识回答下列问题。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
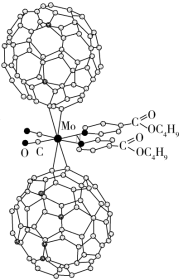
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是___________ ,该超分子中存在的化学键类型有___________ (填选项字母)。
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
②AsF3、IF 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是___________ (填化学式,下同),其立体构型为___________ 。
③室温氟穿梭电池的电解质为氟氢离子液体,含HF 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式___________ 。
④基于CaF2设计的Born-Haber循环如图所示。
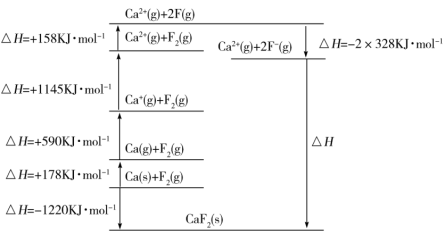
钙的第一电离能为___________ kJ·mol-1;F-F键的键能为___________ kJ·mol-1。
(1)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布图是
A.离子键B.氢键C.σ键D.π键
②该超分子中,配体CO提供孤电子对的原子是
(2)氟及其化合物用途非常广泛。
①聚四氟乙烯是一种准晶体,可通过
②AsF3、IF
 、OF2,BeF2中价层电子对数不同于其它微粒的是
、OF2,BeF2中价层电子对数不同于其它微粒的是③室温氟穿梭电池的电解质为氟氢离子液体,含HF
 、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式
、[(FH)2F]-、[(FH)3F]-等离子,画出[(FH)3F]-的结构式④基于CaF2设计的Born-Haber循环如图所示。

钙的第一电离能为
更新时间:2021-08-30 22:18:17
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途。
请回答下列有关问题:
(1)铜原子的基态电子排布式是____________ 。比较第一电离能Cu______ Zn(填 “>”、“=”、“<”),说明理由___________________ 。
(2)氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为_______ 。(每个球均表示1个原子)

(3)铜可以形成多种多样的配合物。
① NH3可以和很多过渡金属形成配合物。NH3分子中心原子的杂化类型为____ 杂化,与NH3互为等电子体的粒子有___ 。(只写其中一种)
②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。试用离子方程式表示其原因____ 、___ 。
(4)在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键。
请回答下列有关问题:
(1)铜原子的基态电子排布式是
(2)氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为

(3)铜可以形成多种多样的配合物。
① NH3可以和很多过渡金属形成配合物。NH3分子中心原子的杂化类型为
②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。试用离子方程式表示其原因
(4)在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键。

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(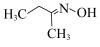 )。回答下列问题:
)。回答下列问题:
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)TiO2和TiCl4均是制备钛硅分子筛的重要中间体。
①TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为
②TiCl4与金属Ti在高温条件下可反应生成TiCl3,TiCl3中Ti3+极易被氧化,还原性很强。试解释Ti3+还原性强的原因
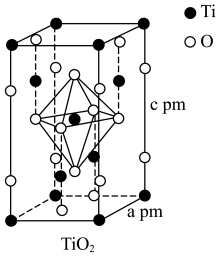
(4)TiO2晶胞如图所示,若其晶体密度为ρg·cm-3,则阿伏加德罗常数的值NA=
您最近一年使用:0次
【推荐3】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A原子的电子只有一种自旋取向,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E的最外层电子数比最内层电子数多1。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
(1)E元素基态原子的简化电子排布式为____ 。F元素基态原子的价电子排布图为____ 。
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为___ 。离子半径:D+___ (填“<”“>”或“=”)B3-。
(3)元素C的简单气态氢化物的沸点____ (填“高于”或“低于”)元素F的简单气态氢化物的沸点,其主要原因是____ 。
(4)元素C与氟元素相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ (填序号字母)。
a.常温下氟气的颜色比C单质的颜色深 b.氟气与C的氢化物剧烈反应,产生C的单质
c.氟与C形成的化合物中C元素呈正价态 d.比较两元素的单质与氢气化合时得电子的数目
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____ 。试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式:____ 。
(6)E元素原子的第一电离能____ 镁(填“>”“<”或“=”),镁燃烧时会产生耀眼的白光,原因是____ 。
(7)元素H的原子核外电子有____ 种空间运动状态,化合物HC在加热条件下容易转化为H2C,从原子结构的角度解释原因____ 。
(1)E元素基态原子的简化电子排布式为
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为
(3)元素C的简单气态氢化物的沸点
(4)元素C与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比C单质的颜色深 b.氟气与C的氢化物剧烈反应,产生C的单质
c.氟与C形成的化合物中C元素呈正价态 d.比较两元素的单质与氢气化合时得电子的数目
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(6)E元素原子的第一电离能
(7)元素H的原子核外电子有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】碳酸二甲酯(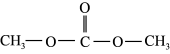 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
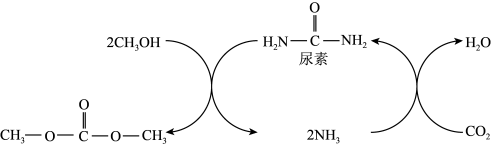
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②_______ 。
(2)下列有关 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。
(3)含钛、铁、铜、锌的催化剂在制备碳酸二甲酯的过程中,催化效果较好。
①基态钛原子核外s能级和p能级的电子数之比为_______ 。
②含钛新型正极材料 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为_______ 。
③已知:存在未成对电子的金属离子具有顺磁性。 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是_______ (填离子符号);这四种金属离子各1mol中,未成对电子数最多的金属离子是_______ (填离子符号)。
④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为_______ 。
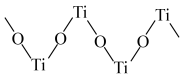
(4)在 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
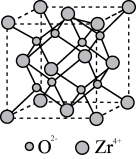
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是_______ 。若该晶胞的密度为 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是_______  (列出计算式)。
(列出计算式)。
 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②
(2)下列有关
 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。A. 的键角小于 的键角小于 的键角,是因为 的键角,是因为 的中心原子上孤电子对对成键电子对有较大的斥力 的中心原子上孤电子对对成键电子对有较大的斥力 |
B. 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 |
C. 的沸点比 的沸点比 的高,是因为N-H键能比P-H键能大 的高,是因为N-H键能比P-H键能大 |
D.1mol 中含有12molσ键 中含有12molσ键 |
①基态钛原子核外s能级和p能级的电子数之比为
②含钛新型正极材料
 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为③已知:存在未成对电子的金属离子具有顺磁性。
 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为

(4)在
 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________ (填标号)。
A.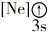 B.
B.
C.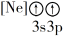 D.
D.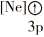
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是___________ 、___________ 。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是___________ ,其中与乙二胺形成的化合物稳定性相对较高的是___________ (填“Mg2+”或“Cu2+”)。
(3)一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因___________ 。
A.
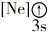 B.
B.
C.
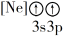 D.
D.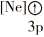
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是
(3)一些氧化物的熔点如下表所示:
| 氧化物 | Li2O | MgO | P4O6 | SO2 |
| 熔点/℃ | 1570 | 2800 | 23.8 | −75.5 |
解释表中氧化物之间熔点差异的原因
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】(1)基态溴原子的价层电子轨道排布式为________ 。第四周期中,与溴原子未成对电子数相同的金属元素有_______ 种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________ (填标号)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________ ;[AlCl4]-的立体构型名称为______ 。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________ 。
A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________ 。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______ 。

(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】五羰基铁是一种黄色液体,熔点-20℃,沸点103℃,可以用细铁粉和 制备,流程如下:
制备,流程如下:
 中含有
中含有 键
键_____  ,配位原子为
,配位原子为_____ 。
(2)下列说法正确的是:_____ 。
A. 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体
B.制备 反应需在隔绝空气下进行
反应需在隔绝空气下进行
C. 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
D.B的分子式为
E.已知在丙酮中 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3) 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为_____ 。
(4)写出反应③的方程式:_____ 。
(5)某实验小组预测 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)_____ 。
 制备,流程如下:
制备,流程如下: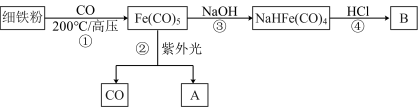

 中含有
中含有 键
键 ,配位原子为
,配位原子为(2)下列说法正确的是:
A.
 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体B.制备
 反应需在隔绝空气下进行
反应需在隔绝空气下进行C.
 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形D.B的分子式为

E.已知在丙酮中
 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3)
 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为(4)写出反应③的方程式:
(5)某实验小组预测
 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】含硫物质在自然界中分布非常广泛,与我们的生活密切相关。回答下列问题:
(1)基态S原子核外电子的空间运动状态有_______ 种。
(2)P、S、Cl第一电离能由大到小的顺序为_______ , 化合物磺酰氯SO2Cl2的空间构型为_______ ,键角∠OSCl_______ ∠ClSCl (填“>”“<”或“=”),原因是_______ 。
(3)SF6是一种无色、无毒、不燃的稳定气体。SF6中心原子的价层电子对数为_______ ,下列对SF6中心原子杂化方式推断合理的是_______ (填标号)。
A. sp2 B. sp3 C. sp3d D. sp3d2
(4)ZnS用作分析试剂、荧光粉的基质和光导体材料,如图是其某种晶胞沿z轴方向在xy平面的投影图,原子旁边标注的数字是该原子位于z轴上的高度(部分相同位置的原子未标注)。Zn2+ 和S2-的最短距离是_______ ,若该晶胞密度是d g·cm-3;则阿伏加德罗常数的值NA=_______ (用含 a、d的式子表示)。

(1)基态S原子核外电子的空间运动状态有
(2)P、S、Cl第一电离能由大到小的顺序为
(3)SF6是一种无色、无毒、不燃的稳定气体。SF6中心原子的价层电子对数为
A. sp2 B. sp3 C. sp3d D. sp3d2
(4)ZnS用作分析试剂、荧光粉的基质和光导体材料,如图是其某种晶胞沿z轴方向在xy平面的投影图,原子旁边标注的数字是该原子位于z轴上的高度(部分相同位置的原子未标注)。Zn2+ 和S2-的最短距离是

您最近一年使用:0次
【推荐3】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为____________
(2)已知HN3是一种弱酸,其在水溶液中的电离方程式为 ,与
,与 互为等电子体的一种分子为:
互为等电子体的一种分子为:_______ , 离子杂化类型为
离子杂化类型为___________ 。
(3)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是___________ ,配位体NH3的空间构型为:___________ 。
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为____________ ,立方体中Fe2+间连接起来形成的空间构型是_____________ 。
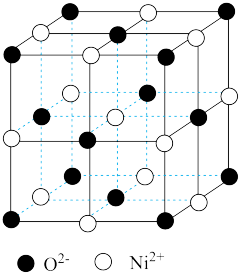
(5)氧化镍和氯化钠的晶体结构相同,可看成镍离子替换钠离子,氧离子替换氯离子。则:
①镍离子的配位数为__________ 。
②若阿伏加 德罗常数的值为NA,晶体密度为ρg·cm-3,则该晶胞中最近的O2-之间的距离为__________ pm(列出表达式)。
(1)基态Co原子的价电子排布式为
(2)已知HN3是一种弱酸,其在水溶液中的电离方程式为
 ,与
,与 互为等电子体的一种分子为:
互为等电子体的一种分子为: 离子杂化类型为
离子杂化类型为(3)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为
(5)氧化镍和氯化钠的晶体结构相同,可看成镍离子替换钠离子,氧离子替换氯离子。则:
①镍离子的配位数为
②若阿伏加 德罗常数的值为NA,晶体密度为ρg·cm-3,则该晶胞中最近的O2-之间的距离为

您最近一年使用:0次
【推荐1】电池级碳酸锂是制造LiCoO2等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含Li+、Fe3+、Mg2+、SO 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:

已知:①HR为有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生的反应可表示为:Fe3++3HR FeR3+3H+;
FeR3+3H+;
②常温时,1mol·L-1LiOH溶液的pH=14。
回答下列问题:
(1)“有机层”的主要成分为___________ (填化学式,下同);“滤渣1”中含有的物质为___________ ;使用HR萃取剂时,需加入一定量的NaOH进行处理,其目的是___________ 。
(2)某种HR的结构简式为 ,该分子中可能与Fe3+形成配位键的原子有
,该分子中可能与Fe3+形成配位键的原子有___________ 。
(3)加适量草酸的目的___________ 。
(4)“混合沉锂”的离子方程式为___________ 。
(5)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式___________ 。
(6)钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如下图所示,各离子位于晶胞的顶点、棱和体内。
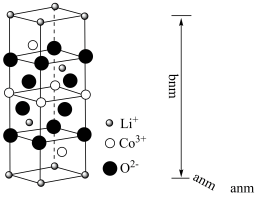
①基态Co原子核外电子排布式为___________ 。
②该晶胞密度为___________ g·cm-3。(写出计算式,阿伏加德罗常数为NA)
 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
已知:①HR为有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生的反应可表示为:Fe3++3HR
 FeR3+3H+;
FeR3+3H+;②常温时,1mol·L-1LiOH溶液的pH=14。
回答下列问题:
(1)“有机层”的主要成分为
(2)某种HR的结构简式为
 ,该分子中可能与Fe3+形成配位键的原子有
,该分子中可能与Fe3+形成配位键的原子有(3)加适量草酸的目的
(4)“混合沉锂”的离子方程式为
(5)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式
(6)钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如下图所示,各离子位于晶胞的顶点、棱和体内。

①基态Co原子核外电子排布式为
②该晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】AA705合金(含 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
(1) 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为_____________________ , 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为_____________________ ;
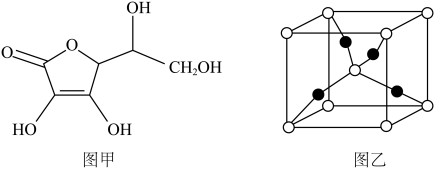
(2)以 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______________ ,推测抗坏血酸在水中的溶解性:_______________ (填“难溶于水”或“易溶于水”),一个 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为_______________ ;
(3) 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含______  键,中心离子的配位数为
键,中心离子的配位数为______________ ;
(4) 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
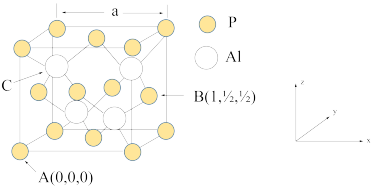
①磷化铝的晶体类型为______________ ,
②A、B点的原子坐标如图所示,则C点的原子坐标为___________ ,
③磷化铝的晶胞参数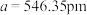 ,其密度为
,其密度为____________  (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);
(5) 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为________________ 。
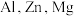 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:(1)
 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为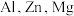 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为(2)以
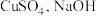 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为
(3)
 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含 键,中心离子的配位数为
键,中心离子的配位数为(4)
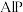 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知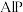 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
①磷化铝的晶体类型为
②A、B点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数
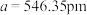 ,其密度为
,其密度为 (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);(5)
 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铁是人体内不可或缺的微量元素,其配合物的研究也是当今科研的重点之一。
 基态Fe原子的价层电子轨道表达式为
基态Fe原子的价层电子轨道表达式为________________________________ ;同周期元素中,基态原子的未成对电子数比Fe多的元素为________  填元素符号
填元素符号 。
。
 常温下,五羰基铁
常温下,五羰基铁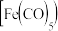 为黄色液体,其晶体类型为
为黄色液体,其晶体类型为________________ ;CO与 互为等电子体,二者中沸点较高的是
互为等电子体,二者中沸点较高的是________ ,原因为________________________ 。
 普鲁士蓝的化学式为
普鲁士蓝的化学式为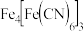 ,碳原子与
,碳原子与 形成配位键,其中提供孤电子对的是
形成配位键,其中提供孤电子对的是________  填元素符号
填元素符号 ,
, 中碳原子的杂化方式为
中碳原子的杂化方式为________ ,1mol普鲁士蓝中所含 键的数目为
键的数目为________________ 。
 邻羟基苯甲醛(
邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛( ) 均能与
) 均能与 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为________________________________________________________ 。
 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为________________ ,晶胞中距离Fe原子最近的S原子有________ 个,若阿伏加 德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为________________________  用含有
用含有 、a、b的代数式表示
、a、b的代数式表示 。
。

 基态Fe原子的价层电子轨道表达式为
基态Fe原子的价层电子轨道表达式为 填元素符号
填元素符号 。
。 常温下,五羰基铁
常温下,五羰基铁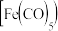 为黄色液体,其晶体类型为
为黄色液体,其晶体类型为 互为等电子体,二者中沸点较高的是
互为等电子体,二者中沸点较高的是 普鲁士蓝的化学式为
普鲁士蓝的化学式为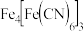 ,碳原子与
,碳原子与 形成配位键,其中提供孤电子对的是
形成配位键,其中提供孤电子对的是 填元素符号
填元素符号 ,
, 中碳原子的杂化方式为
中碳原子的杂化方式为 键的数目为
键的数目为 邻羟基苯甲醛(
邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛( ) 均能与
) 均能与 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为 某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为
某含铁化合物的长方体晶胞结构如图所示,该化合物的化学式为 ,则该晶体的密度为
,则该晶体的密度为 用含有
用含有 、a、b的代数式表示
、a、b的代数式表示 。
。 
您最近一年使用:0次



