五羰基铁是一种黄色液体,熔点-20℃,沸点103℃,可以用细铁粉和 制备,流程如下:
制备,流程如下:
 中含有
中含有 键
键_____  ,配位原子为
,配位原子为_____ 。
(2)下列说法正确的是:_____ 。
A. 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体
B.制备 反应需在隔绝空气下进行
反应需在隔绝空气下进行
C. 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
D.B的分子式为
E.已知在丙酮中 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3) 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为_____ 。
(4)写出反应③的方程式:_____ 。
(5)某实验小组预测 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)_____ 。
 制备,流程如下:
制备,流程如下: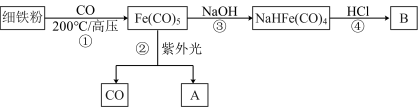

 中含有
中含有 键
键 ,配位原子为
,配位原子为(2)下列说法正确的是:
A.
 中
中 的化合价为0价,为离子晶体
的化合价为0价,为离子晶体B.制备
 反应需在隔绝空气下进行
反应需在隔绝空气下进行C.
 的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形
的结构可以用X射线衍射进行研究,它的空间结构为三角双锥形D.B的分子式为

E.已知在丙酮中
 可以被氯化铜完全氧化,推测产物中有
可以被氯化铜完全氧化,推测产物中有 、
、 和
和
(3)
 在紫外光作用下可以生成
在紫外光作用下可以生成 和化合物A,已知化合物A的1个分子中含有1个
和化合物A,已知化合物A的1个分子中含有1个 键,和3个成桥的羰基,每个
键,和3个成桥的羰基,每个 被6个
被6个 分子以略变形的八面体所包围,则A的分子式为
分子以略变形的八面体所包围,则A的分子式为(4)写出反应③的方程式:
(5)某实验小组预测
 隔绝空气加热产物为
隔绝空气加热产物为 和
和 ,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
,如何设计定量实验证明产物,请设计实验方案:(说明主要试剂和方法即可)
23-24高三上·浙江绍兴·阶段练习 查看更多[3]
浙江省诸暨市2024届高三12月适应性考试化学试题(已下线)专题08 工艺流程综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题11 无机化工流程综合分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
更新时间:2023-12-16 15:26:42
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】锰及其化合物用途非常广泛,也是人体的重要微量元素。请回答下列问题:
(1)锰在元素周期表中的位置为_______ 。
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
(3)锰能形成多种化合物如 、
、 、
、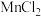 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是_______ 。(已知 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是_______ 原子;该配合物中除氢以外的元素,第一电离能从小到大的顺序为_______ (用元素符号表示)。
(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与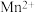 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是_______ (填“A”或“B”),原因是_______ 。
A.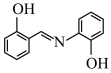 B.
B.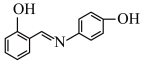
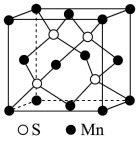
(6)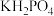 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大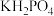 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
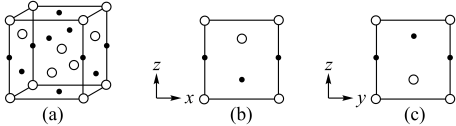
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度_______  (写出表达式)。
(写出表达式)。
②晶胞在x轴方向的投影图为_______ (填标号)。
A.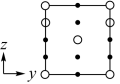 B.
B.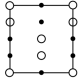 C.
C. D.
D.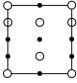
(1)锰在元素周期表中的位置为
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
A.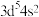 | B.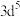 | C.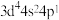 | D.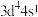 |
 、
、 、
、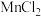 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体
 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与
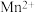 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是A.
 B.
B.

(6)
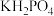 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大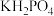 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
,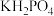 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度
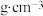 (写出表达式)。
(写出表达式)。②晶胞在x轴方向的投影图为
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】由Sn、V、Gd等元素组成钒基笼目金属在超导电性方面有广阔的应用前景。回答下列问题:
(1)Sn与C同主族,基态Sn原子的价电子排布式为___________ ,Sn和Cl2反应会生成SnCl2和SnCl4。SnCl2(s)以线性聚合状态存在,其结构如图。

Cl-Sn-Cl键角:SnCl2(s)___________ SnCl4(填“>”或“<”),原因是___________ 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为___________ ;钒有+2、+3、+4、+5等多种化合价,从原子结构角度分析最稳定的化合价是___________ ;将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列含V物质中,属于顺磁性物质的是___________ (填标号)。
A.VF4 B.V(NH3)3Cl3 C.Na3VO4 D.Na4[V(CN)6]
(3)已知钒基笼目金属的晶体结构如图。该钒基笼目金属的化学式为___________ ,1号、2号Sn原子间的距离为___________ pm。

(1)Sn与C同主族,基态Sn原子的价电子排布式为

Cl-Sn-Cl键角:SnCl2(s)
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为
A.VF4 B.V(NH3)3Cl3 C.Na3VO4 D.Na4[V(CN)6]
(3)已知钒基笼目金属的晶体结构如图。该钒基笼目金属的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】三元锂电池主要用于手机、无人机等行业,其正极材料为镍钴锰酸锂,电池安全性高。电池工作原理如图所示:(两极之间有一个允许特定的离子 通过的隔膜)
通过的隔膜)

(1)①电池中有三种第四周期元素,其中基态原子未成对电子为5的元素位于周期表第___________ 族,属于___________ 区。
②写出 原子的价层电子排布图
原子的价层电子排布图___________ 。
③比较第二电离能大小
___________  (填“
(填“ ”、“
”、“ ”、“
”、“ ”)。
”)。
(2)电池放电时总反应方程式为: ,写出该电池的正极反应式:
,写出该电池的正极反应式:___________ 。
(3)香港城市大学支春义课题组最近开发出超高容量和能量密度的锌硒电池,工作原理如图所示。

①写出该电池的正极反应式:___________ 。
②外电路中转移 电子时a极增重
电子时a极增重___________ g。
 通过的隔膜)
通过的隔膜)
(1)①电池中有三种第四周期元素,其中基态原子未成对电子为5的元素位于周期表第
②写出
 原子的价层电子排布图
原子的价层电子排布图③比较第二电离能大小

 (填“
(填“ ”、“
”、“ ”、“
”、“ ”)。
”)。(2)电池放电时总反应方程式为:
 ,写出该电池的正极反应式:
,写出该电池的正极反应式:(3)香港城市大学支春义课题组最近开发出超高容量和能量密度的锌硒电池,工作原理如图所示。

①写出该电池的正极反应式:
②外电路中转移
 电子时a极增重
电子时a极增重
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】我国具有悠久的历史,在西汉就有湿法炼铜(Fe+CuSO4=Cu+FeSO4),试回答下列问题。
(1)Cu2+的未成对电子数有______ 个,H、O、S 电负性由大到小的顺序为_______ 。
(2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。[Cu(NH3)4]SO4中化学键类型有_______ ,阴离子中心原子杂化类型为______ 。
(3)铁铜合金晶体类型为_____ ;铁的第三(I3)和第四(I4)电离能分别为2957kJ/mol、5290kJ/mol,比较数据并分析原因________________ 。
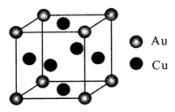
(4)金铜合金的一种晶体结构为立方晶型,如图所示。已知该合金的密度为d g/cm3,阿伏伽德罗常数值为NA,两个金原子间最小间隙为a pm(1pm= 10-10cm)。则铜原子的半径为_______ cm(写出计算表达式)。
(1)Cu2+的未成对电子数有
(2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。[Cu(NH3)4]SO4中化学键类型有
(3)铁铜合金晶体类型为
(4)金铜合金的一种晶体结构为立方晶型,如图所示。已知该合金的密度为d g/cm3,阿伏伽德罗常数值为NA,两个金原子间最小间隙为a pm(1pm= 10-10cm)。则铜原子的半径为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(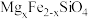 )。回答下列问题:
)。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。橄榄石中,各元素电负性由大到小的顺序为___________ 。
(2)已知一些物质的熔点数据如下表:
① 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是___________ 。
②分析同族元素的氯化物 、
、 、
、 熔点变化趋势的原因
熔点变化趋势的原因___________ 。 的空间结构为
的空间结构为___________ ,其中 的轨道杂化形式为
的轨道杂化形式为___________ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有___________ 个 。该物质化学式为
。该物质化学式为___________ ,B-B最近距离为___________ 。
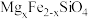 )。回答下列问题:
)。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)已知一些物质的熔点数据如下表:
| 物质 | NaCl | SiCl4 | GeCl4 | SnCl4 |
| 熔点/℃ | 800.7 | -68.8 | -51.5 | -34.1 |
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是②分析同族元素的氯化物
 、
、 、
、 熔点变化趋势的原因
熔点变化趋势的原因 的空间结构为
的空间结构为 的轨道杂化形式为
的轨道杂化形式为(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有
 。该物质化学式为
。该物质化学式为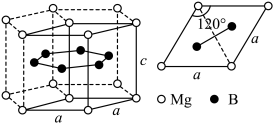
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】金属Mn、Co、Ni、Sb等在电池、储氢材料、催化剂等方面有广泛应用。请回答下列问题:
(1)基态Co原子中,核外电子占据的最高能层的符号是_______ ,基态Ni简化的核外电子排布式为_______ 。
(2)铜锰氧化物( CuMn2O4)能在常温下催化氧化甲醛生成甲酸(结构如图)。
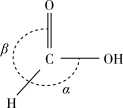
①甲酸的沸点比甲醛的_______ (填“低”或“高”),主要原因是_______ 。
②甲酸分子中O-H键的类型是s-sp3σ键,C-H键的类型是_______ σ键,键角:α_______ β(填“>”“=”或“<”)。
(3)超强酸氟锑酸(结构如图)在化学和化学工业上有很大的应用价值,是活性极高的催化剂。

①该物质中∠FSbF为90°或180° ,则阴离子的空间构型为_______ 。
②阴离子的中心原子的杂化轨道类型是_______ (填序号)。
A. sp3d2 B. sp2 C. sp3 D. sp
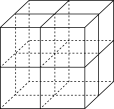
(4)Mg2 NiH4是科学家研究的一种高效固态储氢材料。在Mg2NiH4晶胞中,Ni原子占据如图所示的顶点和面心,Mg2+处于图中八个小立方体的体心。Mg2+和Ni原子的最短距离为d nm,NA为阿伏加德罗常数的值,该晶体的密度为_______ g·cm-3(用含NA、d、M的代数式表示,Mg2NiH4的相对分子质量为M)。
(1)基态Co原子中,核外电子占据的最高能层的符号是
(2)铜锰氧化物( CuMn2O4)能在常温下催化氧化甲醛生成甲酸(结构如图)。

①甲酸的沸点比甲醛的
②甲酸分子中O-H键的类型是s-sp3σ键,C-H键的类型是
(3)超强酸氟锑酸(结构如图)在化学和化学工业上有很大的应用价值,是活性极高的催化剂。

①该物质中∠FSbF为90°或180° ,则阴离子的空间构型为
②阴离子的中心原子的杂化轨道类型是
A. sp3d2 B. sp2 C. sp3 D. sp
(4)Mg2 NiH4是科学家研究的一种高效固态储氢材料。在Mg2NiH4晶胞中,Ni原子占据如图所示的顶点和面心,Mg2+处于图中八个小立方体的体心。Mg2+和Ni原子的最短距离为d nm,NA为阿伏加德罗常数的值,该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】钯(Pd)、锌及其化合物在合成酮类物质中有极其重要的作用,如图为合成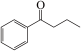 的反应过程:
的反应过程:
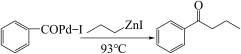
回答下列问题:
(1)I原子价电子排布式为___________ ,其能量最高的能层是___________ (填能层符号)。
(2)H、C、O三种元素的电负性由大到小的顺序为___________ 。
(3)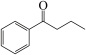 中碳原子的杂化方式为
中碳原子的杂化方式为___________ 。
(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是___________ 。
②NH3的空间构型为___________ 。
③1 mol [Zn(NH3)4]Cl2中含有___________ mol σ键。
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的___________ 。
(6)金属钯的堆积方式如图所示:
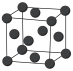
①该晶胞中原子的空间利用率为___________ (用含π的式子表示)。
②若该晶胞参数a=658 pm,则该晶胞密度为___________ (列出计算表达式)g·cm-3。
 的反应过程:
的反应过程:
回答下列问题:
(1)I原子价电子排布式为
(2)H、C、O三种元素的电负性由大到小的顺序为
(3)
 中碳原子的杂化方式为
中碳原子的杂化方式为(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是
②NH3的空间构型为
③1 mol [Zn(NH3)4]Cl2中含有
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的
(6)金属钯的堆积方式如图所示:

①该晶胞中原子的空间利用率为
②若该晶胞参数a=658 pm,则该晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】已知A、B、C、D、E是周期表中前四周期原子序数依次增大的五种元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子;A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体;含E元素的硫酸盐溶液是制备波尔多液的原料之一,按要求回答下列问题:
(1)五种元素中第一电离能最大的是___________ ,电负性最大的是___________ 。(以上两空均填元素名称)
(2)E元素所在周期中基态原子的单电子数最多的元素是___________ 。(填元素符号)
(3)M分子中B原子的轨道杂化类型为___________ ,M分子中两种键角的大小关系是___________ 。(用∠XYZ表示,X、Y、Z代表元素符号)
(4)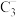 的空间构型为
的空间构型为___________ ;化合物CA3的沸点比BA4的高,其主要原因是___________ 。
(5)向E元素的硫酸盐溶液中通入过量的CA3,得到深蓝色的透明溶液,在此溶液中加入乙醇,析出深蓝色的晶体,此晶体中存在的化学键类型有___________ 。(填代号)
A.离子键 B.σ键 C.非极性共价键 D.配位键 E.金属键 F.氢键
(6)如图是D、E两种元素形成的化合物的晶胞结构示意图,D的配位数为___________ ,已知晶胞中最近两个D原子间距离为a nm,阿伏加德罗常数用NA表示,则该晶体的密度为___________ g/cm3。(用含a、NA的表达式表示)
(1)五种元素中第一电离能最大的是
(2)E元素所在周期中基态原子的单电子数最多的元素是
(3)M分子中B原子的轨道杂化类型为
(4)
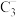 的空间构型为
的空间构型为(5)向E元素的硫酸盐溶液中通入过量的CA3,得到深蓝色的透明溶液,在此溶液中加入乙醇,析出深蓝色的晶体,此晶体中存在的化学键类型有
A.离子键 B.σ键 C.非极性共价键 D.配位键 E.金属键 F.氢键
(6)如图是D、E两种元素形成的化合物的晶胞结构示意图,D的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】CO 易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5; [Cu(NH3)2]Ac 溶液用于除去CO的化学反应方程式:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3] Ac·CO (式中Ac-代表醋酸根)。请回答下列问题:
(1)C、N、O的第一电离能最大的是_____________ ,原因是___________________________ 。基态Fe 原子的价电子排布图为___________________________ 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_____________ ,羰基铁的结构如图,根据该图可知CO作为配位体是以__________ 原子为配位原子与Fe原子结合。

(3)离子水化能是气态离子溶于大量水中成为无限稀释溶液时释放的能量。离子在溶液中的稳定性可以从离子的大小、电荷、水化能等因素来解释。Cu2+和Cu+的水化能分别是-2121kJ·mol-1和-582 kJ·mol-1,在水溶液里Cu2+比Cu+稳定的原因是_______________________________ 。[Cu(NH3)2]+在水溶液中相对稳定,在配合物[Cu(NH3)2]Ac中碳原子的杂化类型是________________________________ 。
(4)用[Cu(NH3)2]Ac除去CO的反应中,肯定有形成________________ 。
a.离子键 b.配位键 c.非极性键 d. σ键
(5)钙铜合金的晶体结构可看成(a) (b) 两种原子层交替堆积排列而成图(c),则该合金六方晶胞(即平行六面体晶胞)中含为Cu________ 个。已知同层的Ca-Cu的距离为294pm,根据图示求同层相邻Ca-Ca的距离__________ pm (已知 =1.73 计算结果保留整数)。
=1.73 计算结果保留整数)。

(1)C、N、O的第一电离能最大的是
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是

(3)离子水化能是气态离子溶于大量水中成为无限稀释溶液时释放的能量。离子在溶液中的稳定性可以从离子的大小、电荷、水化能等因素来解释。Cu2+和Cu+的水化能分别是-2121kJ·mol-1和-582 kJ·mol-1,在水溶液里Cu2+比Cu+稳定的原因是
(4)用[Cu(NH3)2]Ac除去CO的反应中,肯定有形成
a.离子键 b.配位键 c.非极性键 d. σ键
(5)钙铜合金的晶体结构可看成(a) (b) 两种原子层交替堆积排列而成图(c),则该合金六方晶胞(即平行六面体晶胞)中含为Cu
 =1.73 计算结果保留整数)。
=1.73 计算结果保留整数)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸铁铵[ Fe2(SO4)3•2(NH4)2SO4• 2H2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵,并测定产品纯度。
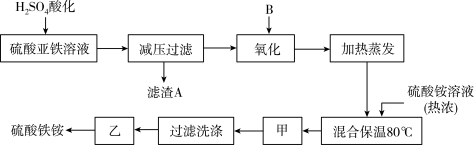
请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是__________ 。
(2)下列物质中最适合作为氧化剂B是_______ ;反应的离子方程式_______ 。
a.NaClO b. H2O2 c.KMnO4 d. K2Cr2O7
(3)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂为________ (写名称),能否用酸性的KMnO4溶液理由是:__________ 。
(4)检验硫酸铁铵中 的方法是
的方法是__________ 。
(5)取样品 7. 5 g 溶于水中,加入足量KI进行处理:加几滴淀粉溶液,然后用0.5 mol·L-1 Na2S2O3标准溶液进行滴定,消耗Na2S2O3溶液体积为 40.00 mL。
已知:2 + I2 = 2I- +
+ I2 = 2I- + 
①滴定终点的现象为_________ 。
②获得的产品纯度为_______ (保留三位有效数字)

请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是
(2)下列物质中最适合作为氧化剂B是
a.NaClO b. H2O2 c.KMnO4 d. K2Cr2O7
(3)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂为
(4)检验硫酸铁铵中
 的方法是
的方法是(5)取样品 7. 5 g 溶于水中,加入足量KI进行处理:加几滴淀粉溶液,然后用0.5 mol·L-1 Na2S2O3标准溶液进行滴定,消耗Na2S2O3溶液体积为 40.00 mL。
已知:2
 + I2 = 2I- +
+ I2 = 2I- + 
①滴定终点的现象为
②获得的产品纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】溴化亚铜可用作工业催化剂,是一种白色粉末,微溶于冷水,不溶于乙醇等有机溶剂,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:

步骤1.在如上图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去水中的________________ (写化学式)。
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为__________________ ;
②控制反应在60℃进行,实验中可采取的措施是____________________ ;
③说明反应已完成的现象是_____________________ 。
(3)步骤2过滤需要避光的原因是_____________________ 。
(4)步骤3中洗涤剂需“溶有SO2”的原因是____________________ 。
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。
请补充实验步骤[须用到SO2(贮存在钢瓶中)、20%NaOH溶液]:
①_________________ 。
②___________________ 。
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④过滤,用乙醇洗涤2~3次。⑤放真空干燥箱中干燥。

步骤1.在如上图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去水中的
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为
②控制反应在60℃进行,实验中可采取的措施是
③说明反应已完成的现象是
(3)步骤2过滤需要避光的原因是
(4)步骤3中洗涤剂需“溶有SO2”的原因是
(5)欲利用上述装置烧杯中的吸收液(经检测主要含Na2SO3、NaHSO3等)制取较纯净的Na2SO3·7H2O晶体。
请补充实验步骤[须用到SO2(贮存在钢瓶中)、20%NaOH溶液]:
①
②
③加入少量维生素C溶液(抗氧剂),蒸发浓缩,冷却结晶。
④过滤,用乙醇洗涤2~3次。⑤放真空干燥箱中干燥。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】某废钯催化剂主要含Pd、活性炭、SiO2、Al2O3、Fe3O4、CuO、ZnO。其一种回收利用工艺如图所示。回答相关问题。

(1)焙烧的目的_______ 。
(2)浸出后Pd以PdCl 形式存在,写出对应的离子方程式
形式存在,写出对应的离子方程式_______ 。
(3)已知Cu2+和Zn2+易与氨水形成Cu(NH3) 和Z(NH3)
和Z(NH3) ,则滤渣2的化学式为
,则滤渣2的化学式为_______ 。
(4)除杂后Pd以Pd(NH3) 形式存在,沉钯时得到的是(NH4)2PdCl4, 写出沉钯时对应的离子方程式
形式存在,沉钯时得到的是(NH4)2PdCl4, 写出沉钯时对应的离子方程式_______ 。
(5)若还原时生成1mol Pd,则理论上需要消耗N2H4的质量为_______ 。
(6)工业上制备乙醛是在PdCI2—CuCl2催化下用氧气氧化乙烯制备。写出该反应的化学方程式_______ 。 该反应过程复杂,可简单用下列3个反应表示,将反应②补齐。
①C2H4+ PdCl2+ H2O= CH3CHO+ Pd+2HCl
②_______ ;
③4CuCl+O2+4HCl=4CuCl2+2H2O

(1)焙烧的目的
(2)浸出后Pd以PdCl
 形式存在,写出对应的离子方程式
形式存在,写出对应的离子方程式(3)已知Cu2+和Zn2+易与氨水形成Cu(NH3)
 和Z(NH3)
和Z(NH3) ,则滤渣2的化学式为
,则滤渣2的化学式为(4)除杂后Pd以Pd(NH3)
 形式存在,沉钯时得到的是(NH4)2PdCl4, 写出沉钯时对应的离子方程式
形式存在,沉钯时得到的是(NH4)2PdCl4, 写出沉钯时对应的离子方程式(5)若还原时生成1mol Pd,则理论上需要消耗N2H4的质量为
(6)工业上制备乙醛是在PdCI2—CuCl2催化下用氧气氧化乙烯制备。写出该反应的化学方程式
①C2H4+ PdCl2+ H2O= CH3CHO+ Pd+2HCl
②
③4CuCl+O2+4HCl=4CuCl2+2H2O
您最近一年使用:0次



