利用锌灰(主要成分为ZnO,含有CuO、PbO、SiO2、FeO、Fe2O3等杂质)制备高纯ZnO的工艺流程如图:

下列说法错误的是

下列说法错误的是
| A.滤渣1的成分只有SiO2 |
| B.加入的试剂a可为Zn,目的是除去Cu2+ |
C.步骤1中发生反应的离子方程式为MnO +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ +3Fe3++7H2O=3Fe(OH)3↓+MnO2↓+5H+ |
| D.若取步骤3后的干燥滤饼11.2g煅烧,得到产品8.1g,则x=2 |
更新时间:2023-02-11 11:09:52
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】磷酸银可用于光催化降解含有机物的污水,一段时间后,溶液变为浅的棕黑色,磷酸银催化效果降低。实验室制备少量磷酸银的工艺流程如下:

已知:① ;
;
②常温时, 。
。
下列说法正确的是

已知:①
 ;
;②常温时,
 。
。下列说法正确的是
A.银氨溶液中的平衡: |
B.“析银”离子方程式: |
| C.“离心沉淀”所得母液中有两种溶质 |
| D.磷酸银催化失效的原因可能是光照分解生成Ag |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如下图所示。下列说法不正确的是
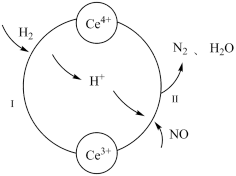

| A.反应Ⅰ的离子方程式为2Ce4++H2= 2Ce3++2H+ |
| B.反应Ⅱ中氧化剂与还原剂的物质的量之比为2∶1 |
| C.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+) |
| D.反应过程中混合溶液内Ce3+和Ce4+的总数一定保持不变 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列反应的离子方程式不正确 的是_______ 。
A.(2022·全国甲卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O
=BaSO4↓+2H2O
B.(2020·全国Ⅲ卷)同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3·H2O
+OH-=NH3·H2O
C.(2014·大纲版全国卷)等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-=Mg(OH)2↓
D.1mol/L的NaAlO2溶液与2.5mol/L的HCl溶液等体积混合2AlO +5H+=Al3++Al(OH)3↓+H2O
+5H+=Al3++Al(OH)3↓+H2O
E.将等浓度的Ba(OH)2溶液与NaHSO4液按体积比2∶3混合:2Ba2++3OH-+3H++2SO =2BaSO4↓+3H2O
=2BaSO4↓+3H2O
A.(2022·全国甲卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
 =BaSO4↓+2H2O
=BaSO4↓+2H2OB.(2020·全国Ⅲ卷)同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH
 +OH-=NH3·H2O
+OH-=NH3·H2OC.(2014·大纲版全国卷)等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-=Mg(OH)2↓
D.1mol/L的NaAlO2溶液与2.5mol/L的HCl溶液等体积混合2AlO
 +5H+=Al3++Al(OH)3↓+H2O
+5H+=Al3++Al(OH)3↓+H2OE.将等浓度的Ba(OH)2溶液与NaHSO4液按体积比2∶3混合:2Ba2++3OH-+3H++2SO
 =2BaSO4↓+3H2O
=2BaSO4↓+3H2O
您最近一年使用:0次
【推荐1】已知反应:①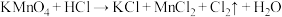
② 、
、
③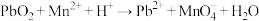 (方程式均未配平)。
(方程式均未配平)。
下列说法不正确的是
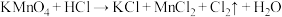
②
 、
、③
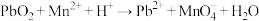 (方程式均未配平)。
(方程式均未配平)。下列说法不正确的是
A.反应③中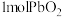 参加反应转移电子2mol 参加反应转移电子2mol |
B.反应①中氧化剂与参与反应的HCl的物质的量之比为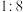 |
C.上述反应中,还原性由强到弱顺序: 、 、 、 、 |
D.反应①和②中消耗相同物质的量的 和 和 时,生成 时,生成 的物质的量之比为 的物质的量之比为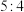 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】用如图所示的装置分别进行如下实验,各离子方程式正确及各组物质反应后,溶液的导电性比反应前增强的是( )


| A.向硝酸银溶液中通入少量氯化氢:Ag++Cl-=AgCl↓ |
| B.向亚硫酸溶液中通入氯气:H2SO3+C12+H2O=SO42-+4H++2Cl- |
| C.向FeBr2溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| D.向NaOH溶液中通入少量氯气:2OH-+Cl2=Cl-+ClO-+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
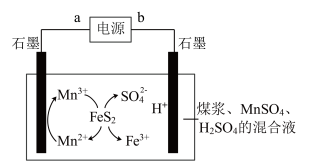
【推荐3】应用电解法对煤电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化成Mn3+,Mn3+再将煤中的含硫物质(主要是FeS2)氧化为Fe3+和SO 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
| A.根据信息推断,a为电源正极 |
| B.整个电解脱硫过程与b连接的石墨电极只发生电极反应2H++2e-=H2↑ |
| C.电解过程中,H+不断消耗,混合溶液的pH逐渐升高 |
D.混合液中发生反应的离子方程式为FeS2+15Mn3++8H2O=Fe3++15Mn2++2SO +16H+ +16H+ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂拟综合处理含NH 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
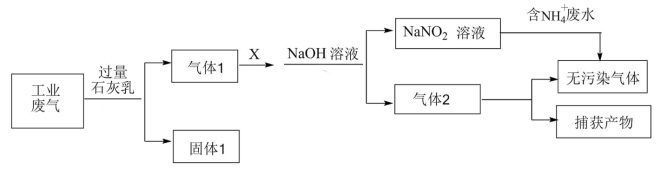
已知: 2NaOH+ NO+NO2 = 2NaNO2+H2O、2NaOH + 2NO2=NaNO3 + NaNO2+H2O。
下列说法正确的是
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
已知: 2NaOH+ NO+NO2 = 2NaNO2+H2O、2NaOH + 2NO2=NaNO3 + NaNO2+H2O。
下列说法正确的是
| A.固体1中只含有CaCO3、CaSO3 |
| B.X可以是空气,且需过量 |
| C.捕获剂所捕获的气体主要是CO |
D.含NH 废水在该流程中作还原剂 废水在该流程中作还原剂 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】工业上以菱镁矿(主要成分为 ,含少量
,含少量 ,
, 和
和 )为原料制备高纯镁砂的工艺流程如下:
)为原料制备高纯镁砂的工艺流程如下:
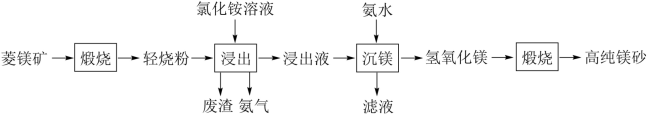
下列说法错误的是
 ,含少量
,含少量 ,
, 和
和 )为原料制备高纯镁砂的工艺流程如下:
)为原料制备高纯镁砂的工艺流程如下:
下列说法错误的是
A.浸出时产生的废渣灼烧后有 , , 和 和 |
B.浸出镁的离子反应为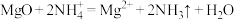 |
| C.浸出镁的过程应在较高温度下进行,沉镁的操作在较低温度下进行 |
D.流程中可循环使用的物质只有 |
您最近一年使用:0次

 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、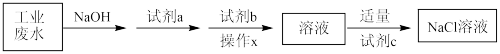
 、
、 等)为原料制备氧化锌的工艺流程如下:
等)为原料制备氧化锌的工艺流程如下: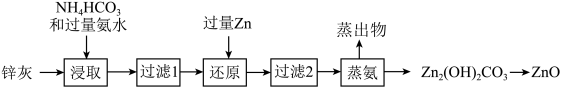
 的离子方程式为
的离子方程式为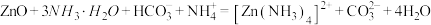
 、
、


