已知反应:①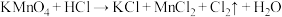
② 、
、
③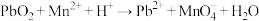 (方程式均未配平)。
(方程式均未配平)。
下列说法不正确的是
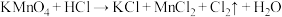
②
 、
、③
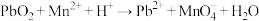 (方程式均未配平)。
(方程式均未配平)。下列说法不正确的是
A.反应③中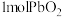 参加反应转移电子2mol 参加反应转移电子2mol |
B.反应①中氧化剂与参与反应的HCl的物质的量之比为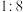 |
C.上述反应中,还原性由强到弱顺序: 、 、 、 、 |
D.反应①和②中消耗相同物质的量的 和 和 时,生成 时,生成 的物质的量之比为 的物质的量之比为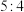 |
更新时间:2023-12-17 20:49:17
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】已知:5PbO2+2Mn2++4H+= 5Pb2++ 2MnO4-+2H2O,下列说法正确的是
| A.PbO2为还原剂,具有还原性 | B.氧化剂与还原剂的物质的量之比为2∶5 |
| C.生成1mol的Pb2+,转移的电子为2mol | D.酸性环境下PbO2的氧化性强于MnO4- |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知Pb3O4与HNO3溶液发生反应I:Pb3O4+4H+=PbO2+2Pb2++2H2O;PbO2与酸化的MnSO4溶液发生反应II:5PbO2+2Mn2++4H++5SO =2MnO
=2MnO +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是
 =2MnO
=2MnO +5PbSO4+2H2O。下列推断正确的是
+5PbSO4+2H2O。下列推断正确的是| A.由反应I可知,Pb3O4中Pb(II)和Pb(IV)含量之比为1:2 |
| B.由反应I可知氧化性:PbO2>HNO3 |
| C.由反应II可知,Pb3O4可与盐酸发生反应:Pb3O4+8HCl=3PbCl2+4H2O+Cl2↑ |
| D.由反应II可知,每生成1 mol PbSO4转移10 mol电子 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】检验加“碘”盐含“KIO3”可通过在酸性条件下,加入碘化钾溶液和淀粉来实现。反应原理如下:KIO3+KI+HCl―→I2+KCl+H2O(未配平)。下列有关说法正确的是
| A.KI是还原剂 |
| B.KIO3被氧化 |
| C.该反应配平后化学计量数依次为:1、5、6、3、6、3 |
| D.每生成3个I2分子,转移6个电子 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况。下列反应中属于这种情况的是
| A.过量的MnO2与浓盐酸反应 | B.过量的Zn与18 mol/L的硫酸反应 |
| C.过量的Br2与FeI2反应 | D.过量的H2与N2在催化剂存在下反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】高倩同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: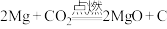 。下列关于该反应的判断正确的是
。下列关于该反应的判断正确的是
 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: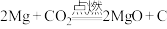 。下列关于该反应的判断正确的是
。下列关于该反应的判断正确的是A. 元素化合价由0价升高到+2价, 元素化合价由0价升高到+2价, 是还原产物 是还原产物 |
B.由此反应可以判断氧化性: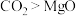 ,还原性: ,还原性: |
C. 作氧化剂,表现氧化性,发生氧化反应 作氧化剂,表现氧化性,发生氧化反应 |
D. 原子失去的电子数目等于氧原子得到的电子数目 原子失去的电子数目等于氧原子得到的电子数目 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】PbO2是褐色固体,受热分解为氧气和Pb的+4价和+2价混合氧化物,+4价的Pb能氧化浓盐酸为Cl2,现将1个PbO2加热分解,向剩余固体中加入足量的浓盐酸得到Cl2,其中,O2与Cl2的个数比为3:2,则剩余固体的组成及个数比可能为:
| A.1:1混合的Pb3O4、PbO | B.1:2 的混合的PbO2、Pb3O4 |
| C.1:4:1混合的PbO、Pb3O4、PbO2 | D.1:1:4混台的PbO2、Pb3O4、PbO |
您最近一年使用:0次

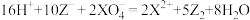
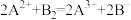
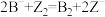
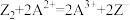
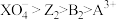
 是
是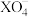 的氧化产物
的氧化产物 、
、 、Mn2+、H2O六种微粒。其中c(
、Mn2+、H2O六种微粒。其中c(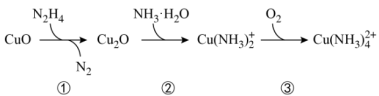
 +O2+8NH3·H2O=4Cu(NH3)
+O2+8NH3·H2O=4Cu(NH3) +4OH-+6H2O
+4OH-+6H2O

